Onglyza لعلاج مرض السكري
اسم العلامة التجارية: Onglyza
الاسم العام: سكساجلبتين
شكل جرعة: قرص ، فيلم المغلفة
محتويات:
مؤشرات والاستخدام
الجرعة والإدارة
أشكال الجرعات ونقاط القوة
موانع
المحاذير والإحتياطات
ردود الفعل السلبية
تفاعل الأدوية
استخدام في السكان محددة
جرعة زائدة
وصف
علم العقاقير
علم السموم غير الإكلينيكي
الدراسات السريرية
كيف زودت
معلومات المريض Onglyza (في سهل الانجليزية)
مؤشرات والاستخدام
وحيد والعلاج المختلط
يشار إلى Onglyza كعنصر مساعد في اتباع نظام غذائي وممارسة الرياضة لتحسين السيطرة على نسبة السكر في الدم لدى البالغين الذين يعانون من داء السكري من النوع 2. [نرى الدراسات السريرية].
القيود الهامة للاستخدام
لا ينبغي أن تستخدم Onglyza لعلاج داء السكري من النوع 1 أو الحماض الكيتوني السكري ، لأنه لن يكون فعالاً في هذه الإعدادات.
لم تتم دراسة Onglyza بالاشتراك مع الأنسولين.
أعلى
الجرعة والإدارة
الجرعات الموصى بها
الجرعة الموصى بها من Onglyza هي 2.5 ملغ أو 5 ملغ مرة واحدة تؤخذ يوميا بغض النظر عن وجبات الطعام.
المرضى الذين يعانون من القصور الكلوي
لا ينصح بتعديل جرعة Onglyza للمرضى الذين يعانون من اختلال كلوي خفيف (تصفية الكرياتينين [CrCl]> 50 مل / دقيقة).
جرعة Onglyza 2.5 ملغ مرة واحدة يوميا للمرضى الذين يعانون من ضعف كلوي معتدلة أو شديدة ، أو مع مرض الكلى في نهاية المرحلة (ESRD) التي تتطلب غسيل الكلى (تصفية الكرياتينين [CrCl] â ¤50 مل / دقيقة). وينبغي أن تدار Onglyza بعد غسيل الكلى. لم تتم دراسة Onglyza في المرضى الذين يخضعون لغسيل الكلى البريتوني.
نظرًا لأن جرعة Onglyza يجب أن تقتصر على 2.5 ملغ بناءً على وظيفة الكلى ، يوصى بتقييم وظيفة الكلى قبل بدء Onglyza وبعد ذلك بشكل دوري. يمكن تقدير وظيفة الكلى من كرياتينين المصل باستخدام صيغة Cockcroft-Gault أو تعديل النظام الغذائي في صيغة مرض الكلى. [نرى علم الصيدلة السريرية، الدوائية.]
مثبطات قوية CYP3A4 / 5
جرعة Onglyza هي 2.5 ملغ مرة واحدة يوميًا عندما تترافق مع مثبطات السيتوكروم القوية P450 3A4 / 5 (CYP3A4 / 5) (على سبيل المثال ، كيتوكونازول ، أتزانافير ، كلاريثروميسين ، إندينافير ، إيتراكونازول ، نيفازودون ، نلفينافير ، ريتونافير ، ساكوينافير ، و telithromycin). [نرى تفاعل الأدويةمثبطات الانزيمات CYP3A4 / 5 علم الصيدلة السريرية، الدوائية.]
أعلى
أشكال الجرعات ونقاط القوة
- أقراص Onglyza (saxagliptin) 5 ملغ هي أقراص وردية ، biconvex ، دائرية ، مغلفة بالأفلام مع طباعة "5" على جانب واحد و "4215" مطبوعة على الجانب الخلفي ، بالحبر الأزرق.
- أقراص Onglyza (saxagliptin) 2.5 ملغ هي أصفر باهت إلى أصفر فاتح ، biconvex ، أقراص دائرية ، مغلفة بالفيلم مع "2.5" مطبوعة على جانب واحد و "4214" مطبوعة على الجانب الخلفي ، بالحبر الأزرق.
أعلى
موانع
لا شيء.
أعلى
المحاذير والإحتياطات
استخدم مع الأدوية المعروفة لتسبب نقص السكر في الدم
إفرازات الأنسولين ، مثل السلفونيل يوريا ، تسبب نقص السكر في الدم. لذلك ، قد تكون هناك حاجة لجرعة أقل من إفراز الأنسولين لتقليل خطر نقص السكر في الدم عند استخدامه مع Onglyza. [نرى ردود الفعل السلبيةتجربة التجارب السريرية.]
نتائج الاوعية الدموية الكبيرة
لم تكن هناك دراسات سريرية تؤكد وجود أدلة قاطعة على الحد من مخاطر الأوعية الدموية الكبرى باستخدام Onglyza أو أي دواء آخر مضاد لمرض السكر.
أعلى
ردود الفعل السلبية
تجارب التجارب السريرية
لأن التجارب السريرية تجرى في ظل ظروف متباينة على نطاق واسع ، لوحظت معدلات رد فعل سلبية في التجارب السريرية ل لا يمكن مقارنة الدواء مباشرة بالمعدلات في التجارب السريرية لعقار آخر وقد لا يعكس المعدلات التي لوحظت فيها ممارسة.
وحيد العلاج والجمع بين العلاج
في تجربتين للعلاج بالعلاج الوهمي يتم التحكم فيهما لمدة 24 أسبوعًا ، تم علاج المرضى باستخدام Onglyza 2.5 ملغ يوميًا ، و Onglyza 5 ملغ يوميًا ، وهمي. كما تم إجراء ثلاث تجارب علاجية مدمجة على مدار 24 أسبوعًا يتم التحكم فيها بالعلاج الوهمي: واحدة مع الميتفورمين ، وواحدة مع ثيازوليدينيديون (بيوغليتازون أو روسيجليتازون) ، وواحدة مع غليبوريد. في هذه التجارب الثلاث ، تم اختيار المرضى بشكل عشوائي للعلاج الإضافي مع Onglyza 2.5 ملغ يوميًا ، Onglyza 5 ملغ يوميًا ، أو وهمي. تم تضمين ذراع معالجة ساكساجليبتين 10 ملغ في إحدى تجارب العلاج الأحادي وفي تجربة الجمع الإضافي مع الميتفورمين.
في تحليل مُجمَّع محدد مسبقًا للبيانات التي مدتها 24 أسبوعًا (بغض النظر عن إنقاذ نسبة السكر في الدم) من تجربتي العلاج الأحادي ، الإضافة إلى تجربة الميتفورمين ، الإضافة إلى تجربة الثيازوليدينيديون (TZD) ، والإضافة إلى تجربة glyburide ، كان إجمالي حدوث الأحداث الضائرة في المرضى الذين عولجوا مع Onglyza 2.5 mg و Onglyza 5 mg مشابهًا للعلاج الوهمي (72.0٪ و 72.2٪ مقابل 70.6٪ ، على التوالي). حدث وقف العلاج بسبب الأحداث السلبية في 2.2 ٪ ، 3.3 ٪ ، و 1.8 ٪ من المرضى الذين يتلقون Onglyza 2.5 ملغ ، Onglyza 5 ملغ ، وهمي ، على التوالي. الأحداث الضائرة الأكثر شيوعًا (تم الإبلاغ عنها في ما لا يقل عن 2 مريض عولجوا بـ Onglyza 2.5 ملغ أو على الأقل 2 من المرضى الذين عولجوا مع Onglyza 5 ملغ) المرتبطة بالتوقف المبكر لأوانه من العلاج شملت ليمفوبيا (0.1 ٪ و 0.5 ٪ مقابل 0 ٪ ، على التوالي) ، طفح (0.2 ٪ و 0.3 ٪ مقابل 0.3 ٪) ، زاد الكرياتينين في الدم (0.3 ٪ و 0 ٪ مقابل 0 ٪) ، وزيادة فسفوكيناز الدم (0.1 ٪ و 0.2 ٪ مقابل 0%). ردود الفعل السلبية في هذا التحليل المجمع ذكرت (بغض النظر عن تقييم المحقق من السببية) في ¥٪٪ 5٪ من المرضى الذين عولجوا بـ Onglyza 5 mg ، والأكثر شيوعًا من المرضى الذين عولجوا بالعلاج الوهمي مبينون في الجدول 1.
الجدول 1: ردود الفعل السلبية (بغض النظر عن تقييم الباحث عن السببية) في التجارب التي تسيطر عليها وهمي * تم الإبلاغ عنه في 5٪ من المرضى الذين عولجوا بـ Onglyza 5 mg وأكثر شيوعًا من المرضى الذين عولجوا بـ الوهمي
| عدد (٪) من المرضى | ||
|---|---|---|
| Onglyza 5 ملغ N = 882 |
الوهمي N = 799 |
|
| * تشمل التجارب الخمسة التي يتم التحكم فيها بالعلاج الوهمي تجربتين أحاديتين وتجربة واحدة للعلاج المركب الإضافي مع كل من الآتي: الميتفورمين ، الثيازيدوليدين ، أو الغليبيريد. يُظهر الجدول بيانات لمدة 24 أسبوعًا بغض النظر عن إنقاذ نسبة السكر في الدم. | ||
| عدوى الجهاز التنفسي العلوي | 68 (7.7) | 61 (7.6) |
| التهاب المسالك البولية | 60 (6.8) | 49 (6.1) |
| صداع الراس | 57 (6.5) | 47 (5.9) |
في المرضى الذين عولجوا بـ Onglyza 2.5 mg ، كان الصداع (6.5٪) هو رد الفعل السلبي الوحيد المبلغ عنه بمعدل 5٪ وأكثر شيوعًا من المرضى الذين عولجوا بالعلاج الوهمي.
في هذا التحليل المجمع ، تضمنت ردود الفعل السلبية التي تم الإبلاغ عنها في 2٪ من المرضى الذين عولجوا Onglyza 2.5 ملغ أو Onglyza 5 ملغ و 1٪ أكثر تكرارًا مقارنةً بالعلاج الوهمي: التهاب الجيوب الأنفية (2.9 ٪ و 2.6 ٪ مقابل 1.6 ٪ ، على التوالي) ، وآلام في البطن (2.4 ٪ و 1.7 ٪ مقابل 0.5 ٪) ، والتهاب المعدة والأمعاء (1.9 ٪ و 2.3 ٪ مقابل 0.9 ٪) ، والقيء (2.2 ٪ و 2.3 ٪ مقابل 1.3 ٪ ).
في الإضافة إلى تجربة TZD ، كانت نسبة حدوث الوذمة المحيطية أعلى عند Onglyza 5 mg مقابل الدواء الوهمي (8.1٪ و 4.3٪ على التوالي). كانت نسبة حدوث الوذمة المحيطية عند Onglyza 2.5 mg 3.1٪. أيا من ردود الفعل السلبية ذكرت من وذمة محيطية أدى إلى التوقف عن دراسة المخدرات. كانت معدلات الوذمة المحيطية لكل من Onglyza 2.5 mg و Onglyza 5 mg مقابل الدواء الوهمي هي 3.6٪ و 2٪ مقابل 3٪ تعطى كعلاج وحيد ، 2.1 ٪ و 2.1 ٪ مقابل 2.2 ٪ تعطى كعلاج إضافي للميتفورمين ، و 2.4 ٪ و 1.2 ٪ مقابل 2.2 ٪ تعطى كعلاج إضافي ل غليبوريد.
كان معدل الإصابة من الكسور 1.0 و 0.6 لكل 100 سنة من المرضى ، على التوالي ، ل Onglyza (تحليل مجمعة من 2.5 ملغ ، 5 ملغ ، و 10 ملغ) وهمي. لم يزداد معدل الإصابة بأحداث الكسر في المرضى الذين تلقوا Onglyza بمرور الوقت. لم تثبت العلاقة السببية ولم تثبت الدراسات غير السريرية آثارًا ضارة لساكساجليبتين على العظام.
وقد لوحظ وجود حدث من نقص الصفيحات ، بما يتفق مع تشخيص فرفرية نقص الصفيحات مجهول السبب ، في البرنامج السريري. علاقة هذا الحدث بـ Onglyza غير معروفة.
ردود الفعل السلبية المرتبطة مع Onglyza Coadministered مع الميتفورمين في مرضى ساذج العلاج مع مرض السكري من النوع 2
يوضح الجدول 2 ردود الفعل السلبية المبلغ عنها (بغض النظر عن تقييم الباحث للسببية) في 5٪ من المرضى المشاركة في تجربة إضافية نشطة لمدة 24 أسبوعًا من Onglyza coadministered و metformin في علاج ساذج المرضى.
الجدول 2: العلاج الأولي مع مزيج من Onglyza والميتفورمين في علاج المرضى ساذج: ردود الفعل السلبية المبلغ عنها (بغض النظر عن تقييم المحقق السببية) في٪٪ 5 ٪ من المرضى الذين عولجوا بالعلاج المركب لـ Onglyza 5 mg Plus Metformin (وأكثر شيوعًا من المرضى الذين عولجوا بالميتفورمين وحده)
| عدد (٪) من المرضى | ||
|---|---|---|
| Onglyza 5 ملغ + ميتفورمين * N = 320 |
الميتفورمين * N = 328 |
|
| * تم بدء استخدام الميتفورمين بجرعة تبدأ من 500 ملغ يوميًا وتم معايرتها بحد أقصى 2000 ملغ يوميًا. | ||
| صداع الراس | 24 (7.5) | 17 (5.2) |
| البلعوم الأنفي | 22 (6.9) | 13 (4.0) |
نقص سكر الدم
استندت ردود الفعل السلبية لنقص السكر في الدم على جميع تقارير نقص السكر في الدم. لم يكن قياس الجلوكوز المتزامن مطلوبًا. في دراسة الإضافة إلى الغليبيريد ، كان معدل الإصابة بنقص السكر في الدم المُبلغ عنه أعلى عند Onglyza 2.5 mg و Onglyza 5 mg (13.3٪ و 14.6٪) مقابل الغفل (10.1٪). الإصابة بنقص السكر في الدم المؤكدة في هذه الدراسة ، والمعروفة باسم أعراض نقص السكر في الدم المصحوب ب بلغت قيمة جلوكوز الأصابع البالغة 50 ملغ / ديسيلتر ، 2.4٪ و 0.8٪ بالنسبة لـ Onglyza 2.5 mg و Onglyza 5 mg و 0.7٪ لـ الوهمي. كانت نسبة حدوث نقص السكر في الدم المبلغ عنها لأونغيليزا 2.5 ملغ وأونجليزا 5 ملغ مقابل الدواء الوهمي المعطى كعلاج وحيد 4.0 ٪ و 5.6 ٪ مقابل 4.1 ٪ ، على التوالي ، 7.8 ٪ و 5.8 ٪ مقابل 5 ٪ تعطى كعلاج إضافي للميتفورمين ، و 4.1 ٪ و 2.7 ٪ مقابل 3.8 ٪ تعطى كعلاج إضافي ل TZD. كانت نسبة حدوث نقص السكر في الدم المبلغ عنها 3.4 ٪ في المرضى الذين يعانون من العلاج ساذج تعطى Onglyza 5 ملغ زائد الميتفورمين و 4.0 ٪ في المرضى الذين يتناولون الميتفورمين وحده.
تفاعلات فرط الحساسية
الأحداث المتعلقة بفرط الحساسية ، مثل الشرى وذمة الوجه في التحليل المجمَّع المكون من 5 دراسات حتى الأسبوع 24 تم الإبلاغ عن 1.5 ٪ و 1.5 ٪ و 0.4 ٪ من المرضى الذين تلقوا Onglyza 2.5 ملغ ، Onglyza 5 ملغ ، وهمي ، على التوالي. لم تتطلب أي من هذه الأحداث في المرضى الذين تلقوا Onglyza دخول المستشفى أو تم الإبلاغ عن تهديد حياتهم من قبل المحققين. توقف أحد المرضى المعالجين بسكساجليبتين في هذا التحليل المجمع بسبب الشرى المعمم وذمة الوجه.
علامات حيوية
لم يلاحظ أي تغييرات ذات مغزى سريري في العلامات الحيوية في المرضى الذين عولجوا مع Onglyza.
اختبارات المعمل
عدد الخلايا اللمفاوية المطلقة
كان هناك انخفاض مرتبط بالجرعة في عدد الخلايا اللمفاوية المطلقة التي لوحظت مع Onglyza. من خط الأساس يعني عدد الخلايا اللمفاوية المطلق لحوالي 2200 خلية / ميكرول ، يعني نقصان حوالي 100 و 120 خلية / ميكرول مع وقد لوحظت Onglyza 5 ملغ و 10 ملغ ، على التوالي ، مقارنةً بالعلاج الوهمي في 24 أسبوعًا في تحليل مُجمَّع لخمس تجارب سريرية يتم التحكم فيها بالغفل. دراسات. وقد لوحظت آثار مماثلة عندما أعطيت Onglyza 5 ملغ في تركيبة أولية مع الميتفورمين مقارنة مع الميتفورمين وحده. لم يكن هناك اختلاف لوحظ ل Onglyza 2.5 ملغ مقارنة مع الدواء الوهمي. كانت نسبة المرضى الذين أبلغوا عن وجود عدد من الخلايا اللمفاوية ¤ cells 750 خلية / microL 0.5 ٪ ، 1.5 ٪ ، 1.4 ٪ ، و 0.4 ٪ في ساكساجليبتين 2.5 ملغ ، 5 ملغ ، 10 ملغ ، وهمي مجموعات ، على التوالي. في معظم المرضى ، لم يلاحظ التكرار مع التعرض المتكرر لأونجليزا على الرغم من أن بعض المرضى كانوا يعانون من نقصان متكرر عند إعادة التأهيل مما أدى إلى توقف Onglyza. لم ترتبط انخفاض في عدد الخلايا اللمفاوية مع ردود الفعل السلبية ذات الصلة سريريا.
الأهمية السريرية لهذا الانخفاض في عدد الخلايا اللمفاوية بالنسبة للعلاج الوهمي غير معروفة. عند الإشارة سريريًا ، كما هو الحال في حالات الإصابة غير العادية أو الطويلة ، يجب قياس عدد الخلايا اللمفاوية. تأثير Onglyza على تعداد الخلايا اللمفاوية في المرضى الذين يعانون من تشوهات الخلايا اللمفاوية (على سبيل المثال ، فيروس نقص المناعة البشرية) غير معروف.
الصفائح
لم يُظهر Onglyza أي تأثير ذي معنى سريريًا أو ثابتًا على تعداد الصفائح الدموية في تجارب السلامة والفعالية الإكلينيكية الستة مزدوجة التعمية التي يتم التحكم فيها.
أعلى
تفاعل الأدوية
محرضات الانزيمات CYP3A4 / 5
Rifampin انخفض بشكل ملحوظ التعرض ساكساجليبتين مع عدم وجود تغيير في المنطقة تحت منحنى تركيز الوقت (AUC) من المستقلب النشط لها ، ساكساجليبتين 5-هيدروكسي. لم يتأثر تثبيط النشاط dipeptidyl peptidase-4 (DPP4) على مدى فاصل زمني لمدة 24 ساعة بالريفامبين. لذلك ، لا ينصح تعديل جرعة Onglyza. [نرى علم الصيدلة السريرية، الدوائية.]
مثبطات إنزيمات CYP3A4 / 5
مثبطات متوسطة من CYP3A4 / 5
زاد الديلتيازيم من التعرض لسكساجليبتين. من المتوقع حدوث زيادات مماثلة في تركيزات ساكساجليبتين في البلازما في وجود CYP3A4 / 5 معتدلة أخرى مثبطات (على سبيل المثال ، amprenavir ، aprepitant ، erythromycin ، فلوكونازول ، fosamprenavir ، عصير الجريب فروت ، وفيراباميل) ؛ ومع ذلك ، لا ينصح تعديل جرعة Onglyza. [نرى علم الصيدلة السريرية، الدوائية.]
مثبطات قوية من CYP3A4 / 5
الكيتوكونازول زيادة كبيرة في التعرض لساكساجليتين. زيادات كبيرة مماثلة في تركيزات البلازما من ساكساجليبتين مع غيرها من مثبطات قوية CYP3A4 / 5 (على سبيل المثال ، أتازانافير ، كلاريثروميسين ، إندينافير ، إيتراكونازول ، نيفازودون ، نلفينافير ، ريتونافير ، ساكوينافير ، و telithromycin). يجب أن تقتصر جرعة Onglyza على 2.5 ملغ عندما يتم مشاركتها مع مثبط قوي CYP3A4 / 5. [نرى الجرعة والإدارة، قوي CYP3A4 / 5 مثبطات و علم الصيدلة السريرية، الدوائية.]
أعلى
استخدام في السكان محددة
حمل
الحمل الفئة ب
لا توجد دراسات كافية وتسيطر عليها بشكل جيد في النساء الحوامل. نظرًا لأن دراسات تكاثر الحيوانات لا تنبئ دائمًا بالاستجابة البشرية ، يجب استخدام Onglyza ، مثل الأدوية المضادة لمرض السكر ، أثناء الحمل فقط إذا لزم الأمر بشكل واضح.
لم يكن Saxagliptin ماسخًا في أي جرعة تم اختبارها عند إعطائه للفئران والأرانب الحوامل أثناء فترات تكوين الأعضاء. حدث التعظم غير الكامل للحوض ، وهو شكل من أشكال التأخر في النمو ، في الفئران بجرعة 240 ملغ / كغ ، أو حوالي 1503 و 66 مرة التعرض البشري لساكساجليبتين والمستقلب النشط ، على التوالي ، في الجرعة البشرية الموصى بها القصوى (MRHD) من 5 ملغ. وقد لوحظت سمية الأم وانخفاض أوزان جسم الجنين في 7986 و 328 أضعاف التعرض البشري في MRHD لساكساجليتين والمستقلب النشط ، على التوالي. حدثت اختلافات طفيفة في الهيكل العظمي في الأرانب بجرعة سامة من الأمهات قدرها 200 مغ / كغ ، أو ما يقرب من 1432 و 992 مرة من MRHD. عند تناوله في الفئران بالاقتران مع الميتفورمين ، لم يكن ساكساجليبتين ماسخًا ولا جنينيًا عند التعرض 21 مرة لساكساجلبتين MRHD. توليفة إدارة الميتفورمين مع جرعة أعلى من ساكساجليبتين (109 أضعاف الساكساجلبتين MRHD) ارتبطت آلام القحف العصبية (عيب نادر في الأنبوب العصبي يتميز بإغلاق غير كامل للجمجمة والعمود الفقري) في جنينين من سد واحد. كانت التعرض للميتفورمين في كل مجموعة 4 مرات التعرض البشري من 2000 ملغ يوميا.
نتج عن تناول ساكساجليبتين للفئران من يوم الحمل 6 إلى يوم الرضاعة 20 انخفاض أوزان الجسم عند الذكور و ذرية الإناث فقط عند تناول جرعات سامة للأم (التعرضات 1629 و 53 مرة ساكساجليبتين ومستقلبه النشط في MRHD). لم يلاحظ أي سمية وظيفية أو سلوكية في ذرية الفئران تدار ساكساجليتين في أي جرعة.
يعبر ساكساجليبتين المشيمة إلى الجنين بعد الجرعات في الفئران الحامل.
الأمهات المرضعات
يفرز ساكساجليبتين في لبن الفئران المرضعة بنسبة 1: 1 تقريبًا بتركيزات عقار البلازما. من غير المعروف ما إذا كان ساكساجليبتين يفرز في حليب الإنسان. نظرًا لإفراز العديد من الأدوية في اللبن البشري ، يجب توخي الحذر عند إعطاء Onglyza لمرضعة.
استخدام الأطفال
لم تثبت سلامة وفعالية Onglyza في مرضى الأطفال.
استخدام المسنين
في التجارب الستة التي أجريت على 6 أشخاص (15.3٪) من 4148 مريضًا العشوائي ، كانت تجارب السلامة والأمان السريرية التي خضعت للتحكم ، والتي تمت مراقبتها ، على 65 عامًا فأكثر ، وبلغ 59 مريضًا (1.4٪) 75 عامًا فأكثر. لم يلاحظ وجود فروق شاملة في السلامة أو الفعالية بين المرضى الذين تبلغ أعمارهم 65 عامًا والمرضى الأصغر سناً. في حين أن هذه التجربة السريرية لم تحدد الاختلافات في الاستجابات بين كبار السن والمرضى الأصغر سنا ، لا يمكن استبعاد حساسية أكبر لبعض الأفراد الأكبر سنا.
يتم التخلص من ساكساجليبتين والمستقلب النشط في جزء منه عن طريق الكلى. لأن المرضى المسنين هم أكثر عرضة لانقاص وظائف الكلى ، يجب توخي الحذر عند اختيار الجرعة لدى المسنين بناءً على وظائف الكلى. [نرى الجرعة والإدارة، المرضى الذين يعانون من القصور الكلوي و علم الصيدلة السريرية، الدوائية.]
أعلى
جرعة زائدة
في تجربة سريرية مسيطر عليها ، مرة واحدة يوميًا ، Onglyza التي تدار عن طريق الفم في موضوعات صحية بجرعات تصل إلى 400 ملغ يوميًا لمدة أسبوعين (80 مرة من MRHD) لم يكن لها أي ردود فعل سلبية سريرية مرتبطة بالجرعة وليس لها أي تأثير ذي معنى سريريًا على فترة QTc أو القلب معدل.
في حالة تناول جرعة زائدة ، يجب بدء العلاج الداعم المناسب كما تمليه الحالة السريرية للمريض. تتم إزالة Saxagliptin ومستقلبه النشط عن طريق غسيل الكلى (23 ٪ من الجرعة على مدى 4 ساعات).
أعلى
وصف
Saxagliptin هو المانع نشط عن طريق الفم من انزيم DPP4.
يوصف ساكساجليبتين أحادي الهيدرات كيميائياً بأنه (1S ، 3S ، 5S) -2 - [(2S) -2-أمينو -2- (3-هيدروكسيستريكلو] [3.3.1.13,7] dec-1-yl) acetyl] -2-azabicyclo [3.1.0] hexane-3-carbonitrile، monohydrate or (1S، 3S، 5S) - 2 - [(2S) - 2 - Amino - 2 - (3 - hydroxyadamantan - 1 - yl) acetyl] - 2 - azabicyclo [3.1.0] hexane - 3 - carbonitrile هيدرات. الصيغة التجريبية هي C18H25ن3O2-H2والوزن الجزيئي هو 333.43. الصيغة الهيكلية هي:
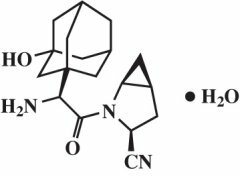
ساكساجلبتين أحادي الهيدرات مسحوق أبيض إلى أصفر فاتح أو بني فاتح ، غير رطب ، مسحوق بلوري. وهو قابل للذوبان في الماء على درجة حرارة منخفضة 24 درجة مئوية ± 3 درجة مئوية ، قابل للذوبان بشكل طفيف في أسيتات الإيثيل ، وقابل للذوبان في الميثانول والإيثانول وكحول الأيزوبروبيل والأسيتونيتريل والأسيتون والبولي إيثيلين غليكول 400 (PEG 400).
يحتوي كل قرص مضغوط بغشاء من Onglyza للاستخدام عن طريق الفم على 2.79 ملغ من ساكساجليبتين هيدروكلوريد (لا مائي) أي ما يعادل 2.5 ملغ من ساكساجليبتين أو 5.58 ملغ من ساكساجليبتين هيدروكلوريد (لا مائي) يعادل 5 ملغ ساكساجليبتين والمكونات غير النشطة التالية: اللاكتوز أحادي الهيدرات ، السليلوز الجريزوفولفين ، الصوديوم كروسكارميلوز ، و ستيرات المغنيسيوم. بالإضافة إلى ذلك ، يحتوي طلاء الفيلم على المكونات غير النشطة التالية: كحول بولي فينيل ، بولي إيثيلين جليكول ، ثاني أكسيد التيتانيوم ، التلك ، وأكسيدات الحديد.
أعلى
علم الصيدلة السريرية
آلية العمل
زيادة تركيزات هرمونات incretin مثل الببتيد -1 الشبيه بالجلوكاجون (GLP-1) والمعتمد على الجلوكوز يتم إطلاق بولي ببتيد الأنسولين (GIP) في مجرى الدم من الأمعاء الدقيقة استجابة ل وجبات. تتسبب هذه الهرمونات في إفراز الأنسولين من خلايا بيتا البنكرياس بطريقة تعتمد على الجلوكوز ولكن يتم إبطال نشاطها بواسطة إنزيم ديبيبتيديل ببتيداز -4 (DPP4) خلال دقائق. GLP-1 يقلل من إفراز الجلوكاجون من خلايا ألفا البنكرياس ، مما يقلل من إنتاج الجلوكوز الكبدي. في مرضى السكري من النوع 2 ، يتم تقليل تركيزات GLP-1 ولكن يتم الحفاظ على استجابة الأنسولين لـ GLP-1. Saxagliptin هو مثبط DPP4 تنافسي يعمل على إبطاء تعطيل هرمونات incretin ، وبالتالي زيادة مجرى الدم لديهم تركيزات وتقليل الصيام وتركيزات الجلوكوز بعد الأكل بطريقة تعتمد على الجلوكوز في المرضى الذين يعانون من مرض السكري من النوع 2 السكري.
الدوائية
في المرضى الذين يعانون من داء السكري من النوع 2 ، يمنع تناول Onglyza نشاط إنزيم DPP4 لمدة 24 ساعة. بعد حمل الجلوكوز عن طريق الفم أو الوجبة ، نتج عن هذا التثبيط DPP4 زيادة في مستويات الدورة الدموية النشطة بمعدل 2-3 أضعاف. GLP-1 و GIP ، انخفضت تركيزات الجلوكاجون ، وزيادة إفراز الأنسولين المعتمد على الجلوكوز من خلايا بيتا البنكرياس. وارتبطت الزيادة في الأنسولين وانخفاض في الجلوكاجون مع انخفاض تركيزات الجلوكوز في الصيام وانخفاض رحلة الجلوكوز بعد الحمل الجلوكوز عن طريق الفم أو وجبة.
الفيزيولوجيا الكهربية للقلب
في دراسة عشوائية متقاربة مزدوجة التعمية وتسيطر عليها وهمي ، وأجرى دراسة مقارنة نشطة باستخدام عقار موكسيفلوكساسين في 40 موضوعًا صحيًا ، لم يرتبط Onglyza بإطالة ذات دلالة إكلينيكية لفترة QTc أو معدل ضربات القلب بجرعات يومية تصل إلى 40 ملغ (8 أضعاف MRHD).
الدوائية
كانت الدوائية من ساكساجليبتين والمستقلب النشط ، ساكساجليبتين 5 هيدروكسي مماثلة في مواضيع صحية وفي المرضى الذين يعانون من داء السكري من النوع 2. جماكس وزادت قيم AUC لساكساجليبتين ومستقلبه النشط بشكل متناسب في نطاق جرعة 2.5 إلى 400 ملغ. بعد جرعة واحدة من 5 ملغ من ساكساجليبتين عن طريق الفم إلى الأشخاص الأصحاء ، كان متوسط قيم AUC للبلازما لساكساجليبتين ومستقلبه النشط 78 نانوغرام / ساعة و 214 نانوغرام / ساعة / مل ، على التوالي. البلازما المقابلة Cماكس كانت القيم 24 نانوغرام / مل و 47 نانوغرام / مل ، على التوالي. معدل التباين (٪ CV) لـ AUC و Cماكس لكل من ساكساجليبتين ومستقلبه النشط كان أقل من 25 ٪.
لم يلاحظ أي تراكم ملحوظ من ساكساجليبتين أو المستقلب النشط مع الجرعات المتكررة مرة واحدة يوميا على أي مستوى الجرعة. لم يلاحظ أي جرعة والاعتماد على الوقت في إزالة ساكساجليبتين والمستقلب النشط أكثر من 14 يوما من الجرعات مرة واحدة يوميا مع ساكساجليبتين بجرعات تتراوح بين 2.5 إلى 400 ملغ.
استيعاب
متوسط الوقت إلى أقصى تركيز (Tماكس) بعد 5 ملغ مرة واحدة كانت الجرعة اليومية 2 ساعة لساكساجلبتين و 4 ساعات عن المستقلب النشط. الإدارة مع وجبة عالية الدهون أدى إلى زيادة في Tماكس من ساكساجليبتين حوالي 20 دقيقة مقارنة بالظروف الصيام. كانت هناك زيادة بنسبة 27 ٪ في AUC من ساكساجليبتين عندما تعطى مع وجبة بالمقارنة مع الظروف الصيام. قد تدار Onglyza مع أو بدون طعام.
توزيع
في البروتين المختبر ملزمة لساكساجليبتين والمستقلب النشط في مصل الإنسان لا يكاد يذكر. لذلك ، من غير المتوقع أن تؤدي التغيرات في مستويات البروتين في الدم في حالات المرض المختلفة (مثل اختلال كلوي أو كبدي) إلى تغيير التخلص من الساكساجليبتين.
التمثيل الغذائي
تتم عملية التمثيل الغذائي لسكساجليبتين بشكل رئيسي عن طريق السيتوكروم P450 3A4 / 5 (CYP3A4 / 5). المستقلب الرئيسي لساكساجليبتين هو أيضا مثبط DPP4 ، والذي هو نصف قوي مثل ساكساجليبتين. لذلك ، فإن مثبطات ومحثات CYP3A4 / 5 القوية ستغير الدوائية للساكساجليبتين والمستقلب النشط. [نرى تفاعل الأدوية.]
إفراز
يتم التخلص من Saxagliptin بواسطة كل من المسارات الكلوية والكبدية. بعد جرعة واحدة 50 ملغ من 14تم إفراز C-saxagliptin ، 24 ٪ ، 36 ٪ ، و 75 ٪ من الجرعة في البول مثل saxagliptin ، المستقلب النشط ، والنشاط الإشعاعي الكلي ، على التوالي. كان متوسط خلوص الكلى لسكساجليبتين (حوالي 230 مل / دقيقة) أكبر من متوسط معدل الترشيح الكبيبي المقدر (حوالي 120 مل / دقيقة) ، مما يشير إلى بعض إفراز الكلى النشط. تم استرداد ما مجموعه 22 ٪ من النشاط الإشعاعي المدار في البراز الذي يمثل جزء من جرعة ساكساجليتين تفرز في الصفراء و / أو المخدرات غير الممتصة من الجهاز الهضمي. بعد جرعة واحدة عن طريق الفم من Onglyza 5 ملغ للأشخاص الأصحاء ، يعني نصف عمر محطة البلازما (ر1/2) لساكساجليبتين وكان المستقلب النشط 2.5 و 3.1 ساعة ، على التوالي.
السكان محددة
القصور الكلوي
تم إجراء دراسة جرعة واحدة ، مفتوحة التسمية لتقييم الحرائك الدوائية لساكساجلبتين (10 ملغ جرعة) في الموضوعات مع درجات متفاوتة من القصور الكلوي المزمن (N = 8 لكل مجموعة) مقارنة مع الأشخاص الذين يعانون من الكلى الطبيعي وظيفة. شملت الدراسة مرضى القصور الكلوي المصنفين على أساس تصفية الكرياتينين على أنها خفيفة (> 50 إلى ¤80 مل / دقيقة) ، معتدلة (30 إلى ¤ ‰50 مل / دقيقة) ، وشديدة (<30 مل / دقيقة) ، وكذلك المرضى الذين يعانون من مرض الكلى في نهاية المرحلة على غسيل الكلى. تم تقدير تصفية الكرياتينين من كرياتينين المصل بناءً على صيغة كوكروفت-جولت:
CrCl = [140 عامًا (بالسنوات)] الوزن (كجم) {—— 0.85 للمرضى من الإناث)
[72 creat كرياتينين المصل (ملغ / دل)]
لم درجة ضعف الكلى لا تؤثر على Cماكس ساكساجليبتين أو المستقلب النشط. في الأشخاص الذين يعانون من اختلال كلوي خفيف ، كانت قيم AUC لسكساجليبتين ومستقلبه النشط أعلى بنسبة 20 ٪ و 70 ٪ ، على التوالي ، من قيم AUC في الأشخاص الذين يعانون من وظائف الكلى الطبيعية. نظرًا لأن الزيادات بهذا الحجم لا تعتبر ذات صلة سريريًا ، فمن غير المستحسن تعديل الجرعة في المرضى الذين يعانون من اختلال كلوي خفيف. في الأشخاص الذين يعانون من اختلال كلوي معتدل أو شديد ، فإن قيم AUC للسكساجليبتين ونشطته كان المستقلب يصل إلى 2.1 و 4.5 أضعاف ، على التوالي ، من القيم AUC في الموضوعات مع الكلوي الطبيعي وظيفة. لتحقيق التعرض للبلازما من ساكساجليبتين وأيضه النشط مماثل لتلك الموجودة في المرضى الذين يعانون من وظائف الكلى الطبيعية ، الجرعة الموصى بها 2.5 ملغ مرة واحدة يوميًا في مرضى القصور الكلوي المعتدل والشديد ، وكذلك في المرضى الذين يعانون من مرض الكلى في المرحلة النهائية التي تتطلب غسيل الكلى. تتم إزالة Saxagliptin عن طريق غسيل الكلى.
اختلال كبدي
في الأشخاص الذين يعانون من اختلال كبدي (فصول تشابك الأطفال A و B و C) ، يعني Cماكس وكان AUC من ساكساجليبتين يصل إلى 8 ٪ و 77 ٪ على التوالي ، مقارنة مع الضوابط المتطابقة صحية بعد إعطاء جرعة واحدة 10 ملغ من ساكساجليبتين. المقابلة جيمماكس و AUC من المستقلب النشط كانت تصل إلى 59 ٪ و 33 ٪ أقل ، على التوالي ، مقارنة مع الضوابط مطابقة صحية. لا تعتبر هذه الاختلافات ذات مغزى سريريًا. لا يوصى بتعديل الجرعة للمرضى المصابين بضعف كبدي.
مؤشر كتلة الجسم
لا يوصى بتعديل الجرعة بناءً على مؤشر كتلة الجسم (BMI) والذي لم يتم تحديده على أنه هام متغير على إزالة واضحة من ساكساجليبتين أو المستقلب النشط في الدوائية السكان تحليل.
جنس
لا يوصى بتعديل الجرعة بناءً على الجنس. لم تكن هناك اختلافات لوحظت في الدوائية ساكساجليبتين بين الذكور والإناث. مقارنةً بالذكور ، كان لدى الإناث قيم تعرض أعلى بنسبة حوالي 25 ٪ للمستقلب النشط من الذكور ، ولكن من غير المرجح أن يكون هذا الاختلاف ذا صلة سريرية. لم يتم تحديد الجنس باعتباره متغير مشترك كبير على إزالة واضحة من ساكساجليبتين والمستقلب النشط في تحليل الحرائك الدوائية السكان.
الشيخوخة
لا يوصى بتعديل الجرعة على أساس العمر وحده. كان لدى كبار السن (65-80 سنة) متوسط هندسي بنسبة 23٪ و 59٪ماكس والقيم الهندسية للقيم AUC ، على التوالي ، لساكساجليبتين من الموضوعات الصغيرة (18-40 سنة). تعكس الاختلافات في الحرائك الدوائية المستقلب النشط بين الأشخاص المسنين والشباب بشكل عام الاختلافات التي لوحظت في الحرائك الدوائية لساكساجليبتين. الفرق بين الدوائية لساكساجليبتين والمستقلب النشط في الشباب وكبار السن الموضوعات على الأرجح بسبب عوامل متعددة بما في ذلك انخفاض وظيفة الكلى والقدرة الأيضية مع زيادة العمر. لم يتم تحديد العمر كمتغيّر مهم في التخلّص الظاهر لساكساجليبتين وأيضه النشط في التحليل الدوائي السكاني.
اخصائي اطفال
لم يتم إجراء الدراسات التي تميز الحرائك الدوائية لساكساجليبتين في مرضى الأطفال.
السلالة والعرق
لا ينصح تعديل الجرعة على أساس العرق. قارن تحليل الحرائك الدوائية للسكان بين الدوائية لساكساجليتين ونشطته المستقلب في 309 موضوعات قوقازية مع 105 موضوعات غير قوقازية (تتكون من ستة عنصرية مجموعات). تم الكشف عن عدم وجود اختلاف كبير في الدوائية من ساكساجليبتين والمستقلب النشط بين هؤلاء السكان.
المخدرات المخدرات التفاعلات
في المختبر تقييم التفاعلات المخدرات
تتم عملية التمثيل الغذائي لسكساجليبتين بشكل رئيسي عن طريق CYP3A4 / 5.
في الدراسات المختبرية ، لم يمنع ساكساجليبتين وأيضه النشط CYP1A2 أو 2A6 أو 2B6 أو 2C9 أو 2C19 أو 2D6 أو 2E1 أو 3A4 أو حمل CYP1A2 أو 2B6 أو 2C9 أو 3A4. لذلك ، لا يُتوقع أن يؤدي ساكساجليبتين إلى تغيير الخلوص الأيضي للعقاقير المتداخلة التي يتم استقلابها بواسطة هذه الإنزيمات. Saxagliptin عبارة عن ركيزة P-glycoprotein (P-gp) ولكنها ليست مثبطًا كبيرًا أو محفزًا لـ P-gp.
في البروتين المختبر ملزمة لساكساجليبتين والمستقلب النشط في مصل الإنسان لا يكاد يذكر. وبالتالي ، فإن ربط البروتين لن يكون له تأثير كبير على الحرائك الدوائية للساكساجليبتين أو الأدوية الأخرى.
في الجسم الحي تقييم التفاعلات المخدرات
آثار Saxagliptin على المخدرات الأخرى
في الدراسات التي أجريت على الأشخاص الأصحاء ، كما هو موضح أدناه ، لم يغير ساكساجليبتين معنى الحرائك الدوائية للميتفورمين ، الغليبيريد ، البيوغليتازون ، الديجوكسين ، سيمفاستاتين ، الديلتيازيم ، أو الكيتوكونازول.
الميتفورمين: لم يغير التناول المشترك للجرعة المفردة من ساكساجليبتين (100 ملغ) والميتفورمين (1000 ملغ) ، الركيزة hOCT-2 ، من الدوائية للميتفورمين في الأشخاص الأصحاء. لذلك ، فإن Onglyza ليس مثبطًا للنقل بواسطة hOCT-2.
Glyburide: تضافرت جرعة واحدة من ساكساجليبتين (10 مجم) و glyburide (5 مجم) ، ركيزة CYP2C9 ، زادت البلازما Cماكس من glyburide بنسبة 16 ٪. ومع ذلك ، فإن AUC من glyburide لم يتغير. لذلك ، Onglyza لا تمنع بشكل صحيح الأيض CYP2C9.
البيوجليتازون: أدى تضافر الجرعات المتعددة مرة واحدة يوميًا من ساكساجليبتين (10 ملغ) والبيوجليتازون (45 مجم) ، وهي مادة أساسية CYP2C8 ، إلى زيادة البلازما Cماكس بيوجليتازون بنسبة 14 ٪. ومع ذلك ، فإن AUC من بيوجليتازون لم يتغير.
الديجوكسين: إن التناول المتعدد للجرعات مرة واحدة يوميًا من ساكساجليبتين (10 ملغ) و الديجوكسين (0.25 ملغ) ، وهو ركيزة P-gp ، لم يغير من الدوائية للديجوكسين. لذلك ، Onglyza ليس مثبط أو محفز للنقل بوساطة P-gp.
سيمفاستاتين: إن التناول المتعدد لجرعات ساكساجليبتين مرة واحدة يوميًا (10 ملغ) وسيمفاستاتين (40 ملغ) ، ركيزة CYP3A4 / 5 ، لم يغير الدوائية للسيمفاستاتين. لذلك ، Onglyza ليس مثبطًا أو محفزًا لعملية الأيض CYP3A4 / 5.
الديلتيازيم: أدى التناول المتعدد لجرعات ساكساجليبتين مرة واحدة يوميًا (10 ملغ) و الديلتيازيم (تركيبة طويلة المفعول 360 ملغ في حالة مستقرة) ، مثبط معتدل لـ CYP3A4 / 5 ، إلى زيادة البلازما Cماكس من الديلتيازيم بنسبة 16 ٪ ؛ ومع ذلك ، فإن AUC من ديلتيازيم لم يتغير.
الكيتوكونازول: التناول المشترك لجرعة واحدة من ساكساجليبتين (100 ملغ) وجرعات متعددة من الكيتوكونازول (200 ملغ كل 12 ساعة في حالة مستقرة) ، مثبط قوي لـ CYP3A4 / 5 و P-gp ، قلل من بلازما Cmax و AUC من الكيتوكونازول بنسبة 16 ٪ و 13 ٪ ، على التوالي.
آثار المخدرات الأخرى على سكساجلبتين
الميتفورمين: أدى التناول المتزامن لجرعة واحدة من ساكساجليبتين (100 ملغ) والميتفورمين (1000 ملغ) ، ركيزة HOCT-2 ، إلى انخفاض Cماكس ساكساجليبتين بنسبة 21 ٪ ؛ ومع ذلك ، فإن AUC لم يتغير.
Glyburide: تضافرت جرعة واحدة من ساكساجليبتين (10 مجم) و glyburide (5 مجم) ، ركيزة CYP2C9 ، مما زاد من Cماكس ساكساجليبتين بنسبة 8 ٪ ؛ ومع ذلك ، فإن AUC من ساكساجليبتين لم يتغير.
بيوجليتازون: التناول المتعدد لجرعات ساكساجليتين مرة واحدة يوميًا (10 ملغ) وبيوجليتازون (45 ملغ) ، CYP2C8 (الكبرى) و CYP3A4 (ثانوية) الركيزة ، لم يغير الدوائية لل ساكساغلبتين.
الديجوكسين: إن التناول المتعدد الجرعات مرة واحدة يوميًا من ساكساجليبتين (10 ملغ) و الديجوكسين (0.25 ملغ) ، ركيزة P-gp ، لم يغير من الدوائية للساكساجليبتين.
سيمفاستاتين: تضافر تناول جرعات متعددة مرة واحدة يوميًا من ساكساجليبتين (10 ملغ) وسيمفاستاتين (40 ملغ) ، ركيزة CYP3A4 / 5 ، زاد Cماكس ساكساجليبتين بنسبة 21 ٪ ؛ ومع ذلك ، فإن AUC من ساكساجليبتين لم يتغير.
ديلتيازيم: أدى التناول المتزامن لجرعة واحدة من ساكساجليبتين (10 ملغ) وديلتيازيم (تركيبة طويلة المفعول 360 ملغ في حالة مستقرة) ، وهو مثبط معتدل لـ CYP3A4 / 5 ، إلى زيادة Cماكس من ساكساجليبتين بنسبة 63 ٪ و AUC بنسبة 2.1 أضعاف. ارتبط هذا مع انخفاض المقابلة في Cماكس و AUC من المستقلب النشط بنسبة 44 ٪ و 36 ٪ ، على التوالي.
الكيتوكونازول: أدى تناول جرعة واحدة من ساكساجليبتين (100 ملغ) والكيتوكونازول (200 ملغ كل 12 ساعة في حالة مستقرة) ، مثبط قوي لـ CYP3A4 / 5 و P-gp ، إلى زيادة Cماكس لسكساجليبتين بنسبة 62 ٪ و AUC بنسبة 2.5 أضعاف. ارتبط هذا مع انخفاض المقابلة في Cماكس و AUC من المستقلب النشط بنسبة 95 ٪ و 91 ٪ ، على التوالي.
في دراسة أخرى ، أدى تزامن جرعة واحدة من ساكساجليبتين (20 ملغ) والكيتوكونازول (200 ملغ كل 12 ساعة في حالة مستقرة) ، إلى زيادة Cماكس و AUC من ساكساجليبتين بنسبة 2.4 أضعاف و 3.7 أضعاف ، على التوالي. ارتبط هذا مع انخفاض المقابلة في Cماكس و AUC من المستقلب النشط بنسبة 96 ٪ و 90 ٪ ، على التوالي.
ريفامبين: أدى انخفاض جرعة واحدة من ساكساجليبتين (5 ملغ) وريفامبين (600 ملغ من الكمية الثابتة في حالة مستقرة) إلى انخفاض جرعة Cماكس و AUC من ساكساجليبتين بنسبة 53 ٪ و 76 ٪ ، على التوالي ، مع زيادة مقابلة في Cماكس (39 ٪) ولكن لا يوجد تغيير كبير في البلازما AUC من المستقلب النشط.
Omeprazole: التناول المتعدد لجرعات ساكساجليتين مرة واحدة يوميًا (10 مجم) وأوميبرازول (40 مجم) ، CYP2C19 (الرئيسية) و CYP3A4 الركيزة ، ومثبط CYP2C19 ، ومحث من MRP-3 ، لم يغير الدوائية ل ساكساغلبتين.
هيدروكسيد الألومنيوم + هيدروكسيد المغنيسيوم + سيميثيكون: إدارة جرعة واحدة من ساكساجليتين (10 ملغ) و سائل يحتوي على هيدروكسيد الألومنيوم (2400 ملغ) ، وهيدروكسيد المغنيسيوم (2400 ملغ) ، وسيميثيكون (240 ملغ) انخفض Cماكس ساكساجليبتين بنسبة 26 ٪ ؛ ومع ذلك ، فإن AUC من ساكساجليبتين لم يتغير.
فاموتيدين: تناول جرعة واحدة من ساكساجليبتين (10 ملغ) بعد 3 ساعات من جرعة واحدة من فاموتيدين (40 ملغ) ، ومثبط من HOCT-1 ، hOCT-2 ، و hOCT-3 ، زاد من Cماكس ساكساجليبتين بنسبة 14 ٪ ؛ ومع ذلك ، فإن AUC من ساكساجليبتين لم يتغير.
أعلى
علم السموم غير الإكلينيكي
التسرطن ، الطفرات ، ضعف الخصوبة
لم يحفز ساكساليبتين الأورام في الفئران (50 ، 250 ، و 600 ملغم / كغم) أو الفئران (25 ، 75 ، 150 ، و 300 ملغم / كغم) في أعلى الجرعات التي تم تقييمها. وكانت أعلى الجرعات التي تم تقييمها في الفئران تعادل حوالي 870 (ذكور) و 1165 (إناث) أضعاف التعرض البشري في MRHD من 5 ملغ / يوم. في الفئران ، كان التعرض ما يقرب من 355 (ذكور) و 2217 (إناث) أضعاف MRHD.
لم يكن ساكساجليبتين طفرات أو طفرات معوية أو بدون تفعيل التمثيل الغذائي في اختبار البكتيريا Ames في المختبر ، وهو اختبار في علم الوراثة الخلوية في المختبر في الإنسان الأولي الخلايا الليمفاوية ، اختبار في النواة الصغرى عن طريق الفم في الفئران ، في الجسم الحي دراسة إصلاح الحمض النووي في الفئران ، عن طريق الفم في الجسم الحي / في علم الوراثة الخلوية دراسة في الدم المحيطي الفئران الخلايا الليمفاوية. المستقلب النشط لم يكن مطفرا في اختبار البكتيريا Ames في المختبر.
في دراسة لخصوبة الفئران ، عولج الرجال بجرعات من الفم عن طريق الفم لمدة 2 أسابيع قبل التزاوج ، وأثناء التزاوج ، وحتى الموعد المحدد الإنهاء (حوالي 4 أسابيع تقريبًا) وتمت معالجة الإناث بجرعات من الجرعات الفموية لمدة أسبوعين قبل التزاوج خلال فترة الحمل اليوم 7. لم يلاحظ أي آثار ضارة على الخصوبة في التعرض لحوالي 603 (ذكور) و 776 (إناث) أضعاف MRHD. جرعات أعلى أثارت سمية الأم زادت أيضا من امتصاص الجنين (حوالي 2069 و 6138 أضعاف MRHD). وقد لوحظت تأثيرات إضافية على ركوب الدراجات الوعرة ، والخصوبة ، والإباضة ، والزرع في حوالي 6138 مرة من MRHD.
علم السموم الحيوانية
أنتج Saxagliptin تغيرات جلدية ضارة في الأطراف القردة cynomolgus (الجرب و / أو تقرح الذيل والأرقام وكيس الصفن و / أو الأنف). كانت الآفات الجلدية قابلة للانعكاس عند حوالي 20 مرة من MRHD ولكن في بعض الحالات كانت لا رجعة فيها وتنخر في التعرضات العالية. لم يلاحظ تغيرات الجلد السلبية في التعرضات المماثلة ل (1-3 مرات) MRHD من 5 ملغ. السريرية لا ترتبط الآفات الجلدية في القردة لم يلاحظ في التجارب السريرية الإنسان من ساكساجليتين.
أعلى
الدراسات السريرية
تمت دراسة Onglyza كعلاج وحيد وبالاقتران مع الميتفورمين ، والجليبورايد ، والثييازوليدينيديون (بيوجليتازون و روزيجليتازون). لم تتم دراسة Onglyza بالاشتراك مع الأنسولين.
تم اختيارهم بصورة عشوائية ما مجموعه 4148 مريضا يعانون من داء السكري من النوع 2 في ستة ، التجارب السريرية مزدوجة التعمية ، التي تسيطر عليها لتقييم سلامة وفعالية نسبة السكر في الدم من Onglyza. تم علاج ما مجموعه 3021 مريضا في هذه التجارب مع Onglyza. في هذه التجارب ، كان متوسط العمر 54 عامًا ، وكان 71٪ من المرضى من القوقاز ، و 16٪ من آسيا ، و 4٪ من السود ، و 9٪ من المجموعات العرقية الأخرى. شارك 423 مريضًا إضافيًا ، من بينهم 315 تلقوا Onglyza ، في دراسة مضبوطة بالجرعات تتراوح بين 6 و 12 أسبوعًا.
في هذه التجارب الستة مزدوجة التعمية ، تم تقييم Onglyza بجرعات 2.5 ملغ و 5 ملغ مرة واحدة يوميًا. ثلاثة من هذه التجارب أيضا تقييم جرعة ساكساجليبتين من 10 ملغ يوميا. لم توفر الجرعة اليومية البالغة 10 ملغ من ساكساجليبتين فعالية أكبر من الجرعة اليومية البالغة 5 ملغ. العلاج مع Onglyza في جميع الجرعات أنتجت تحسينات ذات الصلة سريريا وذات دلالة إحصائية في الهيموغلوبين A1c (A1C) ، الجلوكوز في بلازما الصيام (FPG) ، والجلوكوز بعد الأكل لمدة ساعتين (PPG) في أعقاب اختبار التحمل القياسي للجلوكوز عن طريق الفم (OGTT) ، مقارنةً مراقبة. شوهدت تخفيضات في A1C عبر مجموعات فرعية بما في ذلك الجنس والعمر والعرق ومؤشر كتلة الجسم الأساسي.
لم يرتبط Onglyza مع تغييرات كبيرة من الأساس في وزن الجسم أو الدهون في المصل الصيام مقارنة مع الدواء الوهمي.
وحيد
ما مجموعه 766 مريضًا يعانون من مرض السكري من النوع 2 لا يخضعون لرقابة كافية على النظام الغذائي والتمارين الرياضية (A1C - 7 ٪ إلى - 10 ٪) شارك في تجربتين لمدة 24 أسبوع ، مزدوجة التعمية ، وهمي تسيطر عليها تقييم فعالية وسلامة Onglyza وحيد.
في التجربة الأولى ، بعد نظام غذائي أحادي الأعمى لمدة أسبوعين ، وتمرين ، وهمي الرصاص في الفترة ، تم اختيارهم بصورة عشوائية من 401 مريض إلى 2.5 ملغ ، 5 ملغ ، أو 10 ملغ من Onglyza أو وهمي. تم علاج المرضى الذين فشلوا في تحقيق أهداف نسبة السكر في الدم خلال الدراسة مع العلاج الإنقاذ الميتفورمين ، إضافة إلى الدواء الوهمي أو Onglyza. تم تقييم فعالية في آخر قياس قبل العلاج الإنقاذ للمرضى الذين يحتاجون إلى الإنقاذ. لا يُسمح بمعايرة جرعة Onglyza.
قدمت العلاج مع Onglyza 2.5 ملغ و 5 ملغ يوميا تحسينات كبيرة في A1C ، FPG ، و PPG مقارنة مع الدواء الوهمي (الجدول 3). النسبة المئوية للمرضى الذين توقفوا بسبب نقص السيطرة على نسبة السكر في الدم أو الذين تم إنقاذهم للقاء محدد مسبقًا كانت معايير نسبة السكر في الدم 16 ٪ في مجموعة العلاج Onglyza 2.5 ملغ ، 20 ٪ في مجموعة العلاج Onglyza 5 ملغ ، و 26 ٪ في مجموعة الدواء الوهمي.
الجدول 3: معلمات نسبة السكر في الدم في الأسبوع 24 في دراسة تسيطر عليها وهمي من Onglyza وحيد في مرضى السكري من النوع 2 *
| معلمة الفعالية | Onglyza 2.5 ملغ N = 102 |
Onglyza 5 ملغ N = 106 |
الوهمي N = 95 |
|---|---|---|---|
| * نية لعلاج السكان باستخدام الملاحظة الأخيرة في الدراسة أو الملاحظة الأخيرة قبل العلاج الإنقاذ الميتفورمين للمرضى الذين يحتاجون إلى الإنقاذ. | |||
| †المربعات الصغرى تعني ضبط القيمة الأساسية. | |||
| ج قيمة p <0.0001 مقارنة مع الدواء الوهمي | |||
| § ف القيمة <0.05 مقارنة مع الدواء الوهمي | |||
| ¶ لم يتم اختبار أهمية ل PPG 2 ساعة لجرعة 2.5 ملغ من Onglyza. | |||
| الهيموجلوبين A1C (٪) | N = 100 | N = 103 | N = 92 |
| خط الأساس (الوسط) | 7.9 | 8.0 | 7.9 |
| التغيير من الأساس (المعدل المعدل)†) | −0.4 | −0.5 | +0.2 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) | −0.6ج | −0.6ج | |
| 95 ٪ فاصل الثقة | (−0.9, −0.3) | (−0.9, −0.4) | |
| نسبة المرضى الذين حققوا A1C <7٪ | 35% (35/100) | 38% §(39/103) | 24% (22/92) |
| صيام الجلوكوز في البلازما (mg / dL) | N = 101 | N = 105 | N = 92 |
| خط الأساس (الوسط) | 178 | 171 | 172 |
| التغيير من الأساس (المعدل المعدل)†) | −15 | −9 | +6 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) | −21 § | −15 § | |
| 95 ٪ فاصل الثقة | (−31, −10) | (−25, −4) | |
| 2 ساعة بعد الجلوكوز (ملغ / ديسيلتر) | N = 78 | N = 84 | N = 71 |
| خط الأساس (الوسط) | 279 | 278 | 283 |
| التغيير من الأساس (المعدل المعدل)†) | −45 | −43 | −6 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) | −39 ¶ | −37 § | |
| 95 ٪ فاصل الثقة | (−61, −16) | (−59, −15) |
تم إجراء تجربة علاج أحادي ثانية لمدة 24 أسبوعًا لتقييم مجموعة من أنظمة الجرعات الخاصة بـ Onglyza. خضع مرضى ساذج العلاج مع مرض السكري غير الخاضعة للرقابة (A1C٪ 7 ٪ إلى ¤٪ 10 ٪) على نظام غذائي أحادي المفرد لمدة أسبوعين ، وممارسة ، وهمي الرصاص في الفترة. تم اختيارهم بصورة عشوائية ما مجموعه 365 مريضا إلى 2.5 ملغ كل صباح ، 5 ملغ كل صباح ، 2.5 ملغ مع المعايرة المحتملة إلى 5 ملغ كل صباح ، أو 5 ملغ كل مساء من Onglyza ، أو وهمي. تم علاج المرضى الذين فشلوا في تحقيق أهداف نسبة السكر في الدم أثناء الدراسة مع العلاج الإنقاذ الميتفورمين إضافة إلى الدواء الوهمي أو Onglyza. تراوح عدد المرضى الذين تم اختيارهم بصورة عشوائية لكل مجموعة علاج من 71 إلى 74.
قدم العلاج باستخدام Onglyza 5 ملغ كل صباح أو 5 ملغ كل مساء تحسينات كبيرة في A1C مقابل الدواء الوهمي (يعني التخفيضات الصحيحة تصحيح وهمي من 0ˆ0.4 ٪ و .30.3 ٪ على التوالي). قدمت العلاج مع Onglyza 2.5 ملغ كل صباح تحسنا كبيرا في A1C مقابل الدواء الوهمي (يعني تخفيض تصحيح وهمي من 000.4 ٪).
الجمع بين العلاج
إضافة على الجمع بين العلاج مع الميتفورمين
شارك ما مجموعه 743 مريضًا يعانون من مرض السكري من النوع 2 في هذه التجربة العشوائية التي استمرت 24 أسبوعًا والتي خضعت للتحكم في العلاج الوهمي لمدة 24 أسبوعًا. فعالية وسلامة Onglyza في تركيبة مع الميتفورمين في المرضى الذين يعانون من نقص التحكم في نسبة السكر في الدم (A1C ¥ ¥ ¥ 7 ٪ و â ¤10 ٪) على الميتفورمين وحده. للتأهل للالتحاق ، طُلب من المرضى أن يتناولوا جرعة ثابتة من الميتفورمين (1500-2550 ملغ يوميًا) لمدة 8 أسابيع على الأقل.
تم تسجيل المرضى الذين حققوا معايير الأهلية في دواء وهمي وحيد للمكفوفين لمدة أسبوعين الفترة التي تلقى خلالها المرضى الميتفورمين بجرعة ما قبل الدراسة ، تصل إلى 2500 ملغ يوميًا ، لمدة دراسة. بعد الفترة التي سبقت ، تم اختيارهم بصورة عشوائية المرضى المؤهلين إلى 2.5 ملغ ، 5 ملغ ، أو 10 ملغ من Onglyza أو وهمي بالإضافة إلى الجرعة الحالية من الميتفورمين المفتوح التسمية. تم علاج المرضى الذين فشلوا في تحقيق أهداف نسبة السكر في الدم أثناء الدراسة مع العلاج الإنقاذ بيوجليتازون ، وأضاف إلى الأدوية الموجودة الدراسة. لم يسمح بمعايرة الجرعة من Onglyza و metformin.
قدمت Onglyza 2.5 ملغ و 5 ملغ الوظيفة الإضافية لميفورمين تحسينات كبيرة في A1C ، FPG ، و PPG مقارنة مع الدواء الوهمي إضافة إلى الميتفورمين (الجدول 4). تظهر التغييرات 1 من خط الأساس ل A1C مع مرور الوقت وعند نقطة النهاية في الشكل 1. كانت نسبة المرضى الذين توقفوا بسبب عدم وجود مراقبة نسبة السكر في الدم أو الذين تم إنقاذهم لتلبية معايير نسبة السكر في الدم المحددة مسبقا 15 ٪ في Onglyza 2.5 ملغ الوظيفة الإضافية لمجموعة الميتفورمين ، 13 ٪ في Onglyza 5 ملغ الوظيفة الإضافية إلى مجموعة الميتفورمين ، و 27 ٪ في الدواء الوهمي المضاف إلى الميتفورمين مجموعة.
الجدول 4: معلمات نسبة السكر في الدم في الأسبوع 24 في دراسة تسيطر عليها وهمي من Onglyza كعلاج الجمع بين الوظيفة مع الميتفورمين *
| معلمة الفعالية | Onglyza 2.5 ملغ + ميتفورمين N = 192 |
Onglyza 5 ملغ + ميتفورمين N = 191 |
الوهمي + ميتفورمين N = 179 |
|---|---|---|---|
| * النية لعلاج السكان باستخدام الملاحظة الأخيرة في الدراسة أو الملاحظة الأخيرة قبل العلاج الإنقاذ بيوجليتازون للمرضى الذين يحتاجون إلى الإنقاذ. | |||
| †المربعات الصغرى تعني ضبط القيمة الأساسية. | |||
| ج قيمة p <0.0001 مقارنة مع الدواء الوهمي + الميتفورمين | |||
| § قيمة p <0.05 مقارنة مع الدواء الوهمي + الميتفورمين | |||
| الهيموجلوبين A1C (٪) | N = 186 | N = 186 | N = 175 |
| خط الأساس (الوسط) | 8.1 | 8.1 | 8.1 |
| التغيير من الأساس (المعدل المعدل)†) | −0.6 | −0.7 | +0.1 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) | −0.7ج | −0.8ج | |
| 95 ٪ فاصل الثقة | (−0.9, −0.5) | (−1.0, −0.6) | |
| نسبة المرضى الذين حققوا A1C <7٪ | 37% §(69/186) | 44% §(81/186) | 17% (29/175) |
| صيام الجلوكوز في البلازما (mg / dL) | N = 188 | N = 187 | N = 176 |
| خط الأساس (الوسط) | 174 | 179 | 175 |
| التغيير من الأساس (المعدل المعدل)†) | −14 | −22 | +1 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) | −16 § | −23 § | |
| 95 ٪ فاصل الثقة | (−23, −9) | (−30, −16) | |
| 2 ساعة بعد الجلوكوز (ملغ / ديسيلتر) | N = 155 | N = 155 | N = 135 |
| خط الأساس (الوسط) | 294 | 296 | 295 |
| التغيير من الأساس (المعدل المعدل)†) | −62 | −58 | −18 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) | −44 § | −40 § | |
| 95 ٪ فاصل الثقة | (−60, −27) | (−56, −24) |
الشكل 1: يعني التغيير من خط الأساس في A1C في تجربة دواء وهمي من Onglyza كعلاج إضافي مع ميتفورمين *
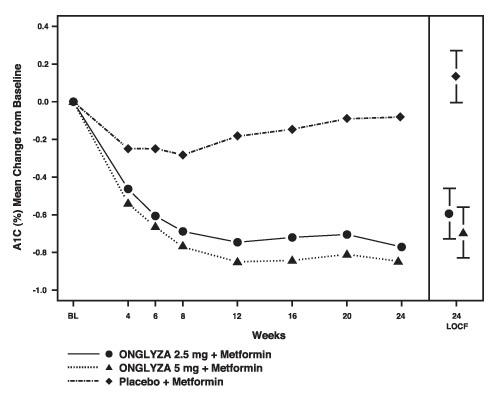
* يشمل المرضى الذين يعانون من خط الأساس وقيمة الأسبوع 24.
يتضمن الأسبوع 24 (LOCF) السكان النية لعلاج باستخدام الملاحظة الأخيرة في الدراسة قبل العلاج الإنقاذ بيوجليتازون للمرضى الذين يحتاجون إلى الإنقاذ. يعني التغيير من الأساس هو ضبط لقيمة الأساس.
إضافة على الجمع بين العلاج مع Thiazolidinedione
شارك ما مجموعه 565 مريضًا مصابين بداء السكري من النوع 2 في هذه التجربة العشوائية التي استمرت 24 أسبوعًا والتي خضعت للتحكم في العلاج الوهمي لمدة 24 أسبوعًا. فعالية وسلامة Onglyza في تركيبة مع ثيازوليدينيديون (TZD) في المرضى الذين يعانون من نقص السكر في الدم التحكم (A1C â ¥٪ 7 ٪ إلى ¤10.5 ٪) على TZD وحده. للتأهل للالتحاق ، طُلب من المرضى تناول جرعة ثابتة من البيوجليتازون (30-45 ملغ مرة واحدة يوميًا) أو روزيجليتازون (4 ملغ مرة واحدة يوميًا أو 8 ملغ إما مرة واحدة يوميًا أو في جرعتين مقسومتين 4 ملغ) لمدة 12 على الأقل أسابيع.
تم تسجيل المرضى الذين استوفوا معايير الأهلية في واحدة عمياء ، 2 أسابيع ، والنظام الغذائي وممارسة الرياضة وهمي الرصاص في الفترة التي تلقى خلالها المرضى TZD في جرعة ما قبل الدراسة لمدة دراسة. بعد الفترة التي سبقت ، تم اختيارهم بصورة عشوائية من المرضى المؤهلين إلى 2.5 ملغ أو 5 ملغ من Onglyza أو وهمي بالإضافة إلى الجرعة الحالية من TZD. تم علاج المرضى الذين فشلوا في تحقيق أهداف نسبة السكر في الدم أثناء الدراسة بإنقاذ الميتفورمين ، إضافة إلى الأدوية الموجودة في الدراسة. لم يسمح بمعايرة الجرعة من Onglyza أو TZD أثناء الدراسة. تم السماح بإجراء تغيير في نظام TZD من روسيجليتازون إلى بيوجليتازون في جرعات علاجية مكافئة محددة حسب تقدير المحقق إذا كان يعتقد أنه مناسب طبياً.
قدمت Onglyza 2.5 ملغ و 5 ملغ الوظيفة الإضافية إلى TZD تحسينات كبيرة في A1C ، FPG ، و PPG مقارنة مع الدواء الوهمي إلى TZD (الجدول 5). نسبة المرضى الذين توقفوا بسبب نقص السيطرة على نسبة السكر في الدم أو الذين تم إنقاذهم لتلبية معايير نسبة السكر في الدم المحددة مسبقًا كان 10 ٪ في Onglyza 2.5 ملغ الوظيفة الإضافية لمجموعة TZD ، 6 ٪ لمجموعة Onglyza 5 ملغ إلى TZD ، و 10 ٪ في إضافة الدواء الوهمي إلى TZD مجموعة.
الجدول 5: معلمات نسبة السكر في الدم في الأسبوع 24 في دراسة تسيطر عليها وهمي من Onglyza كعلاج الجمع بين الوظيفة مع الثيازيدوليديون *
| معلمة الفعالية | Onglyza 2.5 ملغ + TZD N = 195 |
Onglyza 5 ملغ + TZD N = 186 |
الوهمي + TZD N = 184 |
|---|---|---|---|
| * نية لعلاج السكان باستخدام الملاحظة الأخيرة في الدراسة أو الملاحظة الأخيرة قبل العلاج الإنقاذ الميتفورمين للمرضى الذين يحتاجون إلى الإنقاذ. | |||
| †المربعات الصغرى تعني ضبط القيمة الأساسية. | |||
| ج قيمة p <0.0001 مقارنةً بالعلاج الوهمي + TZD | |||
| § قيمة p <0.05 مقارنةً بالعلاج الوهمي + TZD | |||
| الهيموجلوبين A1C (٪) | N = 192 | N = 183 | N = 180 |
| خط الأساس (الوسط) | 8.3 | 8.4 | 8.2 |
| التغيير من الأساس (المعدل المعدل)†) | −0.7 | −0.9 | −0.3 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) | −0.4 § | −0.6ج | |
| 95 ٪ فاصل الثقة | (−0.6, −0.2) | (−0.8, −0.4) | |
| نسبة المرضى الذين حققوا A1C <7٪ | 42% §(81/192) | 42% §(77/184) | 26% (46/180) |
| صيام الجلوكوز في البلازما (mg / dL) | N = 193 | N = 185 | N = 181 |
| خط الأساس (الوسط) | 163 | 160 | 162 |
| التغيير من الأساس (المعدل المعدل)†) | −14 | −17 | −3 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) | −12 § | −15 § | |
| 95 ٪ فاصل الثقة | (−20, −3) | (−23, −6) | |
| 2 ساعة بعد الجلوكوز (ملغ / ديسيلتر) | N = 156 | N = 134 | N = 127 |
| خط الأساس (الوسط) | 296 | 303 | 291 |
| التغيير من الأساس (المعدل المعدل)†) | −55 | −65 | −15 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) | −40 § | −50 § | |
| 95 ٪ فاصل الثقة | (−56, −24) | (−66, −34) |
إضافة على الجمع بين العلاج مع Glyburide
شارك ما مجموعه 768 مريضًا مصابين بداء السكري من النوع 2 في هذه التجربة العشوائية التي استمرت 24 أسبوعًا والتي خضعت للتحكم في العلاج الوهمي لتقييم الفعالية والسلامة من Onglyza في تركيبة مع سلفونيل يوريا (SU) في المرضى الذين يعانون من نقص في نسبة السكر في الدم عند التحاق (A1C - 7.5 ٪ إلى ¤٪ 10 ٪) على جرعة دون الحد الأدنى من SU وحده. للتأهل للالتحاق ، طُلب من المرضى أن يتناولوا جرعة منخفضة من SU لمدة شهرين أو أكثر. في هذه الدراسة ، تمت مقارنة Onglyza مع جرعة ثابتة وسيطة من SU بالمعايرة مع جرعة أعلى من SU.
تم تسجيل المرضى الذين استوفوا معايير الأهلية في فترة واحدة للمكفوفين ، لمدة 4 أسابيع ، والغذائية وممارسة التمرينات الرياضية ، ووضعها على glyburide 7.5 ملغ مرة واحدة يوميًا. بعد الفترة التي سبقت ، تم اختيارهم بصورة عشوائية المرضى المؤهلين مع A1C ¥ ¥ 7 ٪ إلى ¤ ¤ 10 ٪ إلى إما 2.5 ملغ أو 5 ملغ من إضافة Onglyza إلى 7.5 ملغ من غليبوريد أو دواء وهمي بالإضافة إلى 10 ملغ من الجرعة اليومية الكلية غليبوريد. كان المرضى الذين تلقوا العلاج الوهمي مؤهلين للحصول على غليبورايد عيار يصل إلى جرعة يومية إجمالية قدرها 15 ملغ. لم يُسمح بمعايرة الجليبريد في المرضى الذين تلقوا Onglyza 2.5 ملغ أو 5 ملغ. يمكن أن يتم معايرة الغليبيريد في أي مجموعة علاج مرة واحدة خلال فترة الدراسة لمدة 24 أسبوعًا بسبب نقص السكر في الدم حسبما يراه المحقق ضروريًا. تم معايرة حوالي 92 ٪ من المرضى في مجموعة الدواء الوهمي بالإضافة إلى مجموعة الجليبريد إلى الجرعة النهائية الكلية الإجمالية البالغة 15 ملغ خلال الأسابيع الأربعة الأولى من فترة الدراسة. تم علاج المرضى الذين فشلوا في تحقيق أهداف نسبة السكر في الدم أثناء الدراسة بإنقاذ الميتفورمين ، إضافة إلى الأدوية الموجودة في الدراسة. لم يسمح بمعايرة الجرعة من Onglyza أثناء الدراسة.
بالاقتران مع glyburide ، قدم Onglyza 2.5 ملغ و 5 ملغ تحسينات كبيرة في A1C ، FPG ، و PPG مقارنة مع مجموعة الدواء الوهمي بالإضافة إلى مجموعة glyburide أعلى (الجدول 6). كانت نسبة المرضى الذين توقفوا بسبب عدم وجود مراقبة نسبة السكر في الدم أو الذين تم إنقاذهم لتلبية معايير نسبة السكر في الدم المحددة مسبقا 18 ٪ في إضافة Onglyza 2.5 ملغ إلى مجموعة glyburide ، و 17٪ من مجموعة Onglyza 5 mg إلى مجموعة glyburide ، و 30٪ في مجموعة الدواء الوهمي بالإضافة إلى glyburide لأعلى مجموعة.
الجدول 6: معلمات نسبة السكر في الدم في الأسبوع 24 في دراسة تسيطر عليها وهمي من Onglyza كعلاج الجمع بين الوظيفة مع Glyburide *
| معلمة الفعالية | Onglyza 2.5 ملغ + غليبوريد 7.5 ملغ N = 248 |
Onglyza 5 ملغ + غليبوريد 7.5 ملغ N = 253 |
الوهمي + غليبوريد متابعة المعاير N = 267 |
|---|---|---|---|
| * نية لعلاج السكان باستخدام الملاحظة الأخيرة في الدراسة أو الملاحظة الأخيرة قبل العلاج الإنقاذ الميتفورمين للمرضى الذين يحتاجون إلى الإنقاذ. | |||
| †المربعات الصغرى تعني ضبط القيمة الأساسية. | |||
| ج قيمة p <0.0001 مقارنةً بالعلاج المموه + غليبوريد أعلى | |||
| § قيمة p <0.05 مقارنةً بالعلاج الوهمي + غليبوريد غليبيريد | |||
| الهيموجلوبين A1C (٪) | N = 246 | N = 250 | N = 264 |
| خط الأساس (الوسط) | 8.4 | 8.5 | 8.4 |
| التغيير من الأساس (المعدل المعدل)†) | −0.5 | −0.6 | +0.1 |
| الفرق من glyburide أعلى المعايرة (المعدل المعدل†) | −0.6ج | −0.7ج | |
| 95 ٪ فاصل الثقة | (−0.8, −0.5) | (−0.9, −0.6) | |
| نسبة المرضى الذين حققوا A1C <7٪ | 22% §(55/246) | 23% §(57/250) | 9% (24/264) |
| صيام الجلوكوز في البلازما (mg / dL) | N = 247 | N = 252 | N = 265 |
| خط الأساس (الوسط) | 170 | 175 | 174 |
| التغيير من الأساس (المعدل المعدل)†) | −7 | −10 | +1 |
| الفرق من glyburide أعلى المعايرة (المعدل المعدل†) | −8 § | −10 § | |
| 95 ٪ فاصل الثقة | (−14, −1) | (−17, −4) | |
| 2 ساعة بعد الجلوكوز (ملغ / ديسيلتر) | N = 195 | N = 202 | N = 206 |
| خط الأساس (الوسط) | 309 | 315 | 323 |
| التغيير من الأساس (المعدل المعدل)†) | −31 | −34 | +8 |
| الفرق من glyburide أعلى المعايرة (المعدل المعدل†) | −38 § | −42 § | |
| 95 ٪ فاصل الثقة | (−50, −27) | (−53, −31) |
Coadministration مع الميتفورمين في علاج المرضى ساذج
شارك ما مجموعه 1306 مريضاً ساذجًا بالعلاج مصابين بداء السكري من النوع 2 في هذه التجربة العشوائية التي استمرت 24 أسبوعًا والتي خضعت للتحكم بالغفل تقييم فعالية وسلامة Onglyza coadministered مع الميتفورمين في المرضى الذين يعانون من نقص السكر في الدم السيطرة (A1C - 8 ٪ إلى ¤12 ٪) على النظام الغذائي وممارسة الرياضة وحده. كان مطلوبا من المرضى أن يكونوا ساذجين للعلاج في هذه الدراسة.
تم تسجيل المرضى الذين حققوا معايير الأهلية في فترة واحدة من المكفوفين ، لمدة أسبوع واحد ، وهمي في ممارسة الرياضة والغذاء. تم اختيارهم بصورة عشوائية المرضى إلى واحد من أربعة أذرع العلاج: Onglyza 5 ملغ + ميتفورمين 500 ملغ ، ساكساجليتين 10 ملغ + ميتفورمين 500 ملغ ، ساكساجليبتين 10 ملغ + وهمي ، أو ميتفورمين 500 ملغ + وهمي. تم جرعات Onglyza مرة واحدة يوميًا. في مجموعات العلاج الثلاثة التي تستخدم الميتفورمين ، تم زيادة جرعة الميتفورمين أسبوعيًا بزيادات مقدارها 500 ملغ يوميًا ، كما هو مسموح به ، بحد أقصى 2000 ملغ يوميًا على أساس FPG. تم علاج المرضى الذين فشلوا في تحقيق أهداف نسبة السكر في الدم خلال الدراسات مع الإنقاذ بيوجليتازون كعلاج إضافي.
قدمت الإدارة المشتركة لـ Onglyza 5 mg plus metformin تحسينات كبيرة في A1C و FPG و PPG مقارنة مع الدواء الوهمي بالإضافة إلى الميتفورمين (الجدول 7).
الجدول 7: معلمات نسبة السكر في الدم في الأسبوع 24 في تجربة خاضعة للتحكم الغفل للإدارة Onglyza مع الميتفورمين في مرضى ساذج العلاج
| معلمة الفعالية | Onglyza 5 ملغ + ميتفورمين N = 320 |
الوهمي + ميتفورمين N = 328 |
|---|---|---|
| * النية لعلاج السكان باستخدام الملاحظة الأخيرة في الدراسة أو الملاحظة الأخيرة قبل العلاج الإنقاذ بيوجليتازون للمرضى الذين يحتاجون إلى الإنقاذ. | ||
| †المربعات الصغرى تعني ضبط القيمة الأساسية. | ||
| ج قيمة p <0.0001 مقارنة مع الدواء الوهمي + الميتفورمين | ||
| § قيمة p <0.05 مقارنة مع الدواء الوهمي + الميتفورمين | ||
| الهيموجلوبين A1C (٪) | N = 306 | N = 313 |
| خط الأساس (الوسط) | 9.4 | 9.4 |
| التغيير من الأساس (المعدل المعدل)†) | −2.5 | −2.0 |
| الفرق من الدواء الوهمي + الميتفورمين (المعدل المعدل)†) | −0.5ج | |
| 95 ٪ فاصل الثقة | (−0.7, −0.4) | |
| نسبة المرضى الذين حققوا A1C <7٪ | 60% §(185/307) | 41% (129/314) |
| صيام الجلوكوز في البلازما (mg / dL) | N = 315 | N = 320 |
| خط الأساس (الوسط) | 199 | 199 |
| التغيير من الأساس (المعدل المعدل)†) | −60 | −47 |
| الفرق من الدواء الوهمي + الميتفورمين (المعدل المعدل)†) | −13 § | |
| 95 ٪ فاصل الثقة | (−19, −6) | |
| 2 ساعة بعد الجلوكوز (ملغ / ديسيلتر) | N = 146 | N = 141 |
| خط الأساس (الوسط) | 340 | 355 |
| التغيير من الأساس (المعدل المعدل)†) | −138 | −97 |
| الفرق من الدواء الوهمي + الميتفورمين (المعدل المعدل)†) | −41 § | |
| 95 ٪ فاصل الثقة | (−57, −25) |
أعلى
كيف زودت
تحتوي أقراص Onglyza ™ (saxagliptin) على علامات على كلا الجانبين وتتوفر في نقاط القوة والحزم المدرجة في الجدول 8.
| لوح قوة |
فيلم المغلفة اللوحي اللون / الشكل |
لوح علامات |
حجم العبوة | رمز NDC |
|---|---|---|---|---|
| 5 ملغ | زهري biconvex ، الجولة |
"5" على جانب واحد و "4215" على الجانب الخلفي ، بالحبر الأزرق | زجاجات من 30 زجاجات من 90 زجاجات من 500 نفطة 100 |
0003-4215-11 0003-4215-21 0003-4215-31 0003-4215-41 |
| 2.5 ملغ | شاحب أصفر إلى أصفر فاتح biconvex ، الجولة |
"2.5" على جانب واحد و "4214" في الخلف ، بالحبر الأزرق | زجاجات من 30 زجاجات من 90 |
0003-4214-11 0003-4214-21 |
التخزين والمناولة
متجر في 20 درجة مئوية -25 درجة مئوية (68 درجة -77 درجة فهرنهايت) ؛ الرحلات المسموح بها إلى 15 درجة -30 درجة مئوية (59 درجة -86 درجة فهرنهايت) [انظر درجة حرارة الغرفة التي تسيطر عليها جامعة جنوب المحيط الهادئ].
أعلى
آخر تحديث: 07/09
E.R. Squibb & Sons، L.L.C.
معلومات المريض Onglyza
معلومات مفصلة عن العلامات والأعراض والأسباب والعلاج من مرض السكري
لا تهدف المعلومات الواردة في هذه الدراسة إلى تغطية جميع الاستخدامات أو الاتجاهات أو الاحتياطات الممكنة أو التفاعلات الدوائية أو الآثار الضارة. هذه المعلومات معممة ولا تهدف إلى تقديم المشورة الطبية المحددة. إذا كانت لديك أسئلة حول الأدوية التي تتناولها أو ترغب في مزيد من المعلومات ، فاستشر طبيبك أو الصيدلي أو الممرض.
ارجع الى: تصفح جميع الأدوية لمرض السكري



