Janumet لعلاج مرض السكري
اسم العلامة التجارية: Janumet
الاسم العام: سيتاغليبتين وميتفورمين هيدروكلوريد
محتويات:
مؤشرات والاستخدام
الجرعة والإدارة
أشكال الجرعات ونقاط القوة
موانع
المحاذير والإحتياطات
ردود الفعل السلبية
تفاعل الأدوية
استخدام في السكان محددة
جرعة مفرطة
وصف
علم العقاقير
علم السموم غير الإكلينيكي
الدراسات السريرية
كيف زودت
معلومات استشارة المريض
Janumet ، Sitagliptin و Metformin هيدروكلوريد ، معلومات للمرضى (في سهل الانجليزية)
تحذير: الحماض اللبني
الحماض اللبني من المضاعفات الخطيرة النادرة التي قد تحدث بسبب تراكم الميتفورمين. يزداد الخطر مع حالات مثل تعفن الدم والجفاف وزيادة تناول الكحول ، والقصور الكبدي ، وضعف الكلى ، وفشل القلب الاحتقاني الحاد.
تكون البداية في الغالب خفية ، مصحوبة فقط بأعراض غير محددة مثل الشعور بالضيق ، وألم عضلي ، وضيق في التنفس ، وزيادة النعاس ، وضيق في البطن غير محدد. تشوهات المختبرات تشمل انخفاض الرقم الهيدروجيني ، وزيادة الفجوة في أنيون وارتفاع اللاكتات في الدم.
إذا يشتبه الحماض ، Janumet1 يجب وقفها وإدخال المريض إلى المستشفى على الفور. [نرى المحاذير والإحتياطات]
مؤشرات والاستخدام
يشار إلى Janumet كعامل مساعد في اتباع نظام غذائي وممارسة لتحسين السيطرة على نسبة السكر في الدم لدى البالغين الذين يعانون من داء السكري من النوع 2 عندما يكون العلاج مع كل من سيتاجليبتين والميتفورمين مناسبا. [نرى
الدراسات السريرية.]القيود الهامة للاستخدام
لا ينبغي أن تستخدم Janumet في المرضى الذين يعانون من مرض السكري من النوع 1 أو لعلاج الحماض الكيتوني السكري ، لأنها لن تكون فعالة في هذه الإعدادات.
لم يتم دراسة Janumet في تركيبة مع الأنسولين.
أعلى
الجرعة والإدارة
الجرعات الموصى بها
يجب أن يتم تخصيص جرعة العلاج بفرط سكر الدم باستخدام Janumet على أساس نظام المريض الحالي ، الفعالية ، والتسامح مع عدم تجاوز الحد الأقصى الموصى به من الجرعة اليومية من 100 ملغ سيتاجليبتين و 2000 ملغ الميتفورمين. يجب أن يكون العلاج المركب الأولي أو الحفاظ على الجمع بين العلاج فرديًا ويترك لتقدير مقدم الرعاية الصحية.
عموما يجب إعطاء جانوميت مرتين يوميا مع وجبات الطعام ، مع تصاعد الجرعة تدريجيا ، للحد من الآثار الجانبية المعدية المعوية (GI) بسبب الميتفورمين.
يجب أن تعتمد جرعة البدء من Janumet على نظام المريض الحالي. يجب أن تعطى Janumet مرتين يوميا مع وجبات الطعام. الجرعات التالية متوفرة:
50 ملغ سيتاجليبتين / 500 ملغ ميتفورمين هيدروكلوريد
50 ملغ سيتاجليبتين / 1000 ملغ ميتفورمين هيدروكلوريد.
المرضى لا يسيطرون بشكل كاف على النظام الغذائي وممارسة الرياضة وحدها
إذا كان العلاج باستخدام قرص مركب يحتوي على سيتاجليبتين والميتفورمين مناسبًا لمرضى السكري من النوع 2 عدم التحكم بشكل كاف في النظام الغذائي وممارسة التمرينات الرياضية وحدها ، جرعة البدء الموصى بها هي 50 ملغ سيتاجليبتين / 500 ملغ هيدروكلوريد الميتفورمين مرتين اليومي. يمكن معايرة المرضى الذين لا يتحكمون في نسبة السكر في الدم غير الكافية في هذه الجرعة حتى 50 ملغ من سيتاغليبتين / 1000 ملغ هيدروكلوريد الميتفورمين مرتين يوميًا.
المرضى تسيطر بشكل غير كاف على حيد الميتفورمين
إذا كان العلاج باستخدام قرص مركب يحتوي على سيتاجليبتين وميتفورمين مناسبًا للمريض الذي لا يتحكم بشكل كافٍ في الميتفورمين وحده ، يجب أن توفر جرعة البدء الموصى بها من Janumet جرعات سيتاجليبتين بجرعة 50 ملغ مرتين يوميًا (100 ملغ من الجرعة اليومية الكلية) وجرعة الميتفورمين التي يجري بالفعل تؤخذ. بالنسبة للمرضى الذين يتناولون الميتفورمين 850 ملغ مرتين يوميًا ، فإن جرعة البداية الموصى بها من Janumet هي 50 ملغ من سيتاغليبتين / 1000 ملغ من الميتفورمين هيدروكلوريد مرتين يوميًا.
المرضى تسيطر عليها بشكل غير كاف على حيدة سيتاجليبتين
إذا كان العلاج باستخدام قرص مركب يحتوي على سيتاجليبتين و ميتفورمين مناسبًا للمريض بشكل غير ملائم يتم التحكم في سيتاغليبتين وحده ، جرعة البداية الموصى بها من جانوميت هي 50 ملغ سيتاجليبتين / 500 ملغ ميتفورمين هيدروكلوريد مرتين اليومي. يمكن معايرة المرضى الذين لا يتحكمون بشكل كافٍ في هذه الجرعة حتى 50 ملغ من سيتاغليبتين / 1000 ملغ من الميتفورمين هيدروكلوريد مرتين يوميًا. لا ينبغي تبديل المرضى الذين يتناولون جرعة سيتاجليبتين أحادية الضبط لتعديل القصور الكلوي إلى جانوميت [انظر موانع].
المرضى التبديل من الإدارة المشتركة ل sitagliptin والميتفورمين
بالنسبة للمرضى الذين يتحولون من سيتاجلبتيين بإدارة مشتركة مع الميتفورمين ، قد يتم إطلاق جانوميت بجرعة سيتاجليبتين والميتفورمين الذي تم تناوله بالفعل.
المرضى لا يتحكمون بشكل كافٍ في العلاج المزدوج المركب مع أي اثنين من عوامل ارتفاع السكر في الدم التالية: سيتاجليبتين ، ميتفورمين أو سلفونيل يوريا
إذا كان العلاج مع مجموعة أقراص تحتوي على سيتاجليبتين والميتفورمين يعتبر مناسبًا في هذا الإعداد ، يجب أن توفر جرعة البداية المعتادة من Janumet جرعات سيتاغليبتين بجرعة 50 ملغ مرتين يوميًا (إجمالي 100 ملغ جرعة يومية). عند تحديد جرعة البدء لمكون الميتفورمين ، يجب مراعاة مستوى التحكم في نسبة السكر في الدم لدى المريض والجرعة الحالية (إن وجدت) من الميتفورمين. ينبغي النظر في تصاعد الجرعة التدريجية لتقليل الآثار الجانبية المعدية المعوية (GI) المرتبطة بالميتفورمين. قد يحتاج المرضى الموجودون حاليًا أو الذين يبدأون في استخدام السلفونيل يوريا إلى جرعات أقل من السلفونيل يوريا لتقليل خطر نقص السكر في الدم [انظر المحاذير والإحتياطات].
لم يتم إجراء أي دراسات على وجه التحديد لفحص سلامة وفعالية Janumet في المرضى الذين عولجوا سابقًا مع عوامل أخرى لفرط سكر الدم عن طريق الفم وتحولوا إلى Janumet. يجب إجراء أي تغيير في علاج مرض السكري من النوع 2 بعناية ومراقبة مناسبة حيث يمكن أن تحدث تغييرات في السيطرة على نسبة السكر في الدم.
أعلى
أشكال الجرعات ونقاط القوة
- 50 ملغ / 500 ملغ هي أقراص زهرية فاتحة ، على شكل كبسولة ، مغلفة بالفيلم مع "575" مزخرف على جانب واحد.
- 50 ملغ / 1000 ملغ هي أقراص حمراء ، على شكل كبسولة ، مغلفة بالأفلام مع "577" debossed على جانب واحد.
أعلى
موانع
بطلان Janumet (سيتاجليبتين / ميتفورمين حمض الهيدروكلوريك) في المرضى الذين يعانون من:
- مرض كلوي أو اختلال وظيفي كلوي ، على سبيل المثال ، كما هو مقترح بمستويات الكرياتينين في المصل - 1.5 ملغ / ديسيلتر [ذكور] ، أو 1.4 ملغ / ديسيلتر [إناث] أو غير طبيعي خلوص الكرياتينين الذي قد ينتج أيضًا عن حالات مثل الانهيار القلبي الوعائي (صدمة) ، احتشاء عضلة القلب الحاد ، وتسمم الدم [نرى المحاذير والإحتياطات].
- الحماض الأيضي الحاد أو المزمن ، بما في ذلك الحماض الكيتوني السكري ، مع أو بدون غيبوبة.
- تاريخ رد فعل فرط الحساسية الشديد لجانوميت أو سيتاجليبتين (أحد مكونات جانوميت) ، مثل الحساسية المفرطة أو وذمة وعائية. [نرى المحاذير والإحتياطات و ردود الفعل السلبية.]
يجب إيقاف الجانوميت مؤقتًا في المرضى الذين يخضعون لدراسات إشعاعية تشمل داخل الأوعية الدموية إدارة مواد التباين المعالج باليود ، لأن استخدام هذه المنتجات قد يؤدي إلى تغيير حاد في الكلى وظيفة [انظر المحاذير والإحتياطات].
أعلى
المحاذير والإحتياطات
الحماض اللبني
الميتفورمين هيدروكلوريد
الحماض اللبني هو أحد المضاعفات الأيضية النادرة والخطيرة التي يمكن أن تحدث بسبب تراكم الميتفورمين أثناء العلاج مع Janumet ؛ عندما يحدث ذلك ، فإنه قاتل في حوالي 50 ٪ من الحالات. قد يحدث الحماض اللبني أيضًا بالترافق مع عدد من الحالات الفسيولوجية المرضية ، بما في ذلك داء السكري ، وكلما كان هناك نقص كبير في أنسجة الأنسجة ونقص الأكسجة في الدم. يتميز الحماض اللبنيك بمستويات مرتفعة من اللاكتات في الدم (> 5 مليمول / لتر) ، وانخفاض درجة الحموضة في الدم ، واضطرابات بالكهرباء مع زيادة فجوة الأنيون ، وزيادة نسبة اللاكتات / البيروفات. عندما يتورط الميتفورمين كسبب للحماض اللبني ، توجد مستويات بلازما الميتفورمين التي تزيد عن 5 ميكروغرام / مل.
إن نسبة الإصابة بحماض اللبنيك المبلغ عنها في المرضى الذين يتلقون هيدروكلوريد الميتفورمين منخفضة للغاية (حوالي 0.03 حالة / 1000 مريض - سنة ، مع ما يقرب من 0.015 حالات مميتة / 1000 المريض عاما). في أكثر من 20،000 سنة من التعرض للميتفورمين في التجارب السريرية ، لم تكن هناك تقارير عن الحماض اللبني. حدثت الحالات المبلغ عنها في المقام الأول في مرضى السكري الذين يعانون من قصور كلوي كبير ، بما في ذلك كل من الكلى جوهري المرض ونقص جريان الدم الكلوي ، غالبًا في ظل مشاكل طبية / جراحية متعددة مصاحبة وما يصاحب ذلك الأدوية. المرضى الذين يعانون من قصور القلب الاحتقاني الذي يحتاج إلى إدارة دوائية ، لا سيما أولئك الذين يعانون من عدم الاستقرار أو قصور القلب الاحتقاني الحاد الذي يتعرض لخطر نقص تدفق الدم ونقص الأكسجة الحماض. يزداد خطر الإصابة بالحماض اللبني بزيادة درجة الخلل الكلوي وعمر المريض. وبالتالي ، قد ينخفض خطر الإصابة بحماض اللبنيك بشكل كبير من خلال المراقبة المنتظمة لوظيفة الكلى لدى المرضى الذين يتناولون الميتفورمين وباستخدام الجرعة الفعالة الدنيا من الميتفورمين. على وجه الخصوص ، ينبغي أن يكون علاج كبار السن مصحوبًا برصد دقيق لوظيفة الكلى. لا ينبغي أن يبدأ علاج الميتفورمين في المرضى الذين تتراوح أعمارهم بين 80 عامًا ما لم يتم قياس تصفية الكرياتينين يوضح أنه لا يتم تقليل وظائف الكلى ، لأن هؤلاء المرضى أكثر عرضة للإصابة بالحماض اللبني. بالإضافة إلى ذلك ، يجب حجب الميتفورمين على الفور في وجود أي حالة مرتبطة بنقص التأكسج في الدم أو الجفاف أو التسمم. نظرًا لأن ضعف وظائف الكبد قد يحد بشكل كبير من القدرة على إزالة اللاكتات ، يجب تجنب الميتفورمين عمومًا في المرضى الذين لديهم أدلة سريرية أو مخبرية على مرض الكبد. يجب تحذير المرضى من الإفراط في تناول الكحوليات ، سواء كانت حادة أو مزمنة ، عند تناول الميتفورمين ، لأن الكحول يعزز آثار الميتفورمين هيدروكلوريد على استقلاب اللاكتات. بالإضافة إلى ذلك ، يجب إيقاف الميتفورمين مؤقتًا قبل إجراء أي دراسة حول التداخل الشعاعي داخل الأوعية وأي إجراء جراحي [انظر المحاذير والإحتياطات].
غالبًا ما يكون ظهور الحماض اللبني خفيًا ، ولا يرافقه سوى أعراض غير محددة مثل الشعور بالضيق ، ألم عضلي ، ضائقة تنفسية ، زيادة النعاس ، وضيق البطن غير المحدد. قد يكون هناك انخفاض حرارة الجسم ، انخفاض ضغط الدم ، وعدم انتظام ضربات القلب المقاوم مع الحماض أكثر وضوحا. يجب أن يكون المريض وطبيب المريض على دراية بالأهمية المحتملة لمثل هذه الأعراض ، ويجب توجيه المريض لإخطار الطبيب فور حدوثها [انظر المحاذير والإحتياطات]. يجب سحب الميتفورمين حتى يتم توضيح الموقف. قد يكون من المفيد إلكتروليتات المصل والكيتونات والجلوكوز في الدم ، وإذا كان ذلك موضحًا ، فقد تكون درجة الحموضة في الدم ومستويات اللاكتات وحتى مستويات الميتفورمين في الدم مفيدة. بمجرد استقرار المريض على أي مستوى جرعة من الميتفورمين ، من غير المرجح أن تكون أعراض الجهاز الهضمي ، والتي هي شائعة أثناء بدء العلاج ، مرتبطة بالمخدرات. قد يحدث في وقت لاحق من أعراض الجهاز الهضمي بسبب الحماض اللبني أو غيرها من الأمراض الخطيرة.
مستويات الصيام لاكتات البلازما الوريدية أعلى من الحد الأعلى الطبيعي ولكن أقل من 5 مليمول / لتر في المرضى الذين يتناولون الميتفورمين لا تشير بالضرورة إلى اكتئاب وشيك الحماض ويمكن تفسيره عن طريق آليات أخرى ، مثل مرض السكري أو السمنة التي يتم التحكم فيها بشكل سيئ ، أو النشاط البدني القوي ، أو المشكلات الفنية في التعامل مع العينات [نرى المحاذير والإحتياطات].
يجب أن يشتبه الحماض اللبني في أي مريض السكري مع الحماض الأيضي تفتقر إلى دليل على الحماض الكيتوني (كيتونوريا وكيتونيا).
الحماض اللبني هو حالة طبية طارئة يجب معالجتها في المستشفى. في المريض المصاب بالحماض اللبني الذي يتناول الميتفورمين ، يجب إيقاف الدواء على الفور واتخاذ تدابير داعمة عامة على الفور. لأن هيدروكلوريد الميتفورمين قابل للغسل (مع إزالة تصل إلى 170 مل / دقيقة تحت ديناميكية ديناميكية جيدة الظروف) ، ينصح غسيل الكلى السريع لتصحيح الحماض وإزالة المتراكمة الميتفورمين. وغالبًا ما تؤدي هذه الإدارة إلى عكس الأعراض وسرعة الشفاء [انظر موانع; المحاذير والإحتياطات].
اختلال وظائف الكبد
بما أن اختلال وظائف الكبد قد ارتبط ببعض حالات الحماض اللبني ، فيجب تجنب جانوميت بشكل عام في المرضى الذين لديهم أدلة سريرية أو مخبرية على مرض الكبد.
تقييم وظيفة الكلى
من المعروف أن الميتفورمين وال سيتاجليبتين يفرزان بشكل كبير عن طريق الكلية. يزداد خطر تراكم الميتفورمين والحماض اللبني مع زيادة درجة ضعف وظائف الكلى. وبالتالي ، فإن المرضى الذين يعانون من مستويات الكرياتينين في الدم أعلى من الحد الأعلى الطبيعي لسنهم يجب ألا يتلقوا Janumet. في كبار السن ، يجب معايرة Janumet بعناية لتحديد الحد الأدنى للجرعة لتأثير نسبة السكر في الدم المناسبة ، لأن الشيخوخة يمكن أن ترتبط مع انخفاض وظيفة الكلى. [نرى المحاذير والإحتياطات و استخدام في السكان محددة.]
قبل الشروع في العلاج مع Janumet ، وبعد ذلك على الأقل سنويًا ، يجب تقييم وظيفة الكلى والتحقق منها بشكل طبيعي. في المرضى الذين يتوقع حدوث خلل وظيفي في الكلى ، خاصة في المرضى المسنين ، كلوي يجب تقييم الوظيفة بشكل متكرر وإيقاف Janumet في حالة وجود دليل على ضعف الكلى حاضر.
فيتامين ب12 مستويات
في التجارب السريرية الخاضعة للرقابة من الميتفورمين لمدة 29 أسبوعا ، وانخفاض إلى مستويات دون طبيعية من المصل الطبيعي السابق فيتامين ب12 وقد لوحظت مستويات ، دون المظاهر السريرية ، في ما يقرب من 7 ٪ من المرضى. هذا النقص ، ربما بسبب التداخل مع B12 امتصاص من ب12معقد للعامل الداخلي ، نادراً ما يرتبط بفقر الدم ويبدو أنه يمكن عكسه بسرعة عن طريق إيقاف الميتفورمين أو فيتامين ب12 مكملات. ينصح بقياس المعلمات الدموية على أساس سنوي في المرضى الذين يعانون من Janumet وينبغي التحقيق في أي تشوهات واضحة بشكل صحيح وإدارتها. [نرى ردود الفعل السلبية.]
بعض الأفراد (الذين يعانون من نقص فيتامين ب12 أو تناول الكالسيوم أو امتصاصه) يبدو أنه مهيأ لتطوير فيتامين ب دون الطبيعي12 المستويات. في هؤلاء المرضى ، مصل فيتامين ب الروتيني12 قد تكون القياسات على فترات من سنتين إلى ثلاث سنوات مفيدة.
تناول الكحول
من المعروف أن الكحول يحفز تأثير الميتفورمين على استقلاب اللاكتات. لذا ، يجب تحذير المرضى من الإفراط في تناول الكحول ، سواء كان حادًا أو مزمنًا ، أثناء تلقيهم لجانوميت.
العمليات الجراحية
يجب تعليق استخدام Janumet مؤقتًا لأي عملية جراحية (باستثناء الإجراءات البسيطة غير المرتبطة بالمدخول المقيد من الطعام والسوائل) ويجب عدم إعادة تشغيله حتى يتم استئناف تناول المريض عن طريق الفم وتقييم وظيفة الكلى على أنها عادي.
التغير في الحالة السريرية للمرضى المصابين بمرض السكري من النوع الثاني الذي سبق التحكم فيه
مريض مصاب بداء السكري من النوع الثاني كان يسيطر عليه من قبل بشكل جيد على جانوميت الذي يعاني من تشوهات في المختبرات أو سريرية يجب تقييم المرض (وخاصة المرض الغامض والمعرّف بشكل سيئ) على الفور للحصول على أدلة على الحماض الكيتوني أو اللبنيك الحماض. يجب أن يشمل التقييم الشوارد والكيتونات في الدم ، والجلوكوز في الدم ، وإذا كان ذلك موضحًا ، فإن درجة الحموضة في الدم ، واللاكتات ، والبيروفات ، والميتفورمين. في حالة حدوث الحماض في أي من النموذجين ، يجب إيقاف Janumet على الفور والبدء في اتخاذ تدابير تصحيحية مناسبة.
استخدم مع الأدوية المعروفة لتسبب نقص السكر في الدم
سيتاقلبتين
كما هو الحال مع العوامل الأخرى لفرط سكر الدم المستخدمة في توليفة مع سلفونيل يوريا ، عندما تم استخدام سيتاجليبتين مع الميتفورمين و السلفونيل يوريا ، وهو دواء معروف بأنه يسبب نقص السكر في الدم ، وقد زاد معدل الإصابة بنقص السكر في الدم عن الدواء الوهمي بالاشتراك مع الميتفورمين و سلفونيلوريا [انظر ردود الفعل السلبية]. لذلك ، قد يحتاج المرضى الذين يتلقون أيضًا إفراز الأنسولين (مثل السلفونيل يوريا والميغليتينيد) إلى جرعة أقل من إفراز الأنسولين لتقليل خطر نقص السكر في الدم [انظر الجرعة والإدارة].
الميتفورمين هيدروكلوريد
لا يحدث نقص السكر في الدم في المرضى الذين يتلقون الميتفورمين بمفردهم في ظل ظروف الاستخدام المعتادة ، ولكن يمكن أن يحدث عندما تكون كمية السعرات الحرارية ناقصة ، عندما لا يتم تعويض التمرينات الشاقة من خلال إضافة السعرات الحرارية ، أو أثناء الاستخدام المصاحب لعوامل أخرى لخفض الجلوكوز (مثل السلفونيل يوريا والإنسولين) أو الإيثانول. المرضى المسنون أو الوهن أو المصابين بسوء التغذية ، والذين يعانون من قصور الغدة الكظرية أو الغدة النخامية أو تسمم الكحول معرضون بشكل خاص لآثار سكر الدم. قد يكون من الصعب التعرف على نقص السكر في الدم لدى كبار السن ، وفي الأشخاص الذين يتناولون عقاقير مضادة للدرنة في الجسم.
الأدوية المصاحبة التي تؤثر على وظيفة الكلى أو التخلص من الميتفورمين
الأدوية المصاحبة التي قد تؤثر على وظائف الكلى أو تؤدي إلى تغير كبير في الدورة الدموية تتداخل مع التخلص من الميتفورمين ، مثل الأدوية الكاتيونية التي يتم القضاء عليها عن طريق إفراز أنبوبي كلوي [نرى تفاعل الأدوية] ، يجب أن تستخدم بحذر.
دراسات إشعاعية باستخدام مواد التباين باليود داخل الأوعية
دراسات التباين داخل الأوعية مع المواد المُعالجة باليود (على سبيل المثال ، التصوير البولي عن طريق الوريد ، تصوير الأوعية الصفراوية في الوريد ، تصوير الأوعية ، والمسح المقطعي (CT) مع التباين داخل الأوعية الدموية) يمكن أن يؤدي إلى تغيير حاد في وظائف الكلى وارتبط مع الحماض اللبني في المرضى الذين يتلقون الميتفورمين [انظر موانع]. لذلك ، في المرضى الذين يتم التخطيط لإجراء مثل هذه الدراسة ، يجب إيقاف Janumet مؤقتًا في وقت أو قبل الإجراء ، وتم حجبه لمدة 48 ساعة بعد الإجراء ولم يتم إعادته إلا بعد إعادة تقييم وظيفة الكلى ووجد أنها تكون طبيعية.
الدول نقص الأوكسجين
الانهيار القلبي الوعائي (صدمة) من أي سبب ، وفشل القلب الاحتقاني الحاد ، واحتشاء عضلة القلب الحاد و الحالات الأخرى التي تتميز بنقص الأكسجة قد ارتبطت بالحماض اللبني وقد تتسبب أيضًا في حدوث اضطراب ما قبل البلع آزوتيمية. عندما تحدث مثل هذه الأحداث في المرضى الذين يتلقون علاج Janumet ، يجب إيقاف الدواء على الفور.
فقدان السيطرة على السكر في الدم
عندما يستقر المريض على أي نظام مصاب بالسكري يتعرض للإجهاد مثل الحمى أو الصدمة أو العدوى أو الجراحة ، فقد يحدث فقدان مؤقت للتحكم في نسبة السكر في الدم. في مثل هذه الأوقات ، قد يكون من الضروري حجب Janumet وإعطاء الأنسولين مؤقتًا. قد يتم إعادة تشغيل Janumet بعد حل المشكلة الحادة.
تفاعلات فرط الحساسية
كانت هناك تقارير ما بعد التسويق عن تفاعلات فرط الحساسية الخطيرة في المرضى الذين عولجوا بالستاغليبتين ، أحد مكونات جانوميت. تتضمن هذه التفاعلات الحساسية المفرطة ، الوذمة الوعائية ، وأمراض الجلد التقشري بما في ذلك متلازمة ستيفنز جونسون. نظرًا لأن ردود الفعل هذه يتم الإبلاغ عنها طوعًا من مجموعة ذات حجم غير مؤكد ، فهي بشكل عام لا يمكن تقدير تواترها بشكل موثوق أو إقامة علاقة سببية بالتعرض للعقاقير. حدث ظهور هذه التفاعلات خلال الأشهر الثلاثة الأولى بعد بدء العلاج باستخدام سيتاجليبتين ، مع حدوث بعض التقارير بعد الجرعة الأولى. في حالة الاشتباه في حدوث تفاعل فرط الحساسية ، توقف عن استخدام Janumet ، وقم بتقييم الأسباب المحتملة الأخرى للحدث ، وابدأ علاجًا بديلاً لمرض السكري. [نرى ردود الفعل السلبية.]
نتائج الاوعية الدموية الكبيرة
لم تكن هناك دراسات سريرية تثبت وجود أدلة قاطعة على الحد من مخاطر الأوعية الدموية الكبرى مع جانوميت أو أي دواء آخر مضاد للسكري.
أعلى
ردود الفعل السلبية
تجارب التجارب السريرية
لأن التجارب السريرية تجرى في ظل ظروف متباينة على نطاق واسع ، لوحظت معدلات رد فعل سلبية في التجارب السريرية لـ لا يمكن مقارنة الدواء مباشرة بالمعدلات في التجارب السريرية لعقار آخر وقد لا يعكس المعدلات التي لوحظت فيها ممارسة.
سيتاجلبتين و ميتفورمين الإدارة المشتركة في المرضى الذين يعانون من مرض السكري من النوع 2 تسيطر بشكل غير كاف على النظام الغذائي وممارسة
يلخص الجدول 1 ردود الفعل السلبية الأكثر شيوعًا (حوالي 5٪ من المرضى) المُبلغ عنها (بغض النظر عن تقييم الباحث للسببية) خلال 24 أسبوعًا دراسة عامليّة مسيطر عليها بالعلاج الوهمي ، والتي تمت فيها مشاركة سيتاجلبتين وميتفورمين لمرضى السكري من النوع الثاني غير الخاضعين للسيطرة الكافية على النظام الغذائي وممارسة التمارين الرياضية.
الجدول 1: سيتاغليبتين والميتفورمين يشتركان في إدارتهما مع مرضى السكري من النوع الثاني ، الذين لا يتحكمون بشكل كافٍ في النظام الغذائي وممارسة التمارين: ردود الفعل السلبية المبلغ عنها (بغض النظر عن تقييم الباحث للسببية) في حوالي 5 ٪ من المرضى الذين يتلقون العلاج المركب (وأكثر من المرضى الذين يتلقون الوهمي)*
| عدد المرضى (٪) | ||||
الوهمي |
سيتاقلبتين 100 ملغ |
ميتفورمين 500 ملغ / الميتفورمين 1000 ملغ محاولة†|
سيتاقلبتين 50 ملغ محاولة + ميتفورمين 500 ملغ / الميتفورمين 1000 ملغ محاولة†|
|
| ن = 176 | العدد = 179 | العدد = 364†| العدد = 372†| |
| ||||
| إسهال | 7 (4.0) | 5 (2.8) | 28 (7.7) | 28 (7.5) |
| عدوى الجهاز التنفسي العلوي | 9 (5.1) | 8 (4.5) | 19 (5.2) | 23 (6.2) |
| صداع الراس | 5 (2.8) | 2 (1.1) | 14 (3.8) | 22 (5.9) |
العلاج الإضافي Sitagliptin في المرضى الذين يعانون من داء السكري من النوع 2 يتم التحكم فيه بشكل غير كاف على الميتفورمين وحده
في تجربة استمرت 24 أسبوعًا باستخدام الدواء الوهمي لـ sitagliptin 100 ملغ تُعطى مرة واحدة يوميًا تُضاف إلى نظام الميتفورمين مرتين يوميًا ، لم يكن هناك أي ردود الفعل السلبية المبلغ عنها بصرف النظر عن تقييم الباحث للسببية في 5٪ من المرضى وأكثر شيوعًا من المرضى المعطاة الوهمي. وكان وقف العلاج بسبب ردود الفعل السلبية السريرية مماثلة لمجموعة العلاج الوهمي (سيتاجليبتين والميتفورمين ، 1.9 ٪ ؛ الدواء الوهمي والميتفورمين ، 2.5 ٪).
نقص سكر الدم
استندت ردود الفعل السلبية لنقص السكر في الدم على جميع تقارير نقص السكر في الدم. لم يكن قياس الجلوكوز المتزامن مطلوبًا. كانت نسبة حدوث ردود الفعل السلبية المحددة مسبقًا لنقص السكر في الدم لدى المرضى المصابين بداء السكري من النوع 2 والتي لا يتم التحكم فيها بشكلٍ كافٍ على النظام الغذائي وممارسة التمارين الرياضية 0.6٪ في المرضى الذين تم إعطاؤهم الدواء الوهمي ، و 0.6 ٪ في المرضى الذين تناولوا عقار سيتاجلبتين وحده ، و 0.8 ٪ في المرضى الذين تناولوا عقار الميتفورمين وحده ، و 1.6 ٪ في المرضى الذين تناولوا عقار سيتاغليبتين مع الميتفورمين. في المرضى الذين يعانون من مرض السكري من النوع 2 تسيطر بشكل غير كاف على الميتفورمين وحده ، وحدوث الإصابة السلبية كانت ردود فعل نقص السكر في الدم 1.3 ٪ في المرضى الذين يتناولون سيتاجليبتين الإضافة و 2.1 ٪ في المرضى الذين حصلوا على الإضافة الوهمي.
ردود الفعل السلبية على الجهاز الهضمي
كانت حوادث التجارب الضارة المعوية المختارة مسبقًا في المرضى الذين عولجوا بالستاغليبتين والميتفورمين مماثلة لتلك التي أبلغ عنها للمرضى الذين عولجوا بالميتفورمين فقط. انظر الجدول 2.
الجدول 2: ردود فعل سلبية من الجهاز الهضمي المختارة مسبقا (بغض النظر عن تقييم المحقق من السببية) المبلغ عنها في المرضى الذين يعانون من مرض السكري من النوع 2 تلقي سيتاغليبتين والميتفورمين.
| عدد المرضى (٪) | ||||||
| دراسة Sitagliptin والميتفورمين في المرضى التي تسيطر عليها بشكل غير كاف على النظام الغذائي وممارسة |
دراسة إضافات Sitagliptin في المرضى الذين يعانون من عدم التحكم الكافي في الميتفورمين وحده | |||||
الوهمي |
سيتاقلبتين 100 ملغ |
ميتفورمين 500 ملغ / الميتفورمين 1000 ملغ محاولة* |
سيتاقلبتين 50 ملغ محاولة + ميتفورمين 500 ملغ / الميتفورمين 1000 ملغ محاولة* |
الدواء الوهمي والميتفورمين ¥ ¥ 1500 ملغ يوميا |
Sitagliptin 100 ملغ QD والميتفورمين ¥ ¥ 1500 ملغ يوميا |
|
| ن = 176 | العدد = 179 | العدد = 364 | العدد = 372 | العدد = 237 | ن = 464 | |
| ||||||
| إسهال | 7 (4.0) | 5 (2.8) | 28 (7.7) | 28 (7.5) | 6 (2.5) | 11 (2.4) |
| غثيان | 2 (1.1) | 2 (1.1) | 20 (5.5) | 18 (4.8) | 2 (0.8) | 6 (1.3) |
| قيء | 1 (0.6) | 0 (0.0) | 2 (0.5) | 8 (2.2) | 2 (0.8) | 5 (1.1) |
| وجع بطن†| 4 (2.3) | 6 (3.4) | 14 (3.8) | 11 (3.0) | 9 (3.8) | 10 (2.2) |
Sitagliptin في تركيبة مع الميتفورمين و Glimepiride
في دراسة استمرت 24 أسبوعًا باستخدام الدواء الوهمي لـ sitagliptin 100 mg كعلاج إضافي للمرضى الذين يعانون من داء السكري من النوع 2 لا يتحكمون بشكل كافٍ في الميتفورمين و glimepiride (sitagliptin ، N = 116 ؛ العلاج الوهمي ، N = 113) ، وردود الفعل السلبية ذكرت بغض النظر عن تقييم المحقق من السببية في٪٪٪ 5 ٪ من المرضى تعامل مع sitagliptin وأكثر شيوعا من المرضى الذين عولجوا بالدواء الوهمي كانوا: نقص السكر في الدم (sitagliptin ، 16.4 ٪ ؛ وهمي ، 0.9 ٪) والصداع (6.9 ٪ ، 2.7 ٪).
لم يلاحظ أي تغييرات ذات مغزى سريريا في علامات حيوية أو في تخطيط القلب (بما في ذلك في QTc الفاصل) مع مزيج من سيتاجليبتين والميتفورمين.
ذكرت تجربة سلبية الأكثر شيوعا في حيدة sitagliptin بغض النظر عن المحقق كان تقييم السببية في٪٪ commonly 5 ٪ من المرضى وأكثر شيوعا مما كان عليه في المرضى الذين تلقوا العلاج الوهمي البلعوم الأنفي.
ردود الفعل السلبية الأكثر شيوعًا (> 5٪) الناتجة عن بدء علاج الميتفورمين هي الإسهال والغثيان / القيء وانتفاخ البطن وعدم الراحة في البطن وعسر الهضم والوهن والصداع.
اختبارات المعمل
سيتاقلبتين
كانت حالات ردود الفعل السلبية المختبرية مماثلة في المرضى الذين عولجوا سيتاجليبتين والميتفورمين (7.6 ٪) مقارنة مع المرضى الذين عولجوا بالدواء الوهمي والميتفورمين (8.7 ٪). في معظم الدراسات وليس جميعها ، هناك زيادة صغيرة في عدد خلايا الدم البيضاء (حوالي 200 خلية / ميكرول الفرق في WBC مقابل الدواء الوهمي ؛ يعني لوحظ يعني WBC ما يقرب من 6600 خلية / microL) بسبب زيادة طفيفة في العدلات. هذا التغيير في المعلمات المختبر لا يعتبر ذا صلة سريريا.
الميتفورمين هيدروكلوريد
في التجارب السريرية الخاضعة للرقابة من الميتفورمين لمدة 29 أسبوعا ، وانخفاض إلى مستويات دون طبيعية من المصل الطبيعي السابق فيتامين ب12 وقد لوحظت مستويات ، دون المظاهر السريرية ، في ما يقرب من 7 ٪ من المرضى. هذا النقص ، ربما بسبب التداخل مع B12 امتصاص من ب12معقد للعامل الداخلي ، نادراً ما يرتبط بفقر الدم ويبدو أنه يمكن عكسه بسرعة عن طريق إيقاف الميتفورمين أو فيتامين ب12 مكملات. [نرى المحاذير والإحتياطات.]
تجربة ما بعد التسويق
تم تحديد ردود الفعل السلبية الإضافية التالية أثناء استخدام ما بعد الموافقة على Janumet أو sitagliptin ، أحد مكونات Janumet. نظرًا لأن ردود الفعل هذه يتم الإبلاغ عنها طوعًا من مجموعة ذات حجم غير مؤكد ، فهي بشكل عام لا يمكن تقدير تواترها بشكل موثوق أو إقامة علاقة سببية بالتعرض للعقاقير.
تشمل تفاعلات فرط الحساسية الحساسية المفرطة ، الوذمة الوعائية ، الطفح الجلدي ، الشرى ، التهاب الأوعية الدموية الجلدية ، وحالات الجلد التقشري بما في ذلك متلازمة ستيفنز جونسون [انظر المحاذير والإحتياطات]; عدوى الجهاز التنفسي العلوي؛ الارتفاعات الانزيم الكبدي. التهاب البنكرياس.
أعلى
تفاعل الأدوية
العقاقير الكاتيونية
أدوية الكاتيون (مثل الأميلورايد ، الديجوكسين ، المورفين ، البروكيناميد ، الكينيدين ، الكينين ، الرانيتيدين ، تريامتيرين ، تريميتيريم ، أو فانكومايسين) التخلص من إفراز أنبوبي كلوي نظريًا لديه إمكانية للتفاعل مع الميتفورمين عن طريق التنافس على النقل الأنبوبي الكلوي المشترك الأنظمة. وقد لوحظ هذا التفاعل بين الميتفورمين وسيميتيدين عن طريق الفم لدى المتطوعين الأصحاء العاديين في كل من جرعة الميتفورمين-السيميتيدين أحادية ومتعددة الجرعات دراسات التفاعل الدوائي ، مع زيادة 60 ٪ في ذروة بلازما الميتفورمين وتركيزات الدم الكاملة وزيادة بنسبة 40 ٪ في البلازما والميتفورمين في الدم الكامل AUC. لم يكن هناك تغيير في القضاء على نصف العمر في دراسة جرعة واحدة. لم يكن للميتفورمين أي تأثير على الحرائك الدوائية للسيميتيدين. على الرغم من أن مثل هذه التفاعلات تظل نظرية (باستثناء السيميتيدين) ، إلا أن مراقبة المريض بعناية وتعديل جرعات Janumet و / أو ينصح بتدخل الدواء في المرضى الذين يتناولون الأدوية الموجبة التي تفرز عن طريق إفراز أنبوبي الكلوي القريب النظام.
الديجوكسين
كانت هناك زيادة طفيفة في المنطقة تحت المنحنى (AUC ، 11 ٪) ويعني تركيز الدواء الذروة (Cماكس، 18 ٪) من الديجوكسين مع المشاركة في إدارة سيتاجليبتين 100 ملغ لمدة 10 أيام. لا تعتبر هذه الزيادات ذات مغزى سريريًا. الديجوكسين ، كدواء كاتيوني ، لديه القدرة على التنافس مع الميتفورمين في أنظمة النقل الأنبوبي الكلوي الشائعة ، مما يؤثر على تركيز مصل الديجوكسين أو الميتفورمين أو كليهما. يجب مراقبة المرضى الذين يتلقون الديجوكسين بشكل مناسب. لا يوصى بتعديل جرعة الديجوكسين أو Janumet.
غليبوريد
في دراسة تفاعل جرعة واحدة في مرضى السكري من النوع 2 ، لم يؤد المشاركة في إدارة الميتفورمين والجليبريد إلى أي تغييرات في الدوائية الميتفورمين أو الديناميكا الدوائية. النقصان في glyburide AUC و Cماكس وقد لوحظ ، ولكن كانت متغيرة للغاية. إن طبيعة الجرعة المفردة لهذه الدراسة وعدم وجود علاقة بين مستويات الدم في الغليبيريد والتأثيرات الدوائية تجعل من الأهمية السريرية لهذا التفاعل غير مؤكدة.
فوروسيميد
أظهرت دراسة تفاعل جرعة واحدة من عقار الميتفورمين فوروسيميد في موضوعات صحية أن المعلمات الحركية الدوائية لكلا المركبين تأثرت بالإدارة المشتركة. زاد فوروسيميد بلازما الميتفورمين والدم Cماكس بنسبة 22 ٪ والدم AUC بنسبة 15 ٪ ، دون أي تغيير كبير في إزالة الكلى الميتفورمين. عندما تدار مع الميتفورمين ، فإن جيمماكس و AUC من فوروسيميد كانت 31 ٪ و 12 ٪ أصغر ، على التوالي ، مما كانت عليه عندما تدار وحدها ، و انخفض عمر النصف النهائي بنسبة 32 ٪ ، دون أي تغيير كبير في فوروسيميد الكلى تخليص. لا توجد معلومات متاحة حول تفاعل الميتفورمين والفوروسيميد عندما تتم إدارته بشكل مزمن.
النيفيدبين
أظهرت دراسة تفاعل جرعة واحدة من عقار الميتفورمين-نيفيديبين في المتطوعين الأصحاء العاديين أن المشاركة في تناول النيفيديبين زادت من الميتفورمين البلازماماكس و AUC بنسبة 20 ٪ و 9 ٪ ، على التوالي ، وزيادة كمية تفرز في البول. تيماكس ونصف العمر لم يتأثر. Nifedipine يبدو لتعزيز امتصاص الميتفورمين. وكان الميتفورمين الحد الأدنى من الآثار على نيفيديبين.
استخدام الميتفورمين مع أدوية أخرى
بعض الأدوية تميل إلى إنتاج ارتفاع السكر في الدم وقد تؤدي إلى فقدان السيطرة على نسبة السكر في الدم. وتشمل هذه الأدوية الثيازيدات ومدرات البول الأخرى ، الستيرويدات القشرية ، الفينوثيازين ، منتجات الغدة الدرقية ، الاستروجين ، وسائل منع الحمل عن طريق الفم ، الفينيتوين ، حامض النيكوتين ، محاكيات الودي ، عقاقير منع قنوات الكالسيوم ، و ديزاينوزي. عندما يتم إعطاء هذه الأدوية لمريض يتلقى Janumet ، يجب مراقبة المريض عن كثب للحفاظ على التحكم في نسبة السكر في الدم.
في المتطوعين الأصحاء ، لم تتأثر الحرائك الدوائية للميتفورمين وبروبرانولول ، والميتفورمين والإيبوبروفين عند مشاركتهما في دراسات تفاعل جرعة واحدة.
يرتبط الميتفورمين بالإهمال لبروتينات البلازما وبالتالي فهو أقل عرضة للتفاعل مع الأدوية شديدة الارتباط بالبروتين مثل الساليسيلات ، السلفوناميدات ، الكلورامفينيكول ، البروبينسيد ، بالمقارنة مع السلفونيل يوريا ، التي ترتبط على نطاق واسع بالمصل البروتينات.
أعلى
استخدام في السكان محددة
حمل
الحمل الفئة ب:
Janumet
لا توجد دراسات كافية ومضبوطة بشكل جيد في النساء الحوامل المصابات بجانوميت أو مكوناتها الفردية ؛ لذلك ، سلامة Janumet في النساء الحوامل ليست معروفة. يجب استخدام Janumet أثناء الحمل فقط إذا لزم الأمر بشكل واضح.
شركة ميرك وشركاه يحتفظ بسجل لمراقبة نتائج حمل النساء المعرضات لجانوميت أثناء الحمل. نشجع مقدمي الرعاية الصحية على الإبلاغ عن أي تعرض لما قبل الولادة لـ Janumet عن طريق الاتصال بسجل الحمل على (800) 986-8999.
لم تجر أي دراسات على الحيوانات مع المنتجات المدمجة في Janumet لتقييم التأثيرات على التكاثر. تستند البيانات التالية إلى النتائج التي توصلت إليها الدراسات التي أجريت باستخدام سيتاجليبتين أو ميتفورمين بشكل فردي.
سيتاقلبتين
تم إجراء دراسات التكاثر في الفئران والأرانب. جرعات سيتاغليبتين التي تصل إلى 125 مغ / كغ (حوالي 12 ضعف التعرض البشري بجرعة بشرية موصى بها القصوى) لم تضعف الخصوبة أو تضر الجنين. ومع ذلك ، لا توجد دراسات كافية ومضبوطة بشكل جيد مع سيتاجليبتين في النساء الحوامل.
لم يكن Sitagliptin المُعطى للجرذان والأرانب الحوامل من يوم الحمل من 6 إلى 20 (تكوين عضوي) ماسخ عند الجرعات الفموية التي تصل إلى 250 مغ / كغ (الفئران) و 125 ملغ / كغ (الأرانب) ، أو ما يقرب من 30 و 20 مرة من التعرض البشري في الجرعة القصوى البشرية الموصى بها (MRHD) من 100 ملغ / يوم على أساس AUC المقارنات. زادت الجرعات العالية من حدوث تشوهات الأضلاع في النسل عند 1000 ملغم / كغم ، أو ما يقرب من 100 ضعف التعرض البشري في MRHD.
قام سيتاجلبتين الذي تم إعطاؤه للفئران من يوم الحمل 6 إلى يوم الرضاعة 21 بتقليل وزن الجسم في ذرية الذكور والإناث عند 1000 ملغم / كغم. لم يلاحظ أي سمية وظيفية أو سلوكية في ذرية الفئران.
كان نقل المشيمة من سيتاجليبتين تدار إلى الفئران الحوامل حوالي 45 ٪ في 2 ساعة و 80 ٪ في 24 ساعة بعد جرعة. كان نقل المشيمة من سيتاجليبتين تدار إلى الأرانب الحوامل حوالي 66 ٪ في 2 ساعة و 30 ٪ في 24 ساعة.
الميتفورمين هيدروكلوريد
لم يكن الميتفورمين مسخًا في الفئران والأرانب بجرعات تصل إلى 600 مجم / كجم / يوم. ويمثل هذا تعرضًا لحوالي 2 و 6 أضعاف الجرعة اليومية الموصى بها من البشر والتي تبلغ 2،000 ملغ بناءً على مقارنات مساحة سطح الجسم للفئران والأرانب ، على التوالي. أظهر تحديد تركيزات الجنين حاجزًا مشيميًا جزئيًا للميتفورمين.
الأمهات المرضعات
لم تجر أي دراسات على الحيوانات المرضعة مع المكونات المشتركة لـ Janumet. في الدراسات التي أجريت مع المكونات الفردية ، يتم إفراز كل من سيتاجليبتين و ميتفورمين في حليب الفئران المرضعة. من غير المعروف ما إذا كان سيتاجليبتين يفرز في حليب الإنسان. نظرًا لإفراز العديد من الأدوية في اللبن البشري ، يجب توخي الحذر عند إعطاء Janumet لمرضعة.
استخدام الأطفال
لم تثبت سلامة وفعالية Janumet في مرضى الأطفال الذين تقل أعمارهم عن 18 عامًا.
استخدام المسنين
Janumet
نظرًا لأن الكلى سيتاجليبتين والميتفورمين يفرزان بشكل كبير من قبل الكلى ، ولأن الشيخوخة يمكن أن ترتبط بوظيفة الكلى المخفضة ، يجب استخدام جانوميت بحذر مع زيادة العمر. يجب توخي الحذر عند اختيار الجرعة ويجب أن تستند إلى مراقبة دقيقة ومنتظمة لوظيفة الكلى. [نرى المحاذير والإحتياطات; علم الصيدلة السريرية.]
سيتاقلبتين
من إجمالي عدد الموضوعات (N = 3884) في الدراسات السريرية للمرحلة الثانية والثالثة من سيتاجليبتين ، كان 725 مريض 65 سنة وأكثر ، في حين كان 61 مريضا 75 سنة وأكثر. لم يلاحظ أي فروق شاملة في السلامة أو الفعالية بين الموضوعات 65 سنة وما فوق والأصغر سنا. في حين أن هذه وغيرها من التجارب السريرية المبلغ عنها لم تحدد الاختلافات في الاستجابات بين كبار السن والمرضى الأصغر سنا ، لا يمكن أن تكون حساسية أكبر لبعض الأفراد الأكبر سنا استبعد.
الميتفورمين هيدروكلوريد
لم تتضمن الدراسات السريرية الخاضعة للرقابة من الميتفورمين أعدادًا كافية من المرضى المسنين لتحديد ما إذا كانوا يستجيبون بشكل مختلف من المرضى الأصغر سنا ، على الرغم من أن التجارب السريرية الأخرى التي تم الإبلاغ عنها لم تحدد الاختلافات في الاستجابات بين كبار السن والشباب المرضى. يجب استخدام الميتفورمين فقط في المرضى الذين يعانون من وظائف الكلى الطبيعية. يجب أن تكون الجرعات الأولية والصيانة للميتفورمين متحفظة في المرضى الذين يعانون من التقدم في السن ، وذلك بسبب احتمال انخفاض وظيفة الكلى في هذه الفئة من السكان. يجب أن يستند أي تعديل للجرعة إلى تقييم دقيق لوظيفة الكلى. [نرى موانع; المحاذير والإحتياطات; و علم الصيدلة السريرية.]
أعلى
جرعة مفرطة
سيتاقلبتين
خلال التجارب السريرية التي تسيطر عليها في الأشخاص الأصحاء ، كانت تدار جرعات واحدة تصل إلى 800 ملغ sitagliptin. لوحظت زيادات متوسطة قصوى في QTc تبلغ 8.0 ميللي ثانية في إحدى الدراسات بجرعة 800 ملغ من سيتاغليبتين ، وهو تأثير متوسط لا يعتبر مهمًا سريريًا [انظر علم الصيدلة السريرية]. لا توجد تجربة مع الجرعات فوق 800 ملغ في البشر. في دراسات المرحلة الأولى من الجرعات المتعددة ، لم تكن هناك ردود فعل سلبية سريرية مرتبطة بالجرعة لوحظت مع سيتاجليبتين بجرعات تصل إلى 400 ملغ يوميًا لفترات تصل إلى 28 يومًا.
في حالة تناول جرعة زائدة ، من المعقول استخدام التدابير الداعمة المعتادة ، على سبيل المثال ، إزالة المواد غير الممتصة من الجهاز الهضمي المسالك ، استخدم مراقبة سريرية (بما في ذلك الحصول على مخطط كهربية القلب) ، ومعهد علاج داعم كما هو مبين من قبل المريض السريري الحالة.
Sitagliptin هو قابل للغسل متواضعة. في الدراسات السريرية ، تمت إزالة حوالي 13.5 ٪ من الجرعة خلال جلسة غسيل الكلى من 3 إلى 4 ساعات. ويمكن اعتبار غسيل الكلى لفترات طويلة إذا كان ذلك مناسبا سريريا. لا يُعرف ما إذا كان سيتاجليبتين قابل للغسل عن طريق غسيل الكلى البريتوني.
الميتفورمين هيدروكلوريد
حدثت جرعة زائدة من هيدروكلوريد الميتفورمين ، بما في ذلك تناول كميات أكبر من 50 جرام. تم الإبلاغ عن نقص السكر في الدم في حوالي 10 ٪ من الحالات ، ولكن لم يتم تأسيس أي علاقة سببية مع هيدروكلوريد الميتفورمين. تم الإبلاغ عن الحماض اللبني في حوالي 32 ٪ من حالات جرعة زائدة من الميتفورمين [انظر المحاذير والإحتياطات]. الميتفورمين قابل للغسل مع إزالة تصل إلى 170 مل / دقيقة في ظل ظروف الدورة الدموية جيدة. لذلك ، قد يكون غسيل الكلى مفيدًا لإزالة الدواء المتراكم من المرضى الذين يشتبه في وجود جرعة زائدة من الميتفورمين.
أعلى
وصف
تحتوي أقراص جانوميت (سيتاجليبتين / ميتفورمين حمض الهيدروكلوريك) على عقاقير مضادة لفرط سكر الدم عن طريق الفم تستخدم في إدارة مرض السكري من النوع 2: سيتاجليبتين و هيدروكلوريد الميتفورمين.
سيتاقلبتين
Sitagliptin هو المانع نشط عن طريق الفم من انزيم ديبيبتيديل ببتيداز - 4 (DPP-4). سيتاغليبتين موجود في أقراص جانوميت في شكل سيتوهليبتين فوسفات مونوهيدرات. يوصف سيتاجليبتين فوسفات مونوهيدرات كيميائيا بأنه 7 - [(3R) - 3 - أميني - 1 - أوكسو - 4 - (2،4،5 - ثلاثي فلورو فينيل) بوتيل] - 5،6،7،8 - رباعي هيدرو - 3 - (ثلاثي فلورو ميثيل) - 1،2،4 - تريازولو [4،3 - أ] فوسفات بيرازين (1: 1) مونوهيدرات مع صيغة تجريبية من جيم16H15F6ن5يا3PO4-H2ووزنها الجزيئي 523.32. الصيغة الهيكلية هي:
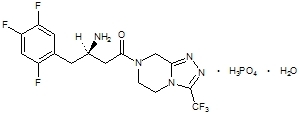
سيتاجليبتين فوسفات أحادي الهيدرات مسحوق أبيض إلى أبيض ، بلوري ، غير رطب. قابل للذوبان في الماء و N ، ثنائي ميثيل فورميميد. قابل للذوبان قليلاً في الميثانول ؛ قابل للذوبان قليلاً في الإيثانول والأسيتون والأسيتونيتريل ؛ وغير قابلة للذوبان في الآيزوبروبانول وخلات الأيزوبروبيل.
الميتفورمين هيدروكلوريد
لا يرتبط هيدروكلوريد الميتفورمين (N ، ثنائي ميثيل ثنائي كربون ثنائي أميد هيدروكلوريد) كيميائيًا أو صيدلانيًا بأي فئات أخرى من عوامل فرط سكر الدم عن طريق الفم. ميتفورمين هيدروكلوريد مركب بلوري أبيض إلى أبيض مع تركيبة جزيئية من C4H11ن5-HCl ويبلغ الوزن الجزيئي 165.63. هيدروكلوريد الميتفورمين قابل للذوبان في الماء بحرية وهو غير قابل للذوبان عملياً في الأسيتون والأثير وكلوروفورم. pkأ الميتفورمين هو 12.4. الرقم الهيدروجيني لمحلول مائي 1 ٪ من هيدروكلوريد الميتفورمين هو 6.68. الصيغة الهيكلية كما هو موضح:
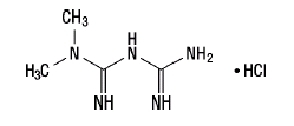
Janumet
Janumet متاح للإعطاء عن طريق الفم كأقراص تحتوي على 64.25 ملغ من فوسفات سيتاجليبتين أحادي الهيدرات وما يعادل الميتفورمين هيدروكلوريد إلى: 50 ملغ سيتاجليبتين كقاعدة حرة و 500 ملغ هيدروكلوريد الميتفورمين (جانوميت 50 ملغ / 500 ملغ) أو 1000 ملغ هيدروكلوريد الميتفورمين (جانوميت 50 ملغ / 1000 ملغ). يحتوي كل قرص من أقراص Janumet المغلفة بالأفلام على المكونات غير النشطة التالية: السليلوز الجريزوفولفين ، البولي فينيل بيروليدون ، سلفات لوريل الصوديوم ، وفومارات ستيرل الصوديوم. بالإضافة إلى ذلك ، يحتوي طلاء الفيلم على المكونات غير النشطة التالية: كحول البولي فينيل ، بولي إيثيلين جليكول ، التلك ، ثاني أكسيد التيتانيوم ، أكسيد الحديد الأحمر ، وأكسيد الحديد الأسود.
أعلى
علم الصيدلة السريرية
آلية العمل
Janumet
Janumet يجمع بين اثنين من وكلاء ارتفاع السكر في الدم مع آليات تكميلية للعمل لتحسين السيطرة على نسبة السكر في الدم في المرضى الذين يعانون من داء السكري من النوع 2: سيتاجليبتين ، مثبط ديبيبتيديل ببتيداز -4 (DPP-4) ، وميتفورمين هيدروكلوريد ، عضو في بيغوانيد صف دراسي.
سيتاقلبتين
Sitagliptin هو مثبط DPP-4 ، والذي يعتقد أنه يمارس أفعاله في المرضى الذين يعانون من مرض السكري من النوع 2 عن طريق إبطاء تعطيل هرمونات incretin. يتم زيادة تركيز هرمونات سليمة نشطة عن طريق سيتاجليبتين ، وبالتالي زيادة وإطالة عمل هذه الهرمونات. هرمونات إنكريتين ، بما في ذلك الببتيد -1 (GLP-1) المشابه للجلوكاجون والانسولين المؤثر على الجلوكوز يتم الإفراج عن polypeptide (GIP) بواسطة الأمعاء طوال اليوم ، ويتم زيادة مستويات الاستجابة لتناول وجبة. يتم تعطيل هذه الهرمونات بسرعة بواسطة الإنزيم DPP-4. و incretins هي جزء من نظام داخلي تشارك في التنظيم الفسيولوجي للتوازن الجلوكوز. عندما تكون تركيزات الجلوكوز في الدم طبيعية أو مرتفعة ، فإن GLP-1 و GIP يزيدان من تخليق الأنسولين ويطلقان من خلايا بيتا البنكرياس عن طريق مسارات إشارات داخل الخلايا تتضمن AMP دوري. GLP-1 يقلل من إفراز الجلوكاجون من خلايا ألفا البنكرياس ، مما يؤدي إلى انخفاض إنتاج الجلوكوز الكبدي. عن طريق زيادة وإطالة مستويات incretin النشطة ، فإن سيتاجليبتين يزيد من إفراز الأنسولين ويقلل مستويات الجلوكاجون في الدورة الدموية بطريقة تعتمد على الجلوكوز. يوضح Sitagliptin الانتقائية لـ DPP-4 ولا يمنع نشاط DPP-8 أو DPP-9 في المختبر بتركيزات تقارب تلك الناتجة عن الجرعات العلاجية.
الميتفورمين هيدروكلوريد
الميتفورمين هو عامل مضاد لفرط سكر الدم يحسن تحمل الجلوكوز لدى مرضى السكري من النوع 2 ، مما يقلل من الجلوكوز في البلازما القاعدية وما بعد الأكل. آلياتها الدوائية للعمل تختلف عن فئات أخرى من وكلاء ارتفاع السكر في الدم عن طريق الفم. يقلل الميتفورمين من إنتاج الجلوكوز الكبدي ، ويقلل من امتصاص الجلوكوز في الأمعاء ، ويحسن حساسية الأنسولين عن طريق زيادة امتصاص الجلوكوز المحيطي واستخدامه. على عكس السلفونيل يوريا ، لا ينتج الميتفورمين نقص سكر الدم في أي من مرضى السكري من النوع 2 أو الأشخاص الطبيعيين (باستثناء الحالات الخاصة [انظر المحاذير والإحتياطات]) ولا يسبب فرط الأنسولين. مع العلاج بالميتفورمين ، يظل إفراز الأنسولين دون تغيير بينما قد تنخفض بالفعل مستويات الأنسولين في الصيام واستجابة الأنسولين للبلازما طوال اليوم.
12.2 الديناميكا الدوائية
سيتاقلبتين
جنرال لواء
في المرضى الذين يعانون من مرض السكري من النوع 2 ، أدت إدارة سيتاجليبتين إلى تثبيط نشاط إنزيم DPP-4 لمدة 24 ساعة. بعد حمل الجلوكوز عن طريق الفم أو الوجبة ، نتج عن تثبيط DPP-4 هذا زيادة في مستويات تعميم GLP-1 و GIP النشط بمقدار 2 إلى 3 أضعاف ، انخفاض تركيزات الجلوكاجون ، وزيادة استجابة إطلاق الأنسولين للجلوكوز ، مما أدى إلى ارتفاع الببتيد C والأنسولين التركيزات. ارتبط ارتفاع الأنسولين مع انخفاض نسبة الجلوكاجون بتركيزات منخفضة من الجلوكوز في الصيام وتقليل رحلة الجلوكوز بعد تناول الجلوكوز عن طريق الفم أو تناول وجبة.
Sitagliptin و Metformin هيدروكلوريد الإدارة المشتركة
في دراسة استمرت يومين في موضوعات صحية ، زاد سيتاجليبتين وحده من تركيزات GLP-1 النشطة ، بينما زاد الميتفورمين وحده من تركيزات GLP-1 النشطة والإجمالية إلى نطاقات مماثلة. كان للإدارة المشاركة للستاجليبتين والميتفورمين تأثير إضافي على تركيزات GLP-1 النشطة. Sitagliptin ، ولكن ليس الميتفورمين ، وزيادة تركيزات GIP النشطة. ليس من الواضح ماذا تعني هذه النتائج بالنسبة للتغيرات في السيطرة على نسبة السكر في الدم لدى مرضى السكري من النوع 2.
في الدراسات التي أجريت على الأشخاص الأصحاء ، لم يقلل سيتاجلبتين من نسبة الجلوكوز في الدم أو يسبب نقص السكر في الدم.
الفيزيولوجيا الكهربية للقلب
في دراسة كروس عشوائية ، خاضعة للتحكم الوهمي ، تم إعطاء 79 شخصًا صحيًا جرعة واحدة عن طريق الفم من سيتاجليبتين 100 ملغ ، سيتاجليبتين 800 ملغ (8 أضعاف الجرعة الموصى بها) ، وهمي. في الجرعة الموصى بها من 100 ملغ ، لم يكن هناك أي تأثير على الفاصل الزمني QTc التي تم الحصول عليها في تركيز البلازما الذروة ، أو في أي وقت آخر أثناء الدراسة. بعد جرعة 800 ملغ ، كانت الزيادة القصوى في تغيير الوسيلة التي تم تصحيحها في الغفل في QTc من خط الأساس عند 3 ساعات من جرعة ما بعد الجرعة 8.0 ميللي ثانية. لا تعتبر هذه الزيادة ذات أهمية سريرية. في جرعة 800 ملغ ، كانت تركيزات البلازما sitagliptin الذروة أعلى بنحو 11 مرة من تركيزات الذروة بعد جرعة 100 ملغ.
في المرضى الذين يعانون من داء السكري من النوع 2 يدار سيتاجلبتين 100 ملغ (N = 81) أو سيتاجلبتين 200 ملغ (N = 63) يوميًا ، هناك لم تكن هناك تغييرات ذات مغزى في QTc الفاصل بناء على بيانات ECG التي تم الحصول عليها في وقت ذروة البلازما المتوقعة تركيز.
الدوائية
Janumet
أظهرت نتائج دراسة التكافؤ الحيوي في الأشخاص الأصحاء أن جانوميت (سيتاجليبتين / ميتفورمين حمض الهيدروكلوريك) 50 ملغ / 500 ملغ و 50 ملغ / 1000 ملغ من أقراص مجموعة مكافئة بيولوجيا للإدارة المشتركة للجرعات المقابلة من سيتاجلبتين (JANUVIA™2) وهيدروكلوريد الميتفورمين كأقراص فردية.
استيعاب
سيتاقلبتين
التوافر الحيوي المطلق لسيتاجليبتين هو حوالي 87 ٪. شارك في تناول وجبة غنية بالدهون مع سيتاجليبتين لم يكن له تأثير على الحرائك الدوائية لسيتاجليبتين.
الميتفورمين هيدروكلوريد
يبلغ التوافر البيولوجي المطلق للقرص 500 ملغ من هيدروكلوريد الميتفورمين المعطى في ظروف الصيام حوالي 50-60 ٪. تشير الدراسات التي استخدمت جرعات فموية واحدة من أقراص هيدروكلوريد الميتفورمين من 500 إلى 1500 ملغ ، ومن 850 إلى 2550 ملغ ، إلى أن هناك قلة الجرعة التناسبية مع زيادة الجرعات ، وهذا بسبب انخفاض الامتصاص بدلاً من التغيير في التخلص منه. يقلل الطعام من مستوى امتصاص الميتفورمين ويؤخر قليلاً ، كما يتضح من متوسط تركيز البلازما الذروة بنسبة 40٪ تقريبًا (Cماكس) ، مساحة أقل بنسبة 25 ٪ تحت تركيز البلازما مقابل منحنى الوقت (AUC) ، وإطالة 35 دقيقة من الوقت إلى ذروة تركيز البلازما (Tماكس) بعد تناول قرص واحد من 850 ملغ من الميتفورمين مع الطعام ، مقارنةً بنفس القوة التي يتناولها الصيام. أهمية السريرية لهذه النقصات غير معروف.
توزيع
سيتاقلبتين
متوسط حجم التوزيع في حالة مستقرة بعد جرعة واحدة 100 ملغ من الوريد من سيتاجليبتين إلى الأشخاص الأصحاء حوالي 198 لتر. جزء من سيتاجليبتين ملزمة عكسيا لبروتينات البلازما منخفضة (38 ٪).
الميتفورمين هيدروكلوريد
بلغ الحجم الظاهري لتوزيع (V / F) من الميتفورمين بعد الجرعات الفردية عن طريق الفم من أقراص الميتفورمين هيدروكلوريد 850 ملغ متوسط 654 ± 358 لتر. يرتبط الميتفورمين بالإهمال لبروتينات البلازما ، على عكس السلفونيل يوريا ، التي ترتبط بأكثر من 90٪ من البروتين. أقسام الميتفورمين إلى كريات الدم الحمراء ، على الأرجح كدالة للوقت. في الجرعات السريرية المعتادة وجداول الجرعات من أقراص هيدروكلوريد الميتفورمين ، يتم الوصول إلى تركيزات بلازما الحالة الثابتة للميتفورمين في غضون 24-48 ساعة وعادة ما تكون
التمثيل الغذائي
سيتاقلبتين
ما يقرب من 79 ٪ من سيتاجليبتين يفرز دون تغيير في البول مع الأيض كونه طريقا صغيرا للقضاء.
بعد [14C] جرعة الفم عن طريق الفم sitagliptin ، ما يقرب من 16 ٪ من النشاط الإشعاعي تفرز كما الأيض من sitagliptin. تم الكشف عن ستة نواتج أيضية عند مستويات التتبع ، وليس من المتوقع أن تساهم في نشاط تثبيط البلازما DPP-4 لل سيتاجليبتين. في الدراسات المختبرية أشارت إلى أن الإنزيم الرئيسي المسؤول عن التمثيل الغذائي المحدود لسيتاجليبتين هو CYP3A4 ، بمساهمة من CYP2C8.
الميتفورمين هيدروكلوريد
أظهرت الدراسات التي أجريت على جرعة واحدة عن طريق الوريد في المواد الطبيعية أن الميتفورمين يفرز دون تغيير في البول ولا يخضع لعملية الأيض الكبدي (لم يتم تحديد أي مستقلبات عند البشر) أو الصفراوي إفراز.
إفراز
سيتاقلبتين
بعد تناوله عن طريق الفم [14C] جرعة سيتاجليبتين إلى الأشخاص الأصحاء ، تم التخلص من حوالي 100 ٪ من النشاط الإشعاعي المدار في البراز (13 ٪) أو البول (87 ٪) في غضون أسبوع واحد من الجرعات. محطة ر واضحة1/2 بعد جرعة عن طريق الفم 100 ملغ من سيتاجليبتين كان حوالي 12.4 ساعة ، وكانت إزالة الكلى حوالي 350 مل / دقيقة.
يحدث القضاء على سيتاجليبتين بشكل أساسي عبر إفراز كلوي وينطوي على إفراز أنبوبي نشط. Sitagliptin هو الركيزة لنقل الأنيون العضوية البشرية 3 (hOAT-3) ، والتي قد تشارك في القضاء على سيتاجليبتين. لم يتم إثبات الصلة السريرية لـ hOAT-3 في نقل سيتاغليبتين. Sitagliptin هو أيضا الركيزة من بروتين سكري البروتين ، والتي قد تشارك أيضا في التوسط في القضاء على الكلوي من سيتاجليبتين. ومع ذلك ، لم يقلل السيكلوسبورين ، وهو مثبط بروتين سكري البروتين ، من الخلوص الكلوي لسيتاجليبتين.
الميتفورمين هيدروكلوريد
الخلوص الكلوي أكبر بنحو 3.5 مرة من خلوص الكرياتينين ، مما يشير إلى أن إفراز أنبوبي هو الطريق الرئيسي للتخلص من الميتفورمين. بعد تناوله عن طريق الفم ، يتم التخلص من حوالي 90 ٪ من المخدرات الممتصة عبر الطريق الكلوي خلال ال 24 ساعة الأولى ، مع عمر النصف للتخلص من البلازما حوالي 6.2 ساعة. في الدم ، يكون نصف عمر التخلص حوالي 17.6 ساعة ، مما يشير إلى أن كتلة كريات الدم الحمراء قد تكون مقصورة للتوزيع.
السكان الخاصة
قصور كلوي
Janumet
لا ينبغي أن تستخدم Janumet في المرضى الذين يعانون من قصور كلوي [انظر موانع; المحاذير والإحتياطات].
سيتاقلبتين
وقد لوحظت زيادة تقريبًا بمقدار 2 أضعاف في البلازما AUC من سيتاجليبتين في المرضى الذين يعانون من قصور كلوي معتدل ، وحوالي 4 أضعاف لوحظت زيادة في المرضى الذين يعانون من قصور كلوي حاد بما في ذلك المرضى الذين يعانون من ESRD على غسيل الكلى ، بالمقارنة مع السيطرة الصحية الطبيعية المواضيع.
الميتفورمين هيدروكلوريد
في المرضى الذين يعانون من انخفاض وظائف الكلى (على أساس تصفية الكرياتينين المقاسة) ، فإن عمر النصف للبلازما والدم يطول الميتفورمين وينخفض خلوص الكلى بما يتناسب مع النقص في الكرياتينين تخليص.
قصور كبدي
سيتاقلبتين
في المرضى الذين يعانون من القصور الكبدي المعتدل (درجة الأطفال من 7 إلى 9) ، يعني AUC و Cماكس من سيتاجليبتين زاد حوالي 21 ٪ و 13 ٪ ، على التوالي ، مقارنة مع الضوابط صحية مطابقة بعد إعطاء جرعة واحدة 100 ملغ من سيتاجليبتين. لا تعتبر هذه الاختلافات ذات مغزى سريريًا.
لا توجد تجربة سريرية في المرضى الذين يعانون من قصور كبدي حاد (درجة تشابك الأطفال> 9).
الميتفورمين هيدروكلوريد
لم تجر أي دراسات الدوائية للميتفورمين في المرضى الذين يعانون من قصور كبدي.
جنس
سيتاقلبتين
لم يكن للجنس أي تأثير ذي معنى سريريًا على الحرائك الدوائية للستاجليبتين على أساس مركب تحليل بيانات الحركية الدوائية للمرحلة الأولى وعلى تحليل الحرائك الدوائية للسكان للمرحلة الأولى والمرحلة الثانية البيانات.
الميتفورمين هيدروكلوريد
لم المعلمات الدوائية الميتفورمين لا تختلف اختلافا كبيرا بين الأشخاص الطبيعيين والمرضى الذين يعانون من مرض السكري من النوع 2 عند تحليلها وفقا لنوع الجنس. وبالمثل ، في الدراسات السريرية الخاضعة للرقابة في المرضى الذين يعانون من مرض السكري من النوع 2 ، كان تأثير ارتفاع السكر في الدم للميتفورمين قابلاً للمقارنة في الذكور والإناث.
الشيخوخة
سيتاقلبتين
عندما تؤخذ آثار العمر على وظيفة الكلى في الاعتبار ، لم يكن العمر وحده سريريًا تأثير ذو مغزى على الحرائك الدوائية للستاجليبتين على أساس الحرائك الدوائية للسكان تحليل. كان لدى كبار السن (من 65 إلى 80 عامًا) تركيزات البلازما أعلى بنسبة 19٪ تقريبًا من سيتاجليبتين مقارنة بالمواد الأصغر سناً.
الميتفورمين هيدروكلوريد
تشير البيانات المحدودة من الدراسات الدوائية المتحكم بها للميتفورمين في الأشخاص المسنين الأصحاء إلى انخفاض الخلوص الكلي للبلازما للميتفورمين ، وطول عمر النصف ، و Cماكس يتم زيادة ، مقارنة مع الموضوعات الشباب الأصحاء. من هذه البيانات ، يبدو أن التغير في الحرائك الدوائية للميتفورمين مع التقدم في السن يعزى في المقام الأول إلى التغيير في وظيفة الكلى (انظر GLUCOPHAGE3 وصف المعلومات: صيدلية سريرية، السكان الخاصة ، أمراض الشيخوخة).
لا ينبغي أن يبدأ علاج جانوميت في المرضى الذين تتراوح أعمارهم بين 80 عامًا ما لم يثبت قياس خلوص الكرياتينين أن وظيفة الكلى لا تقل [انظر المحاذير والإحتياطات].
اخصائي اطفال
لم يتم إجراء أي دراسات مع Janumet في مرضى الأطفال.
سباق
سيتاقلبتين
لم يكن للسباق أي تأثير ذي معنى سريريًا على الحرائك الدوائية للستاجليبتين استنادًا إلى تحليل مركب من البيانات الدوائية المتاحة ، بما في ذلك مواضيع بيضاء ، من أصل اسباني ، أسود ، آسيوي ، وغيرها من العنصري مجموعات.
الميتفورمين هيدروكلوريد
لم يتم إجراء أية دراسات على المعلمات الدوائية للميتفورمين وفقًا للسباق. في الدراسات السريرية الخاضعة للرقابة من الميتفورمين في مرضى السكري من النوع 2 ، كان تأثير ارتفاع السكر في الدم قابل للمقارنة في البيض (ن = 249) ، والسود (ن = 51) ، واللاتينيون (ن = 24).
مؤشر كتلة الجسم (BMI)
سيتاقلبتين
لم يكن لمؤشر كتلة الجسم أي تأثير ذي معنى سريريًا على الحرائك الدوائية للستاجليبتين استنادًا إلى مركب تحليل بيانات الحركية الدوائية للمرحلة الأولى وعلى تحليل الحرائك الدوائية للسكان للمرحلة الأولى والمرحلة الثانية البيانات.
تفاعل الأدوية
Sitagliptin و Metformin هيدروكلوريد
شارك في إعطاء جرعات متعددة من سيتاجلبتين (50 ملغ) وميتفورمين (1000 ملغ) تعطى مرتين يوميًا لا يغير بشكل صحيح الدوائية إما سيتاجليبتين أو ميتفورمين في المرضى الذين يعانون من النوع 2 داء السكري.
لم يتم إجراء دراسات التفاعل الدوائي الدوائي مع Janumet ؛ ومع ذلك ، فقد أجريت مثل هذه الدراسات مع المكونات الفردية لل Janumet (سيتاجليبتين وهيدروكلوريد الميتفورمين).
سيتاقلبتين
في المختبر تقييم التفاعلات المخدرات
Sitagliptin ليس مثبطًا لأنزيمات CYP CYP3A4 أو 2C8 أو 2C9 أو 2D6 أو 1A2 أو 2C19 أو 2B6 ، وليس محفزًا لـ CYP3A4. Sitagliptin هو الركيزة بروتين سكري البروتين ، لكنه لا يمنع نقل بروتين سكري البروتين من الديجوكسين. بناءً على هذه النتائج ، من غير المرجح أن يسبب سيتاجليبتين تفاعلات مع أدوية أخرى تستخدم هذه المسارات.
Sitagliptin ليس مرتبطا على نطاق واسع ببروتينات البلازما. لذلك ، فإن ميل سيتاجليبتين إلى المشاركة في تفاعلات المخدرات المخدرات ذات مغزى سريري بوساطة النزوح ملزمة بروتين البلازما منخفضة جدا.
في الجسم الحي تقييم التفاعلات المخدرات
تأثير Sitagliptin على المخدرات الأخرى
في الدراسات السريرية ، كما هو موصوف أدناه ، لم يغير سيتاجلبتين دواءًا فعالًا في الميتفورمين أو الغليبيريد أو سيمفاستاتين أو روسيجليتازون أو الوارفارين أو الفم. موانع الحمل ، التي توفر دليلًا حيويًا على انخفاض الميل للتسبب في تفاعلات دوائية مع ركائز CYP3A4 و CYP2C8 و CYP2C9 وناقل كاتيوني عضوي (OCT).
الديجوكسين: كان لسيتاغليتين تأثير بسيط على الحرائك الدوائية للديجوكسين. بعد إعطاء 0.25 ملغ من الديجوكسين بالتزامن مع 100 ملغ من سيتاغليبتين يوميًا لمدة 10 أيام ، زادت البلازما AUC من الديجوكسين بنسبة 11٪ ، والبلازما Cماكس بنسبة 18 ٪.
السلفونيل يوريا: لم يتم تغييرها بشكل صحيح في الدوائية جرعة واحدة من الجليكوريد ، وهي ركيزة CYP2C9 ، في الموضوعات التي تتلقى جرعات متعددة من سيتاجليبتين. لن يكون من المتوقع حدوث تفاعلات ذات مغزى سريريًا مع السلفونيل يوريا الأخرى (مثل glipizide ، tolbutamide ، و glimepiride) والتي ، مثل glyburide ، يتم التخلص منها بشكل أساسي بواسطة CYP2C9 [انظر المحاذير والإحتياطات].
سيمفاستاتين: لم يتم تغيير الدوائية أحادية الجرعة من سيمفاستاتين ، وهي ركيزة CYP3A4 ، بشكل مفيد في الأشخاص الذين يتلقون جرعات يومية متعددة من سيتاغليبتين. لذلك ، سيتاغليبتين ليس مثبطًا لعملية التمثيل الغذائي باستخدام CYP3A4.
ثيازوليدينيديون: الدوائية جرعة واحدة من روزيجليتازون لم يتغير معنى في المواضيع تلقي جرعات يومية متعددة من سيتاغليبتين ، مما يشير إلى أن سيتاجليبتين ليس مثبطًا للتوسط في CYP2C8 التمثيل الغذائي.
الوارفارين: جرعات يومية متعددة من سيتاغليبتين لم تغير الحركية الدوائية ، كما تم تقييمها من خلال قياس S (-) أو R (+) enantiomers الوارفارين ، أو الديناميكا الدوائية (كما تم تقييمها عن طريق قياس البروثرومبين INR) من جرعة واحدة من الوارفارين. نظرًا لأنه يتم استقلاب الوارفارين S (-) بشكل أساسي بواسطة CYP2C9 ، فإن هذه البيانات تدعم أيضًا الاستنتاج القائل بأن سيتاجليبتين ليس مثبطًا CYP2C9.
موانع الحمل الفموية: لم يغير المشاركة في تناول الدواء مع سيتاجليبتين دواءًا فعالًا للحرائك الدوائية للحالة المستقرة للنوريثيندرون أو إيثينيل استراديول.
تأثير أدوية أخرى على سيتاجلبتين
تشير البيانات السريرية الموضحة أدناه إلى أن سيتاجليبتين ليس عرضة لتفاعلات ذات مغزى سريريًا من خلال الأدوية التي تتم إدارتها بشكل مشترك.
السيكلوسبورين: أجريت دراسة لتقييم تأثير السيكلوسبورين ، وهو مثبط قوي للبروتين الدهني ، على دواء سيتاكليبتين الدوائي. شارك في إعطاء جرعة واحدة 100 ملغ من الفم من سيتاغليبتين وجرعة عن طريق الفم واحدة من 600 ملغ من السيكلوسبورين مما زاد من AUC و Cماكس من sitagliptin بنحو 29 ٪ و 68 ٪ ، على التوالي. هذه التغييرات المتواضعة في دواء سيتاجليبتين لم تعتبر مفيدة سريريًا. كما أن الخلوص الكلوي لسيتاجليبتين لم يتغير بشكل كبير. لذلك ، لن يكون من المتوقع حدوث تفاعلات ذات معنى مع مثبطات بروتين سكري أخر.
الميتفورمين هيدروكلوريد
[نرى تفاعل الأدوية]
أعلى
علم السموم غير الإكلينيكي
التسرطن ، والطفرات ، وضعف الخصوبة
Janumet
لم تجر أي دراسات حيوانية مع المنتجات المدمجة في Janumet لتقييم التسرطن أو الطفرات أو ضعف الخصوبة. تستند البيانات التالية إلى النتائج التي توصلت إليها الدراسات مع سيتاجليبتين وميتفورمين على حدة.
سيتاقلبتين
أجريت دراسة لمدة عامين على تسرطن في فئران ذكور وإناث تعطى جرعات عن طريق الفم من سيتاجليبتين من 50 ، 150 ، و 500 ملغم / كغم / يوم. كانت هناك زيادة في حدوث ورم غدي كبد / سرطان في الذكور والإناث وسرطان كبد في الإناث عند 500 ملغ / كغ. ينتج عن هذه الجرعة تعرض ما يقرب من 60 ضعف التعرض البشري عند الحد الأقصى الموصى به من الجرعة اليومية للبالغين (MRHD) البالغ 100 ملغ / يوم بناءً على مقارنات AUC. لم يتم ملاحظة أورام الكبد عند 150 مغ / كغ ، أي ما يقرب من 20 مرة من التعرض البشري في MRHD. أجريت دراسة سرطانية مدتها سنتان على فئران ذكور وإناث مُعطاة جرعات فموية من سيتاجليبتين من 50 ، 125 ، 250 ، و 500 ملغم / كغم / يوم. لم يكن هناك زيادة في حدوث الأورام في أي عضو يصل إلى 500 ملغ / كغ ، ما يقرب من 70 مرة تعرض الإنسان في MRHD. لم يكن Sitagliptin مُطفّرًا أو مُمْرِضًا مع أو بدون التنشيط الأيضي في مقايسة طفرات البكتيريا Ames ، وهو مبيض الهامستر الصيني (CHO) فحص انحراف الكروموسوم ، مقايسة الوراثة الخلوية المختبرية في CHO ، ومقايسة شطف الحمض النووي القلوية DNA المختبرية في الجرذان المختبرية ، ونواة الخلايا المجهرية في الجسم الحي فحص.
في دراسات خصوبة الفئران التي تناولت جرعات عن طريق الفم من 125 و 250 و 1000 ملغم / كغم ، عولج الذكور لمدة 4 أسابيع قبل التزاوج ، خلال التزاوج ، حتى الإنهاء المقرر (حوالي 8 أسابيع تقريبًا) ، وتمت معالجة الإناث قبل أسبوعين من التزاوج من خلال الحمل اليوم 7. لم يلاحظ أي تأثير سلبي على الخصوبة عند 125 ملغ / كغ (حوالي 12 مرة من التعرض البشري في MRHD من 100 ملغ / يوم على أساس مقارنات AUC). في الجرعات الأعلى ، لوحظت ارتشافات متزايدة مرتبطة بالنوندوز في الإناث (حوالي 25 و 100 مرة تعرض الإنسان في MRHD على أساس مقارنة AUC).
الميتفورمين هيدروكلوريد
أجريت دراسات مسرطنة طويلة المدى على الفئران (مدة الجرعات 104 أسابيع) والفئران (مدة الجرعات 91 أسبوعًا) بجرعات تصل إلى 900 مجم / كجم / يوم و 1500 مجم / كجم / يوم ، على التوالي. هذه الجرعات على حد سواء أربعة أضعاف تقريبا الجرعة اليومية الموصى بها الإنسان من 2000 ملغ على أساس مقارنات مساحة سطح الجسم. لم يتم العثور على أي دليل على حدوث التسرطن بالميتفورمين في الفئران الذكورية أو الأنثوية. وبالمثل ، لم يكن هناك احتمال وجود ورم مع الميتفورمين في الفئران الذكور. ومع ذلك ، كانت هناك زيادة في حدوث الاورام الحميدة الرحمية الحميدة في الفئران الإناث التي عولجت بـ 900 ملغم / كغم / يوم.
لم يكن هناك أي دليل على وجود احتمال للطفيل الميتفورمين في الاختبارات التالية في المختبر: Ames test (S. التيفيموريوم) ، اختبار طفرة الجينات (خلايا سرطان الغدد الليمفاوية الماوس) ، أو اختبار انحرافات الكروموسومات (الخلايا اللمفاوية البشرية). وكانت النتائج في اختبار النواة المجهرية للماوس سلبية أيضا. لم تتأثر خصوبة الفئران من الذكور أو الإناث بالميتفورمين عند تناوله بجرعات تصل إلى 600 ملغم / كغم / يوم ، وهو ما يقرب من ثلاثة أضعاف الحد الأقصى الموصى به الجرعة اليومية البشرية على أساس مساحة سطح الجسم المقارنات.
أعلى
الدراسات السريرية
تمت دراسة التناول المشترك للستاغليبتين والميتفورمين في مرضى السكري من النوع 2 الذين لا يتحكمون بشكل كافٍ في النظام الغذائي والتمارين الرياضية وبالاقتران مع غليميبيريد.
لم تكن هناك دراسات فعالية سريرية أجريت مع Janumet. ومع ذلك ، فقد تم إثبات التكافؤ الحيوي لـ Janumet مع أقراص سيتاجليبتين المشمولة بالإدارة المشتركة وهيدروكلوريد الميتفورمين.
سيتاجلبتين و ميتفورمين الإدارة المشتركة في المرضى الذين يعانون من مرض السكري من النوع 2 تسيطر بشكل غير كاف على النظام الغذائي وممارسة
شارك ما مجموعه 1091 مريضًا يعانون من مرض السكري من النوع 2 وعدم كفاية التحكم في نسبة السكر في الدم في النظام الغذائي وممارسة التمارين الرياضية على مدار 24 أسبوعًا ، دراسة عشوائية ، مزدوجة التعمية ، وهمي تسيطر عليها وهمي تهدف إلى تقييم فعالية سيتاجليبتين والميتفورمين شارك في الإدارة. خضع المرضى الذين يعانون من عامل ارتفاع السكر في الدم (ن = 541) لنظام غذائي وممارسة وفترة غسل الدواء لمدة تصل إلى 12 أسبوعًا. بعد فترة الغسيل ، تم اختيارهم بصورة عشوائية المرضى الذين يعانون من نقص السكر في الدم السيطرة (A1C 7.5 ٪ إلى 11 ٪) بعد الانتهاء من فترة التشغيل الوهمي المفرد لمدة أسبوعين. المرضى الذين لا يتناولون فرط سكر الدم عند دخول الدراسة (N = 550) مع التحكم غير الكافي في نسبة السكر في الدم (A1C 7.5 ٪ إلى 11 ٪) دخلت على الفور في فترة التشغيل الوهمي المفرد لمدة أسبوعين ، ثم كانت العشوائية. تم اختيارهم بصورة عشوائية ما يقرب من أعداد متساوية من المرضى لتلقي العلاج الوهمي ، 100 ملغ من سيتاجليبتين مرة واحدة يوميا ، 500 ملغ أو 1000 ملغ من الميتفورمين مرتين يوميًا أو 50 ملغ من سيتاجليبتين مرتين يوميًا مع 500 ملغ أو 1000 ملغ من الميتفورمين مرتين اليومي. تم علاج المرضى الذين فشلوا في تحقيق أهداف نسبة السكر في الدم أثناء الدراسة مع glyburide (glibenclamide) الإنقاذ.
قدمت سيتاجليبتين والميتفورمين الإدارة المشتركة تحسينات كبيرة في A1C ، FPG ، و PPG 2 ساعة مقارنة مع الدواء الوهمي ، والميتفورمين وحده ، و sitagliptin وحده (الجدول 3 ، الشكل 1). كانت التخفيضات المتوسطة من خط الأساس في A1C أكبر بشكل عام للمرضى الذين يعانون من ارتفاع قيم A1C الأساسية. بالنسبة للمرضى الذين ليسوا على عامل مضاد لخفض سكر الدم عند الدخول في الدراسة ، فإن التخفيضات من خط الأساس في A1C كانت: sitagliptin 100 mg مرة واحدة يوميًا ، -1.1٪ ؛ الميتفورمين 500 ملغ محاولة ، -1.1 ٪ ؛ الميتفورمين 1000 ملغ محاولة ، -1.2 ٪ ؛ sitagliptin 50 mg bid with metformin 500 mg bid، -1.6٪؛ sitagliptin 50 mg bid with metformin 1000 mg bid، -1.9٪؛ وللمرضى الذين يتلقون العلاج الوهمي ، -0.2 ٪. وكانت آثار الدهون محايدة عموما. كان انخفاض وزن الجسم في المجموعات المعطاة لسيتاجليبتين مع الميتفورمين مماثلاً لتلك الموجودة في المجموعات التي أعطيت الميتفورمين وحده أو الغفل.
الجدول 3: معلمات نسبة السكر في الدم في الزيارة النهائية (دراسة لمدة 24 أسبوعًا) ل Sitagliptin و Metformin ، بمفردها وفي مجموعة من المرضى الذين يعانون من داء السكري من النوع 2 يتم التحكم فيه بشكل غير كافٍ في النظام الغذائي والتمارين الرياضية *
الوهمي |
سيتاقلبتين 100 ملغ |
ميتفورمين 500 ملغ محاولة |
ميتفورمين 1000 ملغ محاولة |
سيتاقلبتين 50 ملغ محاولة + ميتفورمين 500 ملغ محاولة |
سيتاقلبتين 50 ملغ محاولة + ميتفورمين 1000 ملغ محاولة |
|
| ||||||
| A1C (٪) | العدد = 165 | ن = 175 | ن = 178 | العدد = 177 | العدد = 183 | ن = 178 |
| خط الأساس (الوسط) | 8.7 | 8.9 | 8.9 | 8.7 | 8.8 | 8.8 |
| التغيير من الأساس (المعدل المعدل)†) | 0.2 | -0.7 | -0.8 | -1.1 | -1.4 | -1.9 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) (95 ٪ CI) |
-0.8ج (-1.1, -0.6) |
-1.0ج (-1.2, -0.8) |
-1.3ج (-1.5, -1.1) |
-1.6ج (-1.8, -1.3) |
-2.1ج (-2.3, -1.8) |
|
| المرضى (٪) يحققون A1C <7٪ | 15 (9%) | 35 (20%) | 41 (23%) | 68 (38%) | 79 (43%) | 118 (66%) |
| المرضى الذين يتلقون الدواء الإنقاذ | 32 | 21 | 17 | 12 | 8 | 2 |
| FPG (mg / dL) | العدد = 169 | ن = 178 | العدد = 179 | العدد = 179 | العدد = 183 | ن = 180 |
| خط الأساس (الوسط) | 196 | 201 | 205 | 197 | 204 | 197 |
| التغيير من الأساس (المعدل المعدل)†) | 6 | -17 | -27 | -29 | -47 | -64 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) (95 ٪ CI) |
-23ج (-33, -14) |
-33ج (-43, -24) |
-35ج (-45, -26) |
-53ج (-62, -43) |
-70ج (-79, -60) |
|
| PPG لمدة ساعتين (mg / dL) | العدد = 129 | العدد = 136 | العدد = 141 | العدد = 138 | العدد = 147 | العدد = 152 |
| خط الأساس (الوسط) | 277 | 285 | 293 | 283 | 292 | 287 |
| التغيير من الأساس (المعدل المعدل)†) | 0 | -52 | -53 | -78 | -93 | -117 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) (95 ٪ CI) |
-52ج (-67, -37) |
-54ج (-69, -39) |
-78ج (-93, -63) |
-93ج (-107, -78) |
-117ج (-131, -102) |
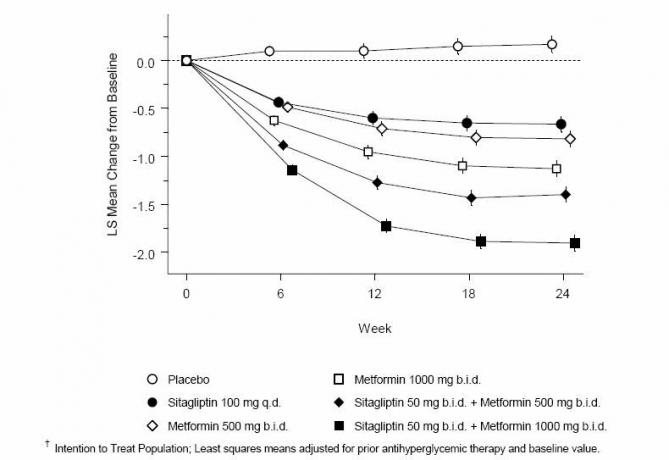
الشكل 1: متوسط التغير من خط الأساس لـ A1C (٪) على مدار 24 أسبوعًا باستخدام Sitagliptin و Metformin ، وحده وبالاشتراك مع مرضى السكري من النوع 2 ، يتم التحكم بشكل غير كافٍ في النظام الغذائي والتمارين الرياضية
بالإضافة إلى ذلك ، شملت هذه الدراسة المرضى (N = 117) مع ارتفاع السكر في الدم أكثر شدة (A1C> 11 ٪ أو الدم الجلوكوز> 280 ملغ / ديسيلتر الذين عولجوا بسيتاغليبتين مرتين يومياً في الملصق المفتوح 50 ملغ وميتفورمين 1000 ملغ. في هذه المجموعة من المرضى ، كان متوسط قيمة A1C الأساسي هو 11.2٪ ، متوسط FPG كان 314 مجم / ديسيلتر ، وكان متوسط PPG لمدة ساعتين 441 مجم / ديسيلتر. بعد 24 أسبوعًا ، لوحظ انخفاض متوسط من -2.9٪ لـ A1C و -127 ملغم / ديسيلتر لـ FPG و -208 ملغم / ديسيلتر لـ PPG لمدة ساعتين.
يجب أن يكون العلاج المركب الأولي أو الحفاظ على الجمع بين العلاج فرديًا ويترك لتقدير مقدم الرعاية الصحية.
العلاج الإضافي Sitagliptin في المرضى الذين يعانون من داء السكري من النوع 2 يتم التحكم فيه بشكل غير كاف على الميتفورمين وحده
شارك ما مجموعه 701 من مرضى السكري من النوع 2 في دراسة عشوائية لمدة 24 أسبوعًا ، مزدوجة التعمية ، وهمي تسيطر عليها تهدف إلى تقييم فعالية sitagliptin في تركيبة مع الميتفورمين. تم اختيارهم بصورة عشوائية من المرضى بالفعل على الميتفورمين (N = 431) بجرعة لا تقل عن 1500 ملغ يوميا بعد الانتهاء من فترة التشغيل الوهمي المفرد لمدة أسبوعين. المرضى الذين يتناولون الميتفورمين وعامل آخر لخفض السكر في الدم (N = 229) والمرضى الذين لا يتناولون أي عوامل لفرط سكر الدم (خارج العلاج لمدة لا تقل عن 8 تم اختيارهم بصورة عشوائية ، N = 41) بعد فترة التشغيل حوالي 10 أسابيع على الميتفورمين (بجرعة لا تقل عن 1500 ملغ يوميا) في وحيد. تم اختيارهم بصورة عشوائية من المرضى لإضافة إما 100 ملغ من sitagliptin أو وهمي ، تدار مرة واحدة يوميا. تم علاج المرضى الذين فشلوا في تحقيق أهداف نسبة السكر في الدم خلال الدراسات مع الإنقاذ بيوجليتازون.
في تركيبة مع الميتفورمين ، قدمت سيتاجليبتين تحسينات كبيرة في A1C و FPG و PPG لمدة ساعتين مقارنةً بالغفل مع الميتفورمين (الجدول 4). تم استخدام علاج نسبة السكر في الدم الإنقاذ في 5 ٪ من المرضى الذين عولجوا سيتاجليبتين 100 ملغ و 14 ٪ من المرضى الذين عولجوا بالدواء الوهمي. وقد لوحظ انخفاض مماثل في وزن الجسم لكلا الفريقين العلاج.
الجدول 4: معلمات نسبة السكر في الدم في الزيارة النهائية (دراسة لمدة 24 أسبوعًا) لسيتاجليبتين في العلاج المركب الإضافي مع الميتفورمين *
| Sitagliptin 100 ملغ QD + الميتفورمين |
الوهمي + الميتفورمين |
|
| ||
| A1C (٪) | ن = 453 | العدد = 224 |
| خط الأساس (الوسط) | 8.0 | 8.0 |
| التغيير من الأساس (المعدل المعدل)†) | -0.7 | -0.0 |
| الفرق من الدواء الوهمي + الميتفورمين (المعدل المعدل)†) (95 ٪ CI) |
-0.7ج (-0.8, -0.5) |
|
| المرضى (٪) يحققون A1C <7٪ | 213 (47%) | 41 (18%) |
| FPG (mg / dL) | ن = 454 | العدد = 226 |
| خط الأساس (الوسط) | 170 | 174 |
| التغيير من الأساس (المعدل المعدل)†) | -17 | 9 |
| الفرق من الدواء الوهمي + الميتفورمين (المعدل المعدل)†) (95 ٪ CI) |
-25ج (-31, -20) |
|
| PPG لمدة ساعتين (mg / dL) | العدد = 387 | ن = 182 |
| خط الأساس (الوسط) | 275 | 272 |
| التغيير من الأساس (المعدل المعدل)†) | -62 | -11 |
| الفرق من الدواء الوهمي + الميتفورمين (المعدل المعدل)†) (95 ٪ CI) |
-51ج (-61, -41) |
العلاج الإضافي Sitagliptin في المرضى الذين يعانون من داء السكري من النوع 2 يتم التحكم فيه بشكل غير مناسب على مزيج من الميتفورمين والجليمبيريد
شارك ما مجموعه 441 مريضًا يعانون من مرض السكري من النوع 2 في 24 أسبوعًا ، والعشوائية ، مزدوجة التعمية ، دراسة وهمي تسيطر عليها تهدف إلى تقييم فعالية سيتاجليبتين في تركيبة مع جليمبيريد ، مع أو بدون الميتفورمين. دخل المرضى في فترة العلاج في الجليميبيريد (حوالي 4 ملغ يوميًا) بمفردهم أو الغليميبيريد في تركيبة مع الميتفورمين (1500 ملغ يوميًا). بعد معايرة الجرعة وتشغيل الجرعة المستقرة في فترة تصل إلى 16 أسبوعًا وفترة التشغيل الوهمي لمدة أسبوعين ، فإن المرضى الذين يعانون من عدم كفاية تم اختيارهم بصورة عشوائية السيطرة على نسبة السكر في الدم (A1C 7.5 ٪ إلى 10.5 ٪) لإضافة إما 100 ملغ من سيتاجليبتين أو وهمي ، تدار مرة واحدة اليومي. تم علاج المرضى الذين فشلوا في تحقيق أهداف نسبة السكر في الدم خلال الدراسات مع الإنقاذ بيوجليتازون.
كان المرضى الذين يتلقون سيتاجليبتين مع الميتفورمين وجليمبيريد تحسينات كبيرة في A1C و FPG مقارنة مع المرضى الذين يتلقون الدواء الوهمي مع الميتفورمين و glimepiride (الجدول 5) ، مع تخفيضات متوسطة من خط الأساس بالنسبة إلى الدواء الوهمي في A1C بنسبة -0.9 ٪ وفي FPG من -21 ملغ / ديسيلتر. تم استخدام علاج الإنقاذ في 8 ٪ من المرضى الذين عولجوا بـ سيتاغليبتين 100 ملغ و 29 ٪ من المرضى الذين عولجوا بدواء وهمي إضافي. كان المرضى الذين عولجوا سيتاجليبتين الإضافية زيادة متوسط في وزن الجسم من 1.1 كجم مقابل. دواء وهمي إضافي (+0.4 كجم مقابل -0.7 كجم). بالإضافة إلى ذلك ، نتج عن إضافات سيتاغليبتين زيادة في معدل السكر في الدم مقارنةً بالعلاج الوهمي الإضافي. [نرى المحاذير والإحتياطات; ردود الفعل السلبية.]
الجدول 5: معلمات نسبة السكر في الدم في الزيارة النهائية (دراسة لمدة 24 أسبوعًا) لسيتاغليبتين مع الميتفورمين والجليمبيرايد *
| Sitagliptin 100 ملغ + الميتفورمين و Glimepiride |
الوهمي + الميتفورمين و Glimepiride |
|
| ||
| A1C (٪) | العدد = 115 | العدد = 105 |
| خط الأساس (الوسط) | 8.3 | 8.3 |
| التغيير من الأساس (المعدل المعدل)†) | -0.6 | 0.3 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) (95 ٪ CI) | -0.9ج (-1.1, -0.7) |
|
| المرضى (٪) يحققون A1C <7٪ | 26 (23%) | 1 (1%) |
| FPG (mg / dL) | العدد = 115 | العدد = 109 |
| خط الأساس (الوسط) | 179 | 179 |
| التغيير من الأساس (المعدل المعدل)†) | -8 | 13 |
| الفرق من الدواء الوهمي (المعدل المعدل)†) (95 ٪ CI) | -21ج (-32, -10) |
العلاج الإضافي Sitagliptin مقابل. Glipizide Add-on Therapy in المرضى الذين يعانون من داء السكري من النوع 2 يتم التحكم فيه بشكل غير كاف على الميتفورمين
تم تقييم فعالية sitagliptin في 52 ، تجربة مزدوجة التعمية ، والتحكم في noniferiority التي تسيطر عليها glipizide في المرضى الذين يعانون من مرض السكري من النوع 2. دخل المرضى الذين لا يتلقون علاجًا أو غيرهم من عوامل ارتفاع السكر في الدم فترة علاجية مدتها 12 أسبوعًا مع الميتفورمين أحادي (جرعة من 1500 ملغ يوميا) والتي شملت غسل الأدوية الأخرى غير الميتفورمين ، إذا المعمول بها. بعد فترة التشغيل ، تم اختيار عشوائي لأولئك الذين يعانون من نقص السكر في الدم السيطرة (A1C 6.5 ٪ إلى 10 ٪) 01:01 لإضافة سيتاجليبتين 100 ملغ مرة واحدة يوميا أو glipizide لمدة 52 أسبوعا. أعطيت للمرضى الذين يتلقون glipizide جرعة أولية من 5 ملغ / يوم ، ثم تم معايرتها بشكل اختياري على مدار الأسابيع الـ 18 التالية إلى الحد الأقصى للجرعة 20 ملغ / يوم حسب الحاجة لتحسين السيطرة على نسبة السكر في الدم. بعد ذلك ، كان من المفترض أن تبقى جرعة glipizide ثابتة ، باستثناء المعايرة لأسفل لمنع نقص السكر في الدم. كانت الجرعة المتوسطة من glipizide بعد فترة المعايرة 10 ملغ.
بعد 52 أسبوعًا ، كان لدى sitagliptin و glipizide تخفيضات مماثلة في الأساس من خط الأساس في A1C في تحليل النية إلى العلاج (الجدول 6). وكانت هذه النتائج متسقة مع تحليل لكل بروتوكول (الشكل 2). قد يقتصر الاستنتاج لصالح عدم النقص في سيتاجليبتين على glipizide على المرضى الذين يعانون من خط الأساس A1C مماثلة لتلك المدرجة في الدراسة (أكثر من 70 ٪ من المرضى لديهم A1C خط الأساس <8 ٪ وأكثر من 90 ٪ لديهم A1C <9%).
الجدول 6: معلمات نسبة السكر في الدم في دراسة مدتها 52 أسبوعًا تقارن سيتاغليبتين بالجليبيزيد كعلاج إضافي للمرضى الذين لا يتحكمون بشكل كافٍ في الميتفورمين (السكان النوايا إلى العلاج) *
| Sitagliptin 100 ملغ + الميتفورمين |
غليبيزيد + الميتفورمين |
|
| ||
| A1C (٪) | ن = 576 | ن = 559 |
| خط الأساس (الوسط) | 7.7 | 7.6 |
| التغيير من الأساس (المعدل المعدل)†) | -0.5 | -0.6 |
| FPG (mg / dL) | العدد = 583 | ن = 568 |
| خط الأساس (الوسط) | 166 | 164 |
| التغيير من الأساس (المعدل المعدل)†) | -8 | -8 |
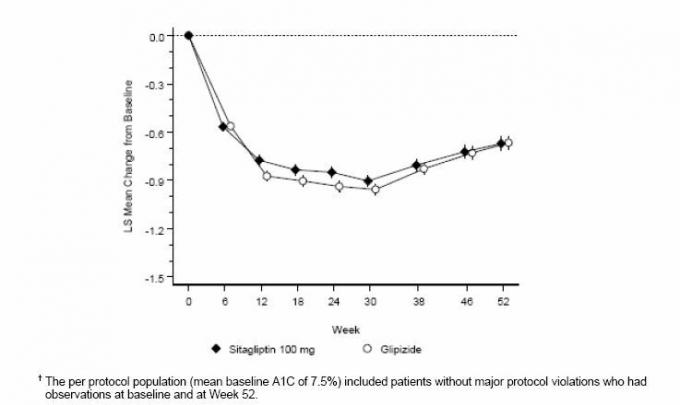
الشكل 2: يعني التغيير من خط الأساس لـ A1C (٪) أكثر من 52 أسبوعًا في دراسة تقارن Sitagliptin بـ Glipizide كعلاج إضافي للمرضى لا يتم التحكم فيه بشكل كافٍ على الميتفورمين (لكل بروتوكول سكان) â€
كانت نسبة الإصابة بنقص السكر في الدم في مجموعة سيتاغليبتين (4.9 ٪) أقل بشكل ملحوظ (P <0.001) عن تلك الموجودة في مجموعة glipizide (32.0 ٪). أظهر المرضى الذين عولجوا بـ سيتاغليبتين انخفاضًا كبيرًا في المتوسط عن خط الأساس في وزن الجسم مقارنةً بزيادة كبيرة في الوزن لدى المرضى الذين يدارون بجليبيزيد (-1.5 كجم مقابل +1.1 كجم).
أعلى
كيف زودت
رقم 6747 - أقراص جانوميت ، 50 مغ / 500 ملغ ، هي أقراص زهرية فاتحة ، على شكل كبسولة ، مغلفة بفيلم "575" على جانب واحد. يتم توفيرها على النحو التالي:
NDC 0006-0575-61 زجاجات الاستخدام من 60 وحدة
NDC 0006-0575-62 زجاجات استخدام وحدة من 180
NDC 0006-0575-52 حزم نفطة جرعة من 50
NDC 0006-0575-82 زجاجات كبيرة من 1000.
رقم 6749 - أقراص جانوميت ، 50 ملغ / 1000 ملغ ، أقراص حمراء على شكل كبسولة ، مغلفة بالأفلام مع "577" مخلوطة على جانب واحد. يتم توفيرها على النحو التالي:
NDC 0006-0577-61 زجاجات الاستخدام من 60 وحدة
NDC 0006-0577-62 زجاجات استخدام وحدة من 180
NDC 0006-0577-52 حزم نفطة وحدة من 50
NDC 0006-0577-82 زجاجات كبيرة من 1000.
متجر في 20-25 درجة مئوية (68-77 درجة فهرنهايت) ، والرحلات المسموح بها إلى 15-30 درجة مئوية (59-86 درجة فهرنهايت).
أعلى
معلومات استشارة المريض
تعليمات
يجب إبلاغ المرضى بالمخاطر والفوائد المحتملة لجانوميت وبالطرق البديلة للعلاج. يجب أن يتم إطلاعهم أيضًا على أهمية الالتزام بالتعليمات الغذائية والنشاط البدني المنتظم والدم الدوري مراقبة الجلوكوز واختبار A1C ، والاعتراف وإدارة نقص السكر في الدم وارتفاع السكر في الدم ، وتقييم لمرض السكري المضاعفات. خلال فترات التوتر مثل الحمى أو الصدمة أو العدوى أو الجراحة ، قد تتغير متطلبات الدواء ويجب أن ينصح المرضى بالتماس المشورة الطبية على الفور.
مخاطر الحماض اللبني الناجم عن مكون الميتفورمين ، وأعراضه ، والظروف التي تؤدي إلى تطوره ، كما هو موضح في المحاذير والإحتياطات، ينبغي شرح للمرضى. يجب أن ينصح المرضى بالتوقف عن استخدام Janumet على الفور وإخطار ممارسهم الصحي على الفور إذا كان فرط التنفس غير المبرر ، ألم عضلي ، الشعور بالضيق ، النعاس غير العادي ، الدوار ، ضربات القلب البطيئة أو غير المنتظمة ، الإحساس بالبرد (خاصة في الأطراف) أو أعراض أخرى غير محددة تحدث. أعراض الجهاز الهضمي شائعة أثناء بدء علاج الميتفورمين وقد تحدث أثناء بدء علاج جانوميت ؛ ومع ذلك ، يجب على المرضى استشارة الطبيب إذا ظهرت عليهم أعراض غير معروفة. على الرغم من أن أعراض الجهاز الهضمي التي تحدث بعد الاستقرار من غير المرجح أن تكون ذات صلة بالمخدرات ، مثل هذا يجب تقييم حدوث الأعراض لتحديد ما إذا كان ذلك بسبب الحماض اللبني أو غيره من الأمراض الخطيرة مرض.
يجب تقديم المشورة للمرضى ضد الإفراط في تناول الكحول ، سواء الحاد أو المزمن ، أثناء تلقي Janumet.
يجب إخطار المرضى بأهمية الاختبار المنتظم لوظيفة الكلى والمعلمات الدموية عند تلقي العلاج مع Janumet.
يجب إخطار المرضى بأنه تم الإبلاغ عن تفاعلات الحساسية أثناء استخدام ستاجليبتين لما بعد البيع ، وهو أحد مكونات جانوميت. إذا ظهرت أعراض الحساسية (بما في ذلك الطفح الجلدي وخلايا النحل وتورم في الوجه والشفتين واللسان والحلق) حدوث صعوبة في التنفس أو البلع) ، يجب على المرضى التوقف عن تناول Janumet وطلب المشورة الطبية حالا.
يجب أن يطلب الأطباء من مرضاهم قراءة إدخال حزمة المريض قبل البدء في علاج Janumet وإعادة قراءة كل مرة يتم فيها تجديد الوصفة. يجب توجيه المرضى لإبلاغ الطبيب أو الصيدلي إذا ظهرت عليهم أي أعراض غير عادية ، أو إذا استمرت أي أعراض معروفة أو تفاقمت.
اختبارات المعمل
يجب مراقبة الاستجابة لجميع علاجات السكري عن طريق القياسات الدورية لمستويات السكر في الدم و A1C ، بهدف خفض هذه المستويات نحو المعدل الطبيعي. A1C مفيد بشكل خاص لتقييم السيطرة على نسبة السكر في الدم على المدى الطويل.
المراقبة المبدئية والدورية للمعلمات الدموية (مثل الهيموغلوبين / الهيماتوكريت والدم الأحمر) يجب إجراء مؤشرات الخلايا) والوظيفة الكلوية (الكرياتينين في الدم) ، على الأقل على أساس سنوي. في حين أن فقر الدم الضخم الأرومي نادراً ما يشاهد مع علاج الميتفورمين ، إذا كان هذا هو المشتبه به ، فيجب استبعاد نقص فيتامين ب 12.
موزع من قبل:
MERCK & CO.، INC. ، محطة وايتهاوس ، NJ 08889 ، الولايات المتحدة الأمريكية
9794108
رقم براءة الاختراع الأمريكية: 6،699،871
1 علامة تجارية مسجلة لشركة MERCK & CO.، Inc. ، Whitehouse Station ، نيو جيرسي 08889 USA
2Trademark of MERCK & CO.، Inc.، Whitehouse Station، New Jersey 08889 USA
3GLUCOPHAGE® هي علامة تجارية مسجلة لشركة Merck Sante S.A.S ، وهي شركة تابعة لشركة Merck KGaA في دارمشتات ، ألمانيا.
مرخص لشركة بريستول مايرز سكويب.
حقوق النشر © 2007 ، 2008 MERCK & CO.، Inc.
كل الحقوق محفوظة
وضع العلامات للمريض من قبل إدارة الأغذية والعقاقير (FDA)
معلومات المريض
Janumet® (JAN-you-met)
(سيتاجليبتين / ميتفورمين حمض الهيدروكلوريك)
أجهزة لوحية
اقرأ معلومات المريض التي تأتي مع Janumet1 قبل البدء في تناولها وفي كل مرة تحصل على عبوة جديدة. قد تكون هناك معلومات جديدة. لا تحل هذه المنشورة مكان التحدث مع طبيبك حول حالتك الطبية أو علاجك.
ما هي أهم المعلومات التي يجب أن أعرفها عن Janumet؟
يمكن أن يسبب الميتفورمين هيدروكلوريد ، أحد المكونات الموجودة في Janumet ، آثارًا جانبية نادرة ولكنها خطيرة تسمى الحماض اللبني (تراكم حمض اللبنيك في الدم) يمكن أن تسبب الوفاة. الحماض اللبني هو حالة طبية طارئة ويجب علاجها في المستشفى.
توقف عن تناول Janumet واتصل بطبيبك على الفور إذا ظهرت لك أي من الأعراض التالية للحماض اللبني:
- تشعر بالضعف والتعب الشديد.
- لديك ألم عضلي غير عادي (غير طبيعي).
- لديك مشكلة في التنفس.
- لديك مشاكل في المعدة أو الأمعاء غير معروفة مع الغثيان والقيء أو الإسهال.
- تشعر بالبرد خاصة في ذراعيك وساقيك.
- تشعر بالدوار أو الدوار.
- لديك نبضات بطيئة أو غير منتظمة.
لديك فرصة أكبر للحصول على الحماض اللبني إذا:
- لديك مشاكل في الكلى.
- لديك مشاكل في الكبد.
- لديك قصور القلب الاحتقاني الذي يتطلب العلاج مع الأدوية.
- شرب الكثير من الكحول (في كثير من الأحيان أو على المدى القصير "الشراهة" الشرب).
- الحصول على الجفاف (فقدان كمية كبيرة من سوائل الجسم). يمكن أن يحدث هذا إذا كنت مريضًا بالحمى أو القيء أو الإسهال. يمكن أن يحدث الجفاف أيضًا عند التعرق كثيرًا بالنشاط أو التمارين ولا تشرب كمية كافية من السوائل.
- إجراء اختبارات معينة للأشعة السينية مع الأصباغ القابلة للحقن أو عوامل التباين.
- لديه عملية جراحية.
- يصاب بنوبة قلبية أو التهاب شديد أو سكتة دماغية.
- تبلغ من العمر 80 عامًا أو أكبر ولم يتم اختبار وظائف الكلى لديك.
ما هو جانوميت؟
تحتوي أقراص جانوميت على دواء وصفة طبية ، سيتاجليبتين (JANUVIA ™ 2) وميتفورمين. Janumet يمكن استخدامها جنبا إلى جنب مع اتباع نظام غذائي وممارسة لخفض نسبة السكر في الدم في المرضى البالغين المصابين بالنوع 2 من مرض السكري. سيحدد طبيبك ما إذا كان Janumet مناسبًا لك وسيحدد أفضل طريقة لبدء ومواصلة علاج مرض السكري الخاص بك.
Janumet:
- يساعد على تحسين مستويات الأنسولين بعد الوجبة.
- يساعد الجسم على الاستجابة بشكل أفضل للأنسولين الذي يصنعه بشكل طبيعي.
- يقلل من كمية السكر التي يصنعها الجسم.
- من غير المرجح أن يسبب انخفاض نسبة السكر في الدم (نقص السكر في الدم) عندما يؤخذ في حد ذاته لعلاج ارتفاع نسبة السكر في الدم.
Janumet لم تدرس في الأطفال دون سن 18 سنة.
لم يتم دراسة Janumet مع الأنسولين ، وهو دواء معروف بأنه يسبب انخفاض نسبة السكر في الدم.
الذي لا ينبغي أن تأخذ Janumet؟
لا تأخذ Janumet إذا كنت:
- لديك مرض السكري من النوع 1.
- لديك بعض مشاكل الكلى.
- لديهم حالات تسمى الحماض الأيضي أو الحماض الكيتوني السكري (زيادة الكيتونات في الدم أو البول).
- كان لديك رد فعل تحسسي ل Janumet أو sitagliptin (JANUVIA) ، أحد مكونات Janumet.
- سيتلقى حقن صبغة أو عوامل تباين لإجراء الأشعة السينية ، سوف تحتاج إلى إيقاف جانوميت لفترة قصيرة. تحدث إلى طبيبك حول موعد إيقاف Janumet وموعد البدء من جديد. راجع "ما هي أهم المعلومات التي يجب أن أعرفها عن Janumet؟"
ماذا يجب أن أخبر طبيبي قبل وأثناء العلاج مع Janumet؟
قد لا يكون Janumet مناسبًا لك. أخبر طبيبك عن جميع الحالات الطبية ، بما في ذلك إذا:
- لديك مشاكل في الكلى.
- لديك مشاكل في الكبد.
- كان لديك رد فعل تحسسي ل Janumet أو sitagliptin (JANUVIA) ، أحد مكونات Janumet.
- لديك مشاكل في القلب ، بما في ذلك قصور القلب الاحتقاني.
- أكبر من 80 سنة. لا ينبغي على المرضى الذين تزيد أعمارهم عن 80 عامًا تناول Janumet إلا إذا تم فحص وظائف الكلى لديهم وكان ذلك طبيعيًا.
- شرب الكثير من الكحول (طوال الوقت أو شرب "حفلة" على المدى القصير).
- حاملا أو تخطط لتصبح حاملا. من غير المعروف ما إذا كانت جانوميت ستؤذي طفلك الذي لم يولد بعد. إذا كنت حاملاً ، فتحدث مع طبيبك حول أفضل طريقة للسيطرة على نسبة السكر في الدم أثناء الحمل. إذا كنت تستخدم Janumet أثناء الحمل ، فتحدث مع طبيبك حول كيفية وجودك في سجل Janumet. رقم الهاتف المجاني لسجل الحمل هو 1-800-986-8999.
- هي الرضاعة الطبيعية أو خطة للرضاعة الطبيعية. ليس من المعروف ما إذا كانت جانوميت ستنتقل إلى حليب الثدي. تحدث إلى طبيبك حول أفضل طريقة لإطعام طفلك إذا كنت تتناول Janumet.
أخبر طبيبك عن جميع الأدوية التي تتناولها ، بما في ذلك الأدوية الموصوفة وغير الموصوفة ، والفيتامينات ، والمكملات العشبية. قد يؤثر Janumet على مدى فعالية الأدوية الأخرى وبعض الأدوية يمكن أن تؤثر على مدى نجاح Janumet.
تعرف الأدوية التي تتناولها. احتفظ بقائمة الأدوية الخاصة بك وأظهرها للطبيب والصيدلي عندما تحصل على دواء جديد. تحدث إلى طبيبك قبل البدء في أي دواء جديد.
كيف يجب أن تأخذ Janumet؟
- سيخبرك طبيبك بعدد أقراص Janumet التي يجب تناولها وعدد مرات تناولها. خذ Janumet تمامًا كما يخبرك طبيبك.
- قد يحتاج طبيبك إلى زيادة الجرعة للسيطرة على نسبة السكر في الدم.
- قد يصف لك الطبيب Janumet مع سلفونيل يوريا (دواء آخر لخفض نسبة السكر في الدم). راجع "ما هي الآثار الجانبية المحتملة لجانوميت؟" للحصول على معلومات حول زيادة خطر انخفاض نسبة السكر في الدم.
- خذ Janumet مع وجبات الطعام لخفض فرصتك في اضطراب في المعدة.
- استمر في تناول Janumet طالما أخبرك طبيبك.
- إذا كنت تأخذ الكثير من Janumet ، فاتصل بطبيبك أو مركز مراقبة السموم على الفور.
- إذا فاتتك جرعة ، خذها مع الطعام بمجرد تذكرها. إذا كنت لا تتذكر حتى يحين وقت تناول الجرعة التالية ، فانتقل للجرعة الفائتة ثم عد إلى جدولك المعتاد. لا تأخذ جرعتين من Janumet في نفس الوقت.
- قد تحتاج إلى التوقف عن تناول Janumet لفترة قصيرة. اتصل بطبيبك للحصول على التعليمات إذا:
- يعانون من الجفاف (فقدوا الكثير من سوائل الجسم). يمكن أن يحدث الجفاف إذا كنت مريضاً بالقيء الشديد أو الإسهال أو الحمى ، أو إذا كنت تشرب كمية أقل بكثير من السوائل عن المعتاد.
- تخطط لإجراء عملية جراحية.
- سيحصلون على حقن صبغة أو عامل تباين لإجراء الأشعة السينية.
راجع "ما هي أهم المعلومات التي يجب أن أعرفها عن Janumet؟" و "من لا يجب أن يأخذ جانوميت؟"
- عندما يكون جسمك تحت بعض أنواع التوتر ، مثل الحمى والصدمات النفسية (مثل حادث سيارة) أو العدوى أو الجراحة ، فقد يتغير مقدار دواء السكري الذي تحتاجه. أخبر طبيبك على الفور إذا كان لديك أي من هذه الشروط واتبع تعليمات الطبيب.
- راقب نسبة السكر في دمك كما يخبرك طبيبك بذلك.
- ابق على نظامك الغذائي وممارسة التمارين الرياضية الموصوفة أثناء تناول Janumet.
- تحدث إلى طبيبك حول كيفية منع انخفاض السكر في الدم (انخفاض السكر في الدم) والتعرف عليه وإدارته (ارتفاع السكر في الدم) ومضاعفات مرض السكري.
- سيقوم طبيبك بمراقبة مرض السكر الخاص بك من خلال اختبارات الدم المنتظمة ، بما في ذلك مستويات السكر في الدم والهيموغلوبين A1C.
- سيقوم الطبيب بإجراء فحوصات دم للتحقق من وظائف الكلى قبل وأثناء العلاج مع Janumet.
ما هي الآثار الجانبية المحتملة لل Janumet؟
Janumet يمكن أن يسبب آثار جانبية خطيرة. راجع "ما هي أهم المعلومات التي يجب أن أعرفها عن Janumet؟"
الآثار الجانبية الشائعة عند تناول Janumet تشمل:
- انسداد أو سيلان الأنف والتهاب الحلق
- عدوى الجهاز التنفسي العلوي
- إسهال
- استفراغ و غثيان
- الغاز ، وعدم الراحة في المعدة ، وعسر الهضم
- ضعف
- صداع الراس
يمكن أن يساعد تناول Janumet مع الوجبات على تقليل الآثار الجانبية الشائعة للمعدة للميتفورمين التي تحدث عادة في بداية العلاج. إذا كنت تعاني من مشاكل غير عادية أو غير متوقعة في المعدة ، فتحدث مع طبيبك. قد تكون مشاكل المعدة التي تبدأ في وقت لاحق أثناء العلاج علامة على شيء أكثر خطورة.
بعض أدوية السكري ، مثل السلفونيل يوريا والميغليتينيدات ، يمكن أن تسبب انخفاض نسبة السكر في الدم (نقص السكر في الدم). عند استخدام Janumet مع هذه الأدوية ، قد يكون لديك سكريات في الدم منخفضة للغاية. قد يصف طبيبك جرعات أقل من دواء السلفونيل يوريا أو دواء ميجليتينيد. أخبر طبيبك إذا كنت تعاني من مشاكل انخفاض السكر في الدم.
تم الإبلاغ عن الآثار الجانبية الإضافية التالية بشكل عام مع Janumet أو sitagliptin:
- يمكن أن تحدث تفاعلات حساسية خطيرة مع Janumet أو sitagliptin ، أحد الأدوية في Janumet. قد تشمل أعراض رد الفعل التحسسي الخطير الطفح الجلدي وخلايا النحل وتورم في الوجه والشفتين واللسان والحلق وصعوبة في التنفس أو البلع. إذا كان لديك رد فعل تحسسي ، فتوقف عن تناول Janumet واتصل بطبيبك على الفور. قد يصف طبيبك دواء لعلاج رد فعلك التحسسي ودواء آخر لمرض السكري الخاص بك.
- انزيمات الكبد المرتفعة.
- التهاب البنكرياس.
هذه ليست جميع الآثار الجانبية المحتملة لل Janumet. لمزيد من المعلومات ، اسأل طبيبك.
أخبر طبيبك إذا كان لديك أي آثار جانبية تزعجك ، أو غير عادية ، أو لا تختفي.
كيف يمكنني تخزين Janumet؟
تخزين Janumet في درجة حرارة الغرفة ، 68-77 درجة فهرنهايت (20-25 درجة مئوية).
الحفاظ على Janumet وجميع الأدوية بعيدا عن متناول الأطفال.
معلومات عامة حول استخدام Janumet
توصف الأدوية في بعض الأحيان للحالات التي لم يتم ذكرها في منشورات معلومات المريض. لا تستخدم Janumet لحالة لم يشرع لها. لا تعطي Janumet لأشخاص آخرين ، حتى لو كان لديهم نفس الأعراض لديك. قد تضر بهم.
تلخص هذه النشرة أهم المعلومات حول Janumet. إذا كنت ترغب في معرفة المزيد من المعلومات ، فتحدث مع طبيبك. يمكنك أن تطلب من طبيبك أو الصيدلي الحصول على معلومات حول Janumet المكتوبة للمهنيين الصحيين. لمزيد من المعلومات اتصل على 1-800-622-4477.
ما هي المكونات في Janumet؟
المكونات النشطة: سيتاجليبتين وميتفورمين هيدروكلوريد.
المكونات غير النشطة: السليلوز الجريزوفولفين ، بولي فينيل بيروليدون ، سلفات لوريل الصوديوم ، وفومارات ستيرل الصوديوم. يحتوي غلاف الفيلم اللوحي على المكونات غير النشطة التالية: كحول البولي فينيل ، بولي إيثيلين جليكول ، التلك ، ثاني أكسيد التيتانيوم ، أكسيد الحديد الأحمر ، وأكسيد الحديد الأسود.
ما هو مرض السكري من النوع 2؟
داء السكري من النوع 2 هو حالة لا ينتج فيها جسمك ما يكفي من الأنسولين ، والانسولين الذي ينتجه جسمك لا يعمل كما ينبغي. يمكن لجسمك أيضًا إنتاج الكثير من السكر. عندما يحدث هذا ، يتراكم السكر (الدم) في الدم. هذا يمكن أن يؤدي إلى مشاكل طبية خطيرة.
الهدف الرئيسي من علاج مرض السكري هو خفض نسبة السكر في الدم إلى المستوى الطبيعي. قد يساعد خفض السكر في الدم والسيطرة عليه في منع أو تأخير مضاعفات مرض السكري ، مثل مشاكل القلب ومشاكل الكلى والعمى والبتر.
يمكن خفض نسبة السكر في الدم المرتفعة عن طريق اتباع نظام غذائي وممارسة ، وبعض الأدوية عند الضرورة.
صدر مارس 2009
موزع من قبل:
MERCK & CO.، INC. ، محطة وايتهاوس ، NJ 08889 ، الولايات المتحدة الأمريكية
آخر تحديث: 03/09
Janumet ، Sitagliptin و Metformin هيدروكلوريد ، معلومات للمرضى (في سهل الانجليزية)
معلومات مفصلة عن العلامات والأعراض والأسباب والعلاج من مرض السكري
لا تهدف المعلومات الواردة في هذه الدراسة إلى تغطية جميع الاستخدامات أو الاتجاهات أو الاحتياطات الممكنة أو التفاعلات الدوائية أو الآثار الضارة. هذه المعلومات معممة ولا تهدف إلى تقديم المشورة الطبية المحددة. إذا كانت لديك أسئلة حول الأدوية التي تتناولها أو ترغب في مزيد من المعلومات ، فاستشر طبيبك أو الصيدلي أو الممرض.
ارجع الى: تصفح جميع الأدوية لمرض السكري



