Iloperidone (fanapt) معلومات وصفية كاملة
اسم العلامة التجارية: Fanapt
الاسم العام: ايلوبيريدون
Fanapt (إيلوبيريدون) دليل وصف (بي دي إف)
محتويات:
تحذير محاصر
مؤشرات والاستخدام
الجرعة والإدارة
موانع
المحاذير والإحتياطات
ردود الفعل السلبية
تفاعل الأدوية
استخدام في السكان محددة
تعاطي المخدرات والاعتماد عليها
جرعة مفرطة
وصف
علم الصيدلة السريرية
علم السموم غير الإكلينيكي
الدراسات السريرية
كيف زودت
دليل الدواء Brintellix
تحذير: زيادة الوفاة لدى المرضى المسنين المصابين بنفسية عقلية
المرضى المسنون الذين يعانون من الذهان المرتبط بالخرف ويعالجون بالأدوية المضادة للذهان هم أكثر عرضة للوفاة. لم تتم الموافقة على FANAPT لعلاج المرضى الذين يعانون من الذهان المرتبط بالخرف.
مؤشرات والاستخدام
يشار إلى FANAPT® لعلاج مرض انفصام الشخصية لدى البالغين.
عند اتخاذ القرار بين العلاجات البديلة المتاحة لهذا الشرط ، ينبغي أن يفكر الواصف في اكتشاف أن FANAPT يرتبط بإطالة فترة QTc. يرتبط إطالة الفاصل الزمني QTc في بعض الأدوية الأخرى مع القدرة على التسبب في توران دي عدم انتظام ضربات القلب ، وهو عدم انتظام دقات القلب البطيني متعدد الأشكال الذي يمكن أن يؤدي إلى مفاجئ الموت. في العديد من الحالات ، قد يؤدي ذلك إلى استنتاج أنه يجب تجربة العقاقير الأخرى أولاً. ما إذا كان FANAPT سوف يتسبب في حدوث torsade de pointes أو زيادة معدل الموت المفاجئ.
يجب معايرة المرضى بجرعة فعالة من FANAPT. وبالتالي ، قد يتأخر التحكم في الأعراض خلال الأسابيع الأولى إلى الأسبوعين من العلاج مقارنة ببعض الأدوية المضادة للذهان الأخرى التي لا تتطلب معايرة مماثلة. يجب أن يأخذ الوصفات في الاعتبار هذا التأخير عند اختيار دواء مضاد للذهان لعلاج الفصام.
مواصلة القصة أدناه
الجرعة والإدارة
الجرعة المعتادة
يجب معايرة FANAPT ببطء من جرعة بدء منخفضة لتجنب انخفاض ضغط الدم الانتصابي نظرًا لخصائص حظر ألفا الأدرينالية. جرعة البدء الموصى بها لأقراص FANAPT هي 1 ملغ عن طريق الفم مرتين يوميًا. يمكن إجراء زيادة الجرعة للوصول إلى النطاق المستهدف وهو 6-12 ملغ مرتين يوميًا (12-24 ملغ / يوم) مع تعديلات جرعات يومية لا تتجاوز 2 ملغ مرتين يوميًا (4 ملغ / يوم). الجرعة القصوى الموصى بها هي 12 ملغ مرتين يوميًا (24 ملغ / يوم). لم يتم تقييم جرعات FANAPT التي تزيد عن 24 ملغ / يوم بشكل منهجي في التجارب السريرية. أثبتت فعالية مع FANAPT في نطاق جرعة من 6 إلى 12 ملغ مرتين يوميا. يجب أن يكون واضعو الأدوية على دراية بحقيقة أن المرضى يحتاجون إلى معايرة الجرعة الفعالة من FANAPT. وبالتالي ، قد يتأخر التحكم في الأعراض خلال الأسابيع الأولى إلى الأسبوعين من العلاج مقارنة ببعض الأدوية المضادة للذهان الأخرى التي لا تتطلب معايرة مماثلة. يجب أن يكون الواصفون أيضًا على دراية بأن بعض الآثار الضارة المرتبطة باستخدام FANAPT ترتبط بالجرعة. يمكن أن تدار FANAPT دون النظر إلى وجبات الطعام.
جرعة في السكان الخاصة
ضبط الجرعة للمرضى الذين يتناولون FANAPT بالتزامن مع مثبطات CYP2D6 المحتملة: يجب أن تكون جرعة FANAPT يتم تقليله بمقدار النصف عند إعطائه بالتزامن مع مثبطات قوية CYP2D6 مثل فلوكستين أو باروكستين. عند سحب مثبط CYP2D6 من العلاج المركب ، ينبغي عندئذ زيادة جرعة FANAPT إلى حيث كانت من قبل.
ضبط الجرعة للمرضى الذين يتناولون FANAPT بالتزامن مع مثبطات CYP3A4 المحتملة: يجب أن تكون جرعة FANAPT يتم تقليله بمقدار النصف عند تناوله بالتزامن مع مثبطات CYP3A4 القوية مثل الكيتوكونازول أو كلاريثروميسين. عندما يتم سحب مثبط CYP3A4 من العلاج المركب ، يجب زيادة جرعة FANAPT إلى ما كانت عليه من قبل.
تعديل الجرعة للمرضى الذين يتناولون FANAPT والذين هم من المستقلبات الضعيفة للـ CYP2D6: يجب تخفيض جرعة FANAPT بمقدار النصف من أجل المستقلبات الضعيفة للـ CYP2D6.
القصور الكبدي: لا توجد حاجة لتعديل جرعة FANAPT في المرضى الذين يعانون من اختلال كبدي خفيف. المرضى الذين يعانون من اختلال كبدي معتدل قد يحتاجون إلى تخفيض الجرعة ، إذا أشير سريريا. لا ينصح FANAPT للمرضى الذين يعانون من اختلال كبدي حاد.
علاج الصيانة
في دراسة طويلة الأجل ، كان FANAPT فعالاً في تأخير الوقت للانتكاس في مرضى الفصام الذين استقروا في FANAPT حتى 24 ملغ / يوم. يجب إعادة تقييم المرضى بشكل دوري لتحديد الحاجة إلى علاج الصيانة.
إعادة العلاج في المرضى الذين تم إيقافهم مسبقًا على الرغم من عدم وجود بيانات خاصة بمعالجة التكرار العلاج ، يوصى باتباع جدول معايرة البدء كلما كان لدى المرضى فاصل قبالة FANAPT أكثر من 3 ايام
أعلى
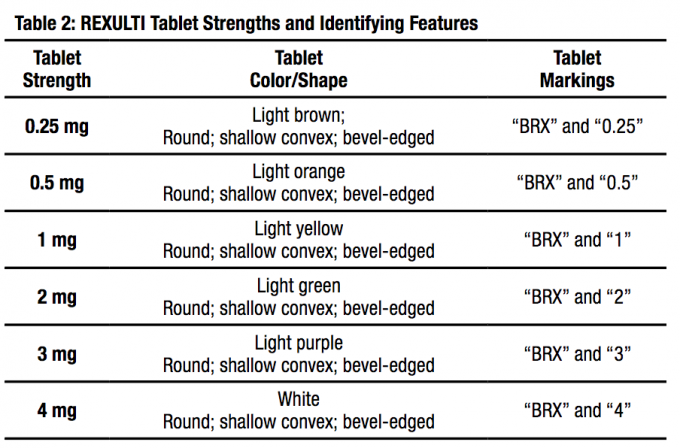
أشكال الجرعات ونقاط القوة
تتوفر أقراص FANAPT في نقاط القوة التالية: 1 ملغ ، 2 ملغ ، 4 ملغ ، 6 ملغ ، 8 ملغ ، 10 ملغ ، و 12 ملغ. تكون الأقراص بيضاء ، مستديرة ، مسطحة ، ذات حواف مشطوفة ومحددة بشعار "" تم نقشه على جانب واحد وقوة الكمبيوتر اللوحي "1" ، "2" ، "4" ، "6" ، "8" ، "10" ، أو "12" debossed على الجانب الآخر.
أعلى
موانع
هو بطلان FANAPT في الأفراد الذين يعانون من رد فعل فرط الحساسية المعروف للمنتج. وقد تم الإبلاغ عن الحساسية المفرطة ، وذمة وعائية ، وغيرها من ردود الفعل فرط الحساسية.
أعلى
المحاذير والإحتياطات
زيادة الوفيات في المرضى المسنين المصابين بذهان متعلق بالخرف
الأدوية المضادة للذهان تزيد من خطر الوفاة في جميع المرضى الذين يعانون من الذهان المرتبط بالخرف. تحليلات لـ 17 تجربة ذات صلة بدواء وهمي مرتبطة بالذهان (مدة مدتها 10 أسابيع وبشكل كبير في المرضى الذين يتناولون غير نمطية الأدوية المضادة للذهان) كشفت عن خطر الوفاة في المرضى الذين عولجوا بالمخدرات من 1.6 إلى 1.7 مرة في المرضى الذين عولجوا بالدواء الوهمي. على مدار تجربة نموذجية مدتها 10 أسابيع ، كان معدل الوفيات في المرضى الذين عولجوا بالمخدرات حوالي 4.5 ٪ ، مقارنة بمعدل حوالي 2.6 ٪ في المرضى الذين عولجوا بالدواء الوهمي.
على الرغم من أن أسباب الوفاة كانت متباينة ، إلا أن معظم الوفيات كانت إما أمراض القلب والأوعية الدموية (على سبيل المثال ، قصور القلب ، الموت المفاجئ) أو المعدية (مثل الالتهاب الرئوي) في الطبيعة. لم تتم الموافقة على FANAPT لعلاج المرضى الذين يعانون من الذهان المرتبط بالخرف.
ردود الفعل السلبية للمخ والأوعية الدموية ، بما في ذلك السكتة الدماغية ، عند المرضى المسنين المصابين بذهان متعلق بالخرف
في التجارب التي تسيطر عليها وهمي في الأشخاص المسنين المصابين بالخرف ، تم اختيار المرضى بشكل عشوائي لريسبيريدون ، أريبيبرازول ، وأولانزيبين كان لهما ارتفاع في الإصابة بالجلطة الدماغية والهجوم الإقفاري العابر ، بما في ذلك الوفاة السكتة الدماغية. لم تتم الموافقة على FANAPT لعلاج المرضى الذين يعانون من الذهان المرتبط بالخرف.
إطالة كيو تي
في دراسة QTc مفتوحة التسمية عند مرضى الفصام أو اضطراب الفصام (ن = 160) ، ارتبط FANAPT بإطالة QTc لمدة 9 مللي ثانية بجرعة iloperidone من 12 ملغ مرتين يوميًا. تمت زيادة تأثير FANAPT على الفاصل الزمني QT من خلال وجود تثبيط أيضي CYP450 2D6 أو 3A4 (الباروكستين 20 ميلي غرام مرة واحدة يوميًا والكيتوكونازول 200 ميلي غرام مرتين يوميًا على التوالي). في ظل ظروف تثبيط الأيض لكل من 2D6 و 3 A4 ، ارتبط FANAPT 12 ملغ مرتين يوميًا بزيادة QTcF المتوسطة من خط الأساس حوالي 19 ميللي ثانية.
لم يلاحظ أي حالات من تورس دي بوينت أو غيرها من عدم انتظام ضربات القلب الشديدة خلال البرنامج السريري قبل التسويق.
يجب تجنب استخدام FANAPT بالاقتران مع أدوية أخرى معروفة بإطالة QTc بما في ذلك الفئة 1A (مثل الكينيدين والبروكيناميد) أو الفئة الثالثة (على سبيل المثال ، الأميودارون ، السوتالول) الأدوية المضادة لاضطراب النظم ، الأدوية المضادة للذهان (مثل الكلوربرومازين ، الثيوريدازين) ، المضادات الحيوية (على سبيل المثال ، جاتيفلوكساسين ، موكسيفلوكساسين) ، أو أي فئة أخرى من الأدوية المعروفة بإطالة فترة QTc (على سبيل المثال ، البنتاميدين ، أسيتات ليفوميثاديل ، الميثادون). كما يجب تجنب FANAPT في المرضى الذين يعانون من متلازمة كيو تي الطويلة الخلقية وفي المرضى الذين لديهم تاريخ من عدم انتظام ضربات القلب.
قد تؤدي بعض الظروف إلى زيادة خطر حدوث torsade de pointes و / أو الموت المفاجئ مع استخدام الأدوية التي تطيل فترة QTc ، بما في ذلك (1) بطء القلب ؛ (2) نقص بوتاسيوم الدم أو نقص مغنيزيوم الدم ؛ (3) ما يصاحب ذلك من استخدام الأدوية الأخرى التي تطيل فترة QTc ؛ و (4) وجود الإطالة الخلقية للفاصل الزمني QT ؛ (5) احتشاء عضلة القلب الحاد مؤخرا. و / أو (6) قصور القلب غير المكافئ.
هناك ما يبرر الحذر عند وصف FANAPT مع الأدوية التي تمنع الأيض FANAPT ، وفي المرضى الذين يعانون من انخفاض نشاط CYP2D6.
من المستحسن أن يتم النظر في علاج المرضى الذين يعانون من خطر كبير الاضطرابات المنحل بالكهرباء لها قياسات البوتاسيوم والمغنيسيوم في المصل بشكل دوري الرصد. نقص بوتاسيوم الدم (و / أو نقص مغنيزيوم الدم) قد يزيد من خطر إطالة كيو تي وعدم انتظام ضربات القلب. يجب تجنب FANAPT shoul d في المرضى الذين يعانون من تاريخ الإصابة بأمراض القلب والأوعية الدموية الهامة ، على سبيل المثال ، كيو تي إطالة ، احتشاء عضلة القلب الحاد في الآونة الأخيرة ، وفشل القلب دون تعويض ، أو عدم انتظام ضربات القلب. يجب إيقاف FANAPT في المرضى الذين وجدوا أن قياسات QTc المستمرة> 500 ميللي ثانية.
إذا كان المرضى الذين يتناولون FANAPT يعانون من الأعراض التي يمكن أن تشير إلى حدوث عدم انتظام ضربات القلب ، على سبيل المثال ، دوخة ، خفقان ، أو إغماء ، ينبغي للواصف الشروع في إجراء مزيد من التقييم ، بما في ذلك القلب الرصد.
متلازمة الخبيثة العصبية (NMS)
تم الإبلاغ عن وجود مجموعة من الأعراض القاتلة التي يُشار إليها أحيانًا باسم متلازمة الخبيثة العصبية (NMS) بالتعاون مع تناول الأدوية المضادة للذهان ، بما في ذلك FANAPT. المظاهر السريرية تشمل فرط بيركسيا الدم ، صلابة العضلات ، تغير الحالة العقلية (بما في ذلك العلامات الكاتونية) و دليل على عدم الاستقرار اللاإرادي (النبض غير المنتظم أو ضغط الدم ، عدم انتظام دقات القلب ، الحجاب الحاجز ، والقلب خلل إيقاعي). قد تشمل العلامات الإضافية ارتفاع فسفوكيناز الكرياتين ، بيلة الميوغلوبين (انحلال الربيدات) ، والفشل الكلوي الحاد. التقييم التشخيصي للمرضى الذين يعانون من هذه المتلازمة معقد. عند الوصول إلى التشخيص ، من المهم تحديد الحالات التي يشملها العرض السريري كل من مرض طبي خطير وعلامات وأعراض خارج هرمية غير معالجة أو غير كافية (EPS). تشمل الاعتبارات المهمة الأخرى في التشخيص التفريقي السمية المركزية المضادة للكولين ، والسكتة الحرارية ، وحمى المخدرات ، وأمراض الجهاز العصبي المركزي (CNS) الأساسية.
يجب أن تشمل إدارة هذه المتلازمة ما يلي: (1) الإيقاف الفوري للعقاقير المضادة للذهان والأدوية الأخرى غير الضرورية للعلاج المتزامن ، (2) علاج الأعراض المركزة والمراقبة الطبية ، و (3) علاج أي مشاكل طبية خطيرة يصاحبها والتي تتوفر علاجات محددة. لا يوجد اتفاق عام حول أنظمة علاج دوائية محددة لل NMS.
إذا كان المريض يحتاج إلى علاج للأدوية المضادة للذهان بعد الشفاء من NMS ، فيجب إعادة النظر في إعادة المعالجة المحتملة للعلاج الدوائي بعناية. يجب مراقبة المريض بعناية ، حيث تم الإبلاغ عن تكرار NMS.
خلل الحركة المتأخر
خلل الحركة المتأخر هو متلازمة تتكون من حركات خلل الحركة التي لا رجعة فيها ، والتي قد تحدث في المرضى الذين عولجوا بالأدوية المضادة للذهان. على الرغم من أن معدل انتشار المتلازمة يبدو أعلى بين كبار السن ، وخاصة النساء المسنات ، إلا أنه من المستحيل الاعتماد على تقديرات الانتشار للتنبؤ ، عند بدء العلاج بمضادات الذهان ، والتي من المحتمل أن يصاب بها المرضى متلازمة. ما إذا كانت منتجات الأدوية المضادة للذهان تختلف في قدرتها على التسبب في خلل الحركة المتأخر غير معروف.
ويعتقد خطر الاصابة بخلل الحركة المتأخر واحتمال أن تصبح لا رجعة فيه لزيادة مدة العلاج والجرعة التراكمية الإجمالية المضادة للذهان تدار يزيد. ومع ذلك ، يمكن أن تحدث المتلازمة ، على الرغم من أنها أقل شيوعًا ، بعد فترات العلاج القصيرة نسبياً بجرعات منخفضة.
لا يوجد علاج معروف لحالات خلل الحركة المتأخر ، على الرغم من أن المتلازمة قد تتحول جزئيًا أو كليًا إذا تم سحب العلاج المضاد للذهان. ومع ذلك ، فإن العلاج المضاد للذهان نفسه قد يقمع (أو يقمع جزئيًا) علامات وأعراض المتلازمة وبالتالي قد يخفي العملية الأساسية. تأثير قمع الأعراض على المسار الطويل الأجل للمتلازمة غير معروف.
بالنظر إلى هذه الاعتبارات ، ينبغي وصف FANAPT بطريقة من المرجح أن تقلل من حدوث خلل الحركة المتأخر. ينبغي عمومًا حجز المعالجة المضادة للذهان المزمنة للمرضى الذين يعانون من مرض مزمن يعرف عنه (1) الاستجابة له الأدوية المضادة للذهان ، و (2) الذين لا تتوفر أو تتوفر علاجات بديلة لهم نفس القدر من الفعالية ، ولكن ربما تكون أقل ضرراً مناسب. بالنسبة للمرضى الذين يحتاجون إلى علاج مزمن ، يجب البحث عن أصغر جرعة وأقصر مدة علاج تنتج استجابة سريرية مرضية. يجب إعادة تقييم الحاجة لاستمرار العلاج بشكل دوري.
إذا ظهرت علامات وأعراض خلل الحركة المتأخر في المريض على FANAPT ، فينبغي مراعاة وقف الدواء. ومع ذلك ، قد يحتاج بعض المرضى إلى العلاج باستخدام FANAPT على الرغم من وجود المتلازمة.
التغييرات الأيضية
ارتبطت الأدوية المضادة للذهان غير التقليدية بالتغيرات الأيضية التي قد تزيد من خطر الإصابة بالأمراض القلبية الوعائية / المخية. وتشمل هذه التغييرات الأيضية ارتفاع السكر في الدم ، دسليبيدميا ، وزيادة وزن الجسم. بينما ثبت أن جميع الأدوية المضادة للذهان غير التقليدية تنتج بعض التغييرات الأيضية ، فإن كل دواء في الفئة لديه بيان مخاطر خاص به.
ارتفاع السكر في الدم والسكري
تم الإبلاغ عن ارتفاع السكر في الدم ، في بعض الحالات المتطرفة والمرتبط بالحماض الكيتوني أو الغيبوبة المفرطة أو الوفاة ، في المرضى الذين عولجوا بمضادات الذهان غير التقليدية بما في ذلك FANAPT. تعقيد تقييم العلاقة بين استخدام مضادات الذهان غير التقليدية وتشوهات الجلوكوز بسبب احتمال زيادة خطر الخلفية لمرض السكري في مرضى الفصام وتزايد حالات الإصابة بداء السكري بشكل عام تعداد السكان. بالنظر إلى هذه الإرباك ، فإن العلاقة بين استخدام مضادات الذهان غير التقليدية والأحداث الضارة المرتبطة بفرط سكر الدم ليست مفهومة تمامًا. ومع ذلك ، تشير الدراسات الوبائية إلى زيادة خطر حدوث أحداث سلبية مرتبطة بفرط سكر الدم في المرضى الذين عولجوا بمضادات الذهان غير التقليدية المشمولة في هذه الدراسات.
يجب مراقبة المرضى الذين يعانون من تشخيص مؤكد لمرض السكري الذين بدأوا في تناول مضادات الذهان غير التقليدية بانتظام لتفاقم السيطرة على الجلوكوز. المرضى الذين يعانون من عوامل الخطر لمرض السكري (على سبيل المثال ، السمنة ، والتاريخ العائلي لمرض السكري) الذين يبدأون العلاج مع يجب أن تخضع مضادات الذهان غير التقليدية لاختبار السكر في الدم في بداية العلاج وخلال فترة العلاج علاج او معاملة. يجب مراقبة أي مريض يعالج بمضادات الذهان غير التقليدية لأعراض ارتفاع السكر في الدم بما في ذلك polydipsia ، polyuria ، polyphagia ، والضعف. المرضى الذين يعانون من أعراض ارتفاع السكر في الدم أثناء العلاج بمضادات الذهان غير التقليدية يجب أن يخضعوا لاختبار صيام لجلوكوز الدم. في بعض الحالات ، تم حل ارتفاع السكر في الدم عندما توقف مضادات الذهان غير التقليدية ؛ ومع ذلك ، فقد تطلب بعض المرضى استمرار العلاج المضاد للسكري على الرغم من التوقف عن تناول الدواء المشتبه به.
ترد في الجدول 1 بيانات من دراسة أجريت على الجرعة الثابتة لمدة 4 أسابيع في الأشخاص البالغين المصابين بالفصام ، والتي تم فيها أخذ عينات من الدم الصائم.
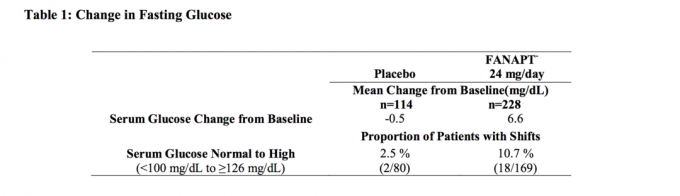
ويرد في الجدول 2 تحليلات مجمعة لبيانات الجلوكوز من الدراسات السريرية بما في ذلك التجارب طويلة الأجل.
عسر شحميات الدم
وقد لوحظت تغييرات غير مرغوب فيها في الدهون في المرضى الذين عولجوا بمضادات الذهان غير التقليدية.
وترد في الجدول 3 بيانات من عشبة ذ ، جرعة ثابتة ، خاضعة للتحكم الوهمي ، لمدة 4 أسابيع ، حيث تم سحب عينات من الدم الصائم ، في الأشخاص البالغين المصابين بمرض انفصام الشخصية.

يرد في الجدول 4 والجدول 5 تحليلات مجمعة لبيانات الكوليسترول والدهون الثلاثية من الدراسات السريرية بما في ذلك التجارب طويلة الأجل.
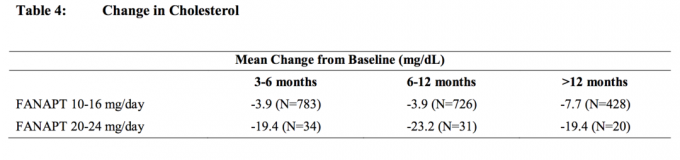
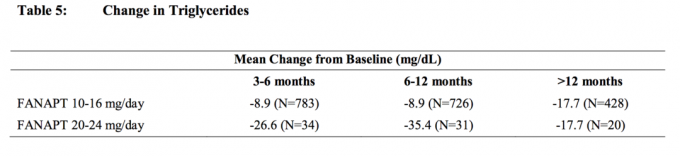
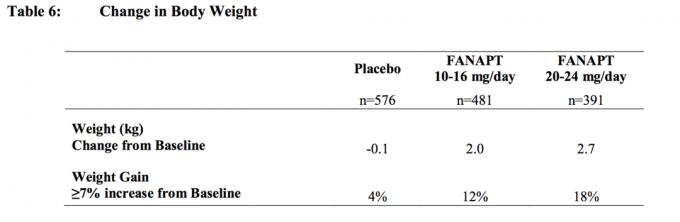
زيادة الوزن
وقد لوحظ زيادة الوزن مع استخدام مضادات الذهان غير التقليدية. ينصح الرصد السريري للوزن.
في جميع الدراسات قصيرة وطويلة الأجل ، كان التغير الإجمالي المتوسط من خط الأساس عند نقطة النهاية 2.1 كجم.
التغيرات في وزن الجسم (كغالعلامة) ونسبة الموضوعات مع زيادة ≥7 ٪ في وزن الجسم من 4 وهمي تسيطر عليها ، 4- أو 6 أسابيع ، يتم تقديم دراسات ثابتة أو مرنة الجرعة في مواضيع الكبار في الجدول 6.
النوبات
في التجارب القصيرة الأجل التي تسيطر عليها وهمي (4- إلى 6 أسابيع) ، وقعت نوبات في 0.1 ٪ (1/1344) من المرضى الذين عولجوا مع FANAPT مقارنة مع 0.3 ٪ (2/587) على الدواء الوهمي. كما هو الحال مع مضادات الذهان الأخرى ، يجب استخدام FANAPT بحذر في المرضى الذين لديهم تاريخ من النوبات أو مع الحالات التي من المحتمل أن تخفض عتبة النوبة. قد تكون الحالات التي تخفض عتبة النوبة أكثر شيوعًا بين سكان يبلغ عمرهم 65 عامًا أو أكبر.
انخفاض ضغط الدم الانتصابي والإغماء
يمكن أن يسبب FANAPT انخفاض ضغط الدم الانتصابي المرتبط بالدوار ، عدم انتظام دقات القلب ، والإغماء. هذا يعكس خصائصها المضادة للهرمونات ألفا 1. في الدراسات قصيرة الأجل التي تسيطر عليها وهمي مزدوجة التعمية ، حيث تم زيادة الجرعة ببطء ، على النحو الموصى به أعلاه ، تم الإبلاغ عن إغماء في 0.4 ٪ (5/1344) من المرضى الذين عولجوا مع FANAPT ، مقارنة مع 0.2 ٪ (1/587) على الوهمي. تم الإبلاغ عن انخفاض ضغط الدم الانتصابي في 5 ٪ من المرضى الذين تلقوا 20-24 ملغ / يوم ، 3 ٪ من المرضى الذين تلقوا 10-16 ملغ / يوم ، و 1 ٪ من المرضى الذين تناولوا الدواء الوهمي. من المتوقع أن يزيد معدل المعايرة السريعة من انخفاض ضغط الدم الانتصابي والإغماء.
يجب استخدام FANAPT بحذر في المرضى الذين يعانون من أمراض القلب والأوعية الدموية المعروفة (على سبيل المثال ، قصور القلب ، تاريخ احتشاء عضلة القلب ، نقص التروية ، أو التوصيل تشوهات) ، أو أمراض الدماغ الوعائية ، أو الحالات التي تهيئ المريض لخفض ضغط الدم (الجفاف ، نقص حجم الدم ، والعلاج مع ارتفاع ضغط الدم الأدوية). ينبغي النظر في رصد العلامات الحيوية الانتصابية في المرضى الذين يعانون من انخفاض ضغط الدم.
نقص الكريات البيض ، قلة العدلات ونبات المحببات
في التجارب السريرية وتجربة ما بعد التسويق ، تم الإبلاغ عن أحداث قلة الكريات البيض / قلة العدلات ذات الصلة مؤقتًا بالعوامل المضادة للذهان. ندرة المحببات (بما في ذلك الحالات المميتة) تم الإبلاغ عنها أيضًا.
تشتمل عوامل الخطر المحتملة لنقص الكريات البيض / قلة العدلات على عدد خلايا الدم البيضاء المنخفض مسبقًا وتاريخ قلة الكريات البيض / قلة العدلات الناجم عن المخدرات. المرضى الذين يعانون من نقص الكريات البيض المنخفض مسبقًا أو لديهم تاريخ من نقص الكريات البيض / قلة العدلات الناجم عن المخدرات يجب أن يخضعوا لمراقبة تعداد الدم الكامل (CBC) في كثير من الأحيان خلال الأشهر القليلة الأولى من العلاج ويجب التوقف عن FANAPT في أول علامة على انخفاض في WBC في غياب مسببات أخرى العوامل.
يجب مراقبة المرضى الذين يعانون من قلة العدلات بعناية لمعرفة الحمى أو غيرها من الأعراض أو علامات العدوى ومعالجتها على الفور في حالة حدوث هذه الأعراض أو الأعراض. يجب على المرضى الذين يعانون من قلة العدلات الوخيمة (عدد العدلات المطلق <1000 / مم 3) التوقف عن FANAPT ومتابعة WBC الخاص بهم حتى الشفاء.
فرط برولاكتين الدم
كما هو الحال مع الأدوية الأخرى التي تستعد لمستقبلات الدوبامين D2 ، فإن FANAPT يرفع مستويات البرولاكتين.
فرط برولاكتين الدم قد يثبط GnRH المهاد ، مما يؤدي إلى انخفاض إفراز الغدد التناسلية في الغدة النخامية. هذا ، بدوره ، قد تمنع وظيفة الإنجابية عن طريق إضطراب تكوين الغدد التناسلية السكرية في كل من المرضى من الإناث والذكور. تم الابلاغ عن وجود الجراثيم ، انقطاع الطمث ، التثدي ، والعجز مع المركبات المرتفعة للبرولاكتين. قد يؤدي فرط برولاكتين الدم طويل الأمد عندما يرتبط بقصور الغدد التناسلية إلى انخفاض كثافة العظام لدى كل من المرضى من الإناث والذكور.
تشير تجارب زراعة الأنسجة إلى أن حوالي ثلث سرطانات الثدي البشرية تعتمد على البرولاكتين في المختبر ، أ عامل ذو أهمية محتملة إذا تم التفكير في وصفة هذه الأدوية في مريض مصاب بالثدي المكتشف مسبقًا سرطان. شوهدت تغييرات تكاثري الغدة الثديية والزيادات في مصل البرولاكتين في الفئران والجرذان التي عولجت باستخدام FANAPT. لا الدراسات السريرية ولا الدراسات الوبائية التي أجريت حتى الآن أظهرت وجود علاقة بين الإدارة المزمنة لهذه الفئة من الأدوية والأورام السرطانية لدى البشر ؛ تعتبر الأدلة المتاحة محدودة للغاية بحيث لا تكون حاسمة في هذا الوقت.
في تجربة قصيرة الأجل يتم التحكم فيها بالعلاج الوهمي (4 أسابيع) ، يعني التغير المتوسط من خط الأساس إلى نقطة النهاية في مستويات هرمون البرولاكتين في البلازما بالنسبة لمجموعة FANAPT 24 ملغ / يوم المعالجة اليومية كانت زيادة قدرها 2.6 نانوغرام / مل مقارنة بانخفاض قدره 6.3 نانوغرام / مل في همي-المجموعة. في هذه التجربة ، لوحظ ارتفاع مستويات البرولاكتين في البلازما في 26 ٪ من البالغين الذين عولجوا بـ FANAPT مقارنة بـ 12 ٪ في المجموعة الثانية. في التجارب قصيرة المدى ، ارتبط FANAPT بمستويات متواضعة من ارتفاع البرولاكتين مقارنة بارتفاع البرولاكتين المرتفع الذي لوحظ مع بعض العوامل المضادة للذهان الأخرى. في التحليل المجمع من الدراسات السريرية بما في ذلك التجارب على المدى الطويل ، في 3210 من البالغين الذين عولجوا بآيلوبيريدون ، تم الإبلاغ عن التثدي في شخصين ذكور (0.1 ٪) مقارنة مع 0 ٪ في المرضى الذين عولجوا بالعلاج الوهمي ، وتم الإبلاغ عن وجود الجرة في 8 موضوعات إناث (0.2 ٪) مقارنة ب 3 موضوعات إناث (0.5 ٪) في العلاج المموه المرضى.
تنظيم درجة حرارة الجسم
يعزى اضطراب قدرة الجسم على خفض درجة حرارة الجسم الأساسية إلى عوامل مضادة للذهان. ينصح الرعاية المناسبة عند وصف FANAPT للمرضى الذين سوف يعانون من الظروف التي قد تسهم في ارتفاع الجسم الأساسي درجة الحرارة ، على سبيل المثال ، ممارسة التمارين الرياضية بقوة ، والتعرض للحرارة الشديدة ، وتلقي الأدوية المصاحبة للنشاط المضاد للكولين ، أو التعرض ل تجفيف.
عسر البلع
ارتبط عدم القدرة على المريء والطموح مع تعاطي المخدرات المضادة للذهان. الالتهاب الرئوي الطموح هو سبب شائع للمراضة والوفيات في المرضى المسنين. يجب استخدام FANAPT والأدوية المضادة للذهان الأخرى بحذر في المرضى المعرضين لخطر الإصابة بالتهاب رئوي طموح.
انتحار
إن إمكانية محاولة الانتحار متأصلة في مرض ذهاني ، ويجب أن ترافق الإشراف عن كثب للمرضى المعرضين لخطر كبير العلاج الدوائي. يجب كتابة وصفات FANAPT لأصغر كمية من الأقراص بما يتوافق مع الإدارة الجيدة للمريض من أجل الحد من خطر الجرعة الزائدة.
قساح
تم الإبلاغ عن ثلاث حالات من priapism في برنامج FANAPT قبل التسويق. تم الإبلاغ عن العقاقير ذات تأثيرات حصر ألفا الأدرينالية للحث على الإصابة بمرض السرطان. يشارك FANAPT هذا النشاط الدوائي. قد تتطلب priapism شديدة التدخل الجراحي.
المحتملة للإعاقة المعرفية والحركية
FANAPT ، مثل مضادات الذهان الأخرى ، لديه القدرة على إضعاف الحكم أو التفكير أو المهارات الحركية. في المدى القصير ، التجارب التي تسيطر عليها وهمي ، تم الإبلاغ عن نعاس (بما في ذلك التخدير) في 11.9 ٪ (104/874) من المرضى البالغين الذين عولجوا بـ FANAPT بجرعات 10 ملغ / يوم أو أكثر مقابل 5.3 ٪ (31/587) الذين عولجوا الوهمي. يجب توخي الحذر عند تشغيل الآلات الخطرة ، بما في ذلك السيارات ، حتى يتأكدوا بشكل معقول من أن العلاج باستخدام FANAPT لا يؤثر عليهم سلبًا.
أعلى
ردود الفعل السلبية
تجربة الدراسات السريرية
لأن التجارب السريرية تجرى في ظل ظروف متباينة على نطاق واسع ، لوحظت معدلات رد فعل سلبية في التجربة السريرية للدواء لا يمكن مقارنتها مباشرة بالمعدلات في التجارب السريرية لعقار آخر وقد لا تعكس المعدلات التي لوحظت في التجارب السريرية ممارسة. المعلومات الواردة أدناه مستمدة من قاعدة بيانات التجارب السريرية لـ FANAPT التي تتكون من 3229 مريضًا يتعرضون لـ FANAPT بجرعات 10 ملغ / يوم أو أكثر ، لعلاج انفصام الشخصية. من بين هؤلاء ، تلقى 999 FANAPT لمدة 6 أشهر على الأقل ، مع 657 تعرضوا لـ FANAPT لمدة 12 شهرًا على الأقل. كان كل هؤلاء المرضى الذين تلقوا FANAPT يشاركون في تجارب سريرية متعددة الجرعات. تباينت ظروف ومدة العلاج مع FANAPT إلى حد كبير وشملت (في فئات متداخلة) ، التسمية المفتوحة و مراحل الدراسات مزدوجة التعمية ، المرضى الداخليين والخارجيين ، دراسات الجرعة الثابتة والجرعة المرنة ، دراسات قصيرة الأجل وطويلة الأجل مكشوف.
المعلومات الواردة في هذه الأقسام مستمدة من بيانات مجمعة من 4 دواء وهمي ، 4 أو 6 أسابيع ، دراسات جرعة ثابتة أو مرنة في المرضى الذين تلقوا FANAPT بجرعات يومية في حدود 10 إلى 24 ملغ (ن = 874).
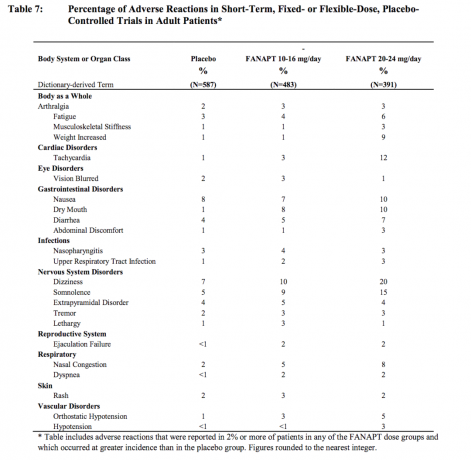
ردود الفعل السلبية التي تحدث بنسبة 2 ٪ أو أكثر بين المرضى الذين عولجوا من FANAPT وأكثر تواترا من العلاج الوهمي
الجدول 7 يعدد الحوادث المجمعة من ردود الفعل السلبية التي تم الإبلاغ عنها تلقائيا في أربعة وهمي تسيطر عليها ، 4 أو 6 أسابيع ، دراسات الجرعة الثابتة أو المرنة ، تدرج ردود الفعل التي حدثت في 2٪ أو أكثر من المرضى الذين عولجوا بـ FANAPT في أي من الجرعة المجموعات ، والتي كانت نسبة حدوثها في المرضى الذين عولجوا من قبل FANAPT في أي مجموعة جرعة أكبر من الإصابة في المرضى الذين عولجوا الوهمي.
ردود الفعل السلبية المتعلقة بالجرعة في التجارب السريرية
استنادًا إلى البيانات المجمعة من 4 دراسات بالجرعات الوهمية أو من 4 إلى 6 أسابيع أو ثابتة أو مرنة ، فإن التفاعلات الضارة التي حدثت مع أكثر من 2٪ الإصابة في المرضى الذين عولجوا بواسطة FANAPT ، والتي كانت نسبة الإصابة بها في المرضى الذين عولجوا بـ FANAPT 20-24 ملغ / يوم ضعف معدل الإصابة في المرضى الذين عولجوا بـ FANAPT 10-16 ملغ / يوم كانوا: عدم الراحة في البطن ، الدوار ، انخفاض ضغط الدم ، تصلب العضلات والعظام ، عدم انتظام دقات القلب ، والوزن زيادة.
ردود الفعل السلبية والمخدرات ذات الصلة في التجارب السريرية
استنادًا إلى البيانات المجمّعة من 4 دراسات ذات جرعات ثابتة أو بأربعة أو ستة أسابيع من جرعات الدواء الوهمي أو الوهمي أو المرن ، حدثت ردود الفعل السلبية التالية في حالات ≥ 5٪ في المرضى الذين عولجوا مع FANAPT وعلى الأقل ضعفي الدواء الوهمي لجرعة واحدة على الأقل: الدوخة ، جفاف الفم ، التعب ، احتقان الأنف ، النعاس ، عدم انتظام دقات القلب ، انخفاض ضغط الدم الانتصابي ، والوزن زيادة. كانت الدوخة ، عدم انتظام دقات القلب ، والوزن زيادة شائعة على الأقل في 20-24 ملغ / يوم في 10-16 ملغ / يوم.
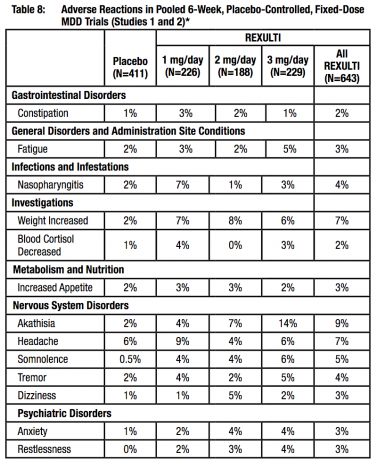
الأعراض خارج الهرمية (EPS) في التجارب السريرية
قدمت بيانات مجمعة من الدراسات 4 الجرعة التي تسيطر عليها وهمي ، أو 4- أو 6- أسابيع ، جرعة ثابتة أو مرنة معلومات حول EPS. أظهرت بيانات الأحداث السلبية التي تم جمعها من تلك التجارب المعدلات التالية للأحداث السلبية المرتبطة بـ EPS كما هو موضح في الجدول 8.
ردود الفعل السلبية المرتبطة بوقف العلاج في التجارب السريرية
استنادًا إلى البيانات المجمّعة من 4 دراسات جرعات تسيطر عليها وهمي أو 4 أو 6 أسابيع أو ثابتة أو مرنة ، لم يكن هناك الاختلاف في حدوث الإيقاف بسبب الأحداث الضائرة بين علاج FANAPT (5٪) والعلاج الوهمي (5٪) المرضى. كانت أنواع الأحداث السلبية التي أدت إلى وقف مماثلة لمرضى FANAPT- وهمي.
الاختلافات الديموغرافية في ردود الفعل السلبية في التجارب السريرية
فحص مجموعات فرعية من السكان في 4 همي تسيطر عليها ، 4- أو 6 أسابيع ، ثابت أو دراسات الجرعة المرنة لم تكشف عن أي دليل على وجود اختلافات في السلامة على أساس العمر ، الجنس أو العرق.
تشوهات الاختبارات المعملية في التجارب السريرية
لم تكن هناك فروق بين FANAPT وهمي في حالات التوقف بسبب التغيرات في أمراض الدم ، تحليل البول ، أو كيمياء المصل.
في التجارب القصيرة الأجل التي تسيطر عليها وهمي (4- إلى 6 أسابيع) ، كان هناك 1.0 ٪ (13/1342) المرضى الذين عولجوا إيلوبيريدون مع الهيماتوكريت مرة واحدة على الأقل أقل من المعدل الطبيعي الممتد أثناء العلاج بعد التوزيع العشوائي ، مقارنة بـ 0.3٪ (2/585) في الوهمي. تم تعريف المدى الطبيعي الممتد للهيماتوكريت المنخفض في كل تجربة من هذه التجارب على أنها القيمة 15٪ أقل من المعدل الطبيعي للمختبر المركزي الذي تم استخدامه في التجربة.
ردود الفعل الأخرى خلال تقييم ما قبل التسويق من FANAPT
فيما يلي قائمة بمصطلحات MedDRA التي تعكس ردود الفعل السلبية في المرضى الذين عولجوا باستخدام FANAPT في جرعات متعددة ≥ 4 ملغ / يوم خلال أي مرحلة من التجربة مع قاعدة بيانات 3210 FANAPT المعالجة المرضى. يتم تضمين جميع ردود الفعل المبلغ عنها باستثناء تلك المدرجة بالفعل في الجدول 7 ، أو أجزاء أخرى من ردود الفعل السلبية (6) ، تلك التي تم النظر فيها في التحذيرات والاحتياطات (5) ، مصطلحات التفاعل تلك التي كانت عامة لدرجة أنها غير معلوماتية ، تم الإبلاغ عن ردود الفعل في أقل من 3 مرضى والتي لم تكن خطيرة ولا تهدد الحياة ، ردود الفعل التي هي شائعة خلاف ذلك مثل ردود الفعل الخلفية ، وردود الفعل التي من غير المرجح أن تكون دواء ذات صلة.
يتم تصنيف التفاعلات بشكل أكبر بواسطة فئة الجهاز لنظام MedDRA ويتم سردها من أجل تقليل التردد وفقًا لما يلي التعاريف: الأحداث السلبية المتكررة هي تلك التي تحدث في ما لا يقل عن 1/100 مريض (فقط تلك غير المدرجة في الجدول 7 تظهر في هذا قائمة)؛ ردود الفعل السلبية النادرة هي تلك التي تحدث في 1/100 إلى 1/1000 مريض ؛ الأحداث النادرة هي تلك التي تحدث في أقل من 1/1000 مريض.
اضطرابات الدم والليمفاوية: نادرة - فقر الدم ، فقر الدم بسبب نقص الحديد ؛ النادرة الكريات البيض
اضطرابات القلب: كثرة الخفقان. نادر - عدم انتظام ضربات القلب ، كتلة الأذيني البطيني من الدرجة الأولى ، فشل القلب (بما في ذلك الاحتقاني والحاد)
اضطرابات الأذن والمتاهة: نادرة -النفس ، طنين الأذن
اضطرابات الغدد الصماء: نادرة - قصور الغدة الدرقية
اضطرابات العين: التهاب الملتحمة المتكرر (بما في ذلك الحساسية) ؛ نادر - جفاف العين ، التهاب الجفن ، وذمة الجفن ، تورم العين ، عتامة عدسي ، إعتام عدسة العين ، فرط الدم (بما في ذلك الملتحمة)
اضطرابات الجهاز الهضمي: نادرة - التهاب المعدة ، فرط إفراز اللعاب ، سلس البراز ، تقرح الفم ؛ نادر - التهاب الفم القلاعي ، قرحة الاثني عشر ، فتق الحجاب الحاجز ، فرط الكلور ، تقرح الشفاه ، التهاب المريء الارتجاعي ، التهاب الفم
الاضطرابات العامة وظروف الموقع الإداري: نادرة - وذمة (عامة ، تأليب ، بسبب أمراض القلب) ، صعوبة في المشي والعطش ؛ نادر - ارتفاع الحرارة
اضطرابات الكبد الصفراوية: نادرة - تحص صفراوي
التحقيقات: متكررة: انخفض الوزن. نادرة - الهيموغلوبين انخفض ، زاد عدد العدلات ، الهيماتوكريت انخفض
الأيض واضطرابات التغذية: نادرة - زيادة الشهية ، الجفاف ، نقص بوتاسيوم الدم ، احتباس السوائل
الاضطرابات العضلية الهيكلية واضطرابات الأنسجة: متكررة - ألم عضلي ، تشنجات في العضلات. نادر - صعر
اضطرابات الجهاز العصبي: نادرة ، تشوش الحس ، فرط النشاط الحركي النفسي ، الأرق ، فقدان الذاكرة ، رأرأة. نادر - متلازمة تململ الساقين
الاضطرابات النفسية: متكررة - الأرق ، العدوان ، الوهم ؛ نادرة - العداء ، نقص الرغبة الجنسية ، جنون العظمة ، فقدان الشهية ، حالة الارتباك ، الهوس ، القطط ، تقلب المزاج ، الذعر هجوم ، اضطراب الوسواس القهري ، الشره المرضي العصبي ، الهذيان ، الشلل الدماغي النفسي ، اضطراب التحكم في النبضات ، كبير كآبة
اضطرابات الكلى والمسالك البولية: سلس البول المتكرر. نادرة - عسر البول ، بولاكيا ، سلس البول ، التهاب الكلية. نادر - احتباس البول ، الفشل الكلوي الحاد
الجهاز التناسلي واضطرابات الثدي: ضعف الانتصاب المتكرر. نادرة - ألم الخصية ، انقطاع الطمث ، ألم الثدي ؛ نادر - عدم انتظام الحيض ، التثدي ، الطمث ، النزيف الرحمي ، نزيف ما بعد انقطاع الطمث ، التهاب البروستاتا.
اضطرابات الجهاز التنفسي والصدر و المنصف: نادرة - الرعاف ، الربو ، سيلان الأنف ، احتقان الجيوب الأنفية ، جفاف الأنف. نادر - الحلق الجاف ، متلازمة توقف التنفس أثناء النوم ، ضيق التنفس
تجربة ما بعد التسويق
تم تحديد التفاعلات الضارة التالية أثناء استخدام FANAPT بعد الموافقة عليها: قذف رجعي وردود فعل فرط الحساسية (بما في ذلك الحساسية المفرطة) ؛ وذمة وعائية. ضيق الحلق. تورم البلعوم. تورم في الوجه والشفتين والفم واللسان ؛ الشرى. طفح جلدي. والحكة). نظرًا لأن ردود الفعل هذه تم الإبلاغ عنها طوعًا من مجموعة سكانية ذات حجم غير مؤكد ، فمن غير الممكن تقدير تواترها بشكل موثوق أو إنشاء علاقة سببية بالتعرض للعقاقير.
أعلى
تفاعل الأدوية
بالنظر إلى التأثيرات الأساسية للجهاز العصبي المركزي من FANAPT ، يجب توخي الحذر عند تناوله مع أدوية أخرى ذات تأثير مركزي وكحول. نظرًا لحدوث مستقبلات alpha1 الأدرينالية ، فإن FANAPT لديها القدرة على تعزيز تأثير بعض العوامل الخافضة لضغط الدم.
المحتملة للعقاقير الأخرى التي تؤثر على FANAPT
Iloperidone ليس ركيزة لأنزيمات CYP1A1 أو CYP1A2 أو CYP2A6 أو CYP2B6 أو CYP2C8 أو CYP2C9 أو CYP2C19 أو CYP2C19 أو CYP2E1. هذا يشير إلى أن تفاعل الإيلوبيريدون مع مثبطات أو محفزات هذه الإنزيمات ، أو عوامل أخرى ، مثل التدخين ، أمر غير مرجح. كلا CYP3A4 و CYP2D6 مسؤولان عن أيض الأيلوبيريدون. مثبطات CYP3A4 (على سبيل المثال ، الكيتوكونازول) أو CYP2D6 (على سبيل المثال ، فلوكستين ، باروكستين) يمكن أن تمنع القضاء على إيلوبيريدون وتتسبب في زيادة مستويات الدم.
الكيتوكونازول: شارك في تناول الكيتوكونازول (200 ملغ مرتين يوميًا لمدة 4 أيام) ، وهو مثبط قوي لـ CYP3A4 ، مع جرعة واحدة 3 ملغ من الإيلوبيريدون إلى 19 زاد المتطوعون الأصحاء الذين تتراوح أعمارهم بين 18 و 45 عامًا من المساحة الواقعة تحت منحنى iloperidone وعناصره P88 و P95 بنسبة 57٪ و 55٪ و 35٪ ، على التوالي. يجب تقليل جرعات إيلوبيريدون بمقدار النصف تقريبًا عند تناولها مع الكيتوكونازول أو مثبطات قوية أخرى من CYP3A4 (على سبيل المثال ، إيتراكونازول). لم تتم دراسة مثبطات الضعف (مثل الإريثروميسين وعصير الجريب فروت). عندما يتم سحب مثبط CYP3A4 من العلاج المركب ، يجب إعادة جرعة إليوبيريدون إلى المستوى السابق.
فلوكستين: التناول المتزامن للفلوكستين (20 ملغ مرتين يوميًا لمدة 21 يومًا) ، وهو مثبط قوي لـ CYP2D6 ، مع جرعة واحدة 3 ملغ من إيلوبيريدون إلى 23 متطوعًا صحيًا تتراوح أعمارهم بين 29 و 44 عامًا ، الذين تم تصنيفهم على أنهم مستقلبات مكثفة CYP2D6 ، زادوا من AUC للأيلوبيريدون وأيضه P88 ، بحوالي 2 إلى 3 أضعاف ، وقللوا AUC من المستقلب P95 الخاص به بواسطة نصف. يجب تخفيض جرعات إيلوبيريدون بمقدار النصف عند تناولها بالفلوكستين. عند سحب فلوكستين من العلاج المركب ، يجب إعادة جرعة إليوبيريدون إلى المستوى السابق. من المتوقع أن يكون لمثبطات قوية أخرى من CYP2D6 آثار مماثلة وستحتاج إلى تخفيضات مناسبة في الجرعة. عند سحب مثبط CYP2D6 من العلاج المركب ، يمكن عندئذ زيادة جرعة الإيلوبيريدون إلى المستوى السابق.
الباروكستين: التناول المتزامن للباروكستين (20 مغ / يوم لمدة 5-8 أيام) ، وهو مثبط قوي لـ CYP2D6 ، مع جرعات متعددة من الإيلوبيريدون (8 أو 12 ملغ مرتين يوميًا) لمرضى الفصام الذين تتراوح أعمارهم بين 18 و 65 عامًا مما أدى إلى زيادة متوسط تركيزات الذروة في حالة الاستقرار ايلوبيريدون ومستقلبه P88 ، بحوالي 1.6 أضعاف ، وانخفض متوسط تركيزات الذروة في حالة الاستقرار في مستقلبه P95 بواسطة نصف. يجب تخفيض جرعات إيلوبيريدون بمقدار النصف عند تناولها بالباروكستين. عند سحب الباروكستين من العلاج المركب ، يجب إعادة جرعة الإيلوبيريدون إلى المستوى السابق. من المتوقع أن يكون لمثبطات قوية أخرى من CYP2D6 آثار مماثلة وستحتاج إلى تخفيضات مناسبة في الجرعة. عندما يتم سحب مثبط CYP2D6 من العلاج المركب ، يمكن بعد ذلك زيادة جرعة إيلوبيريدون إلى المستويات السابقة.
باروكستين و الكيتوكونازول: التناول المتزامن للباروكستين (20 ملغ مرة واحدة يوميا لمدة 10 أيام) ، مثبط CYP2D6 ، و الكيتوكونازول (200 ملغ مرتين يوميا) مع جرعات متعددة من إيلوبيريدون (8 أو 12 ملغ مرتين يوميا) لمرضى الفصام الذين تتراوح أعمارهم بين 18-65 سنة أسفرت عن 1.4 زيادة أضعاف في تركيزات الحالة المستقرة للأيلوبيريدون وأيض المستحلب P88 وانخفاض 1.4 مرة في P95 في وجود الباروكستين. لذا فإن إعطاء iloperidone مع مثبطات كل من مساراته الأيضية لا يضيف إلى تأثير أي مثبط يعطى بمفرده. لذلك ينبغي تخفيض جرعات إيلوبيريدون بمقدار النصف تقريبًا في حالة إعطائها في نفس الوقت مع مثبط CYP2D6 و CYP3A4.
إمكانية FANAPT للتأثير على المخدرات الأخرى
في الدراسات المختبرية في ميكروسومات الكبد البشري أظهرت أن الإيلوبيريدون لا يمنع بشكل كبير عملية التمثيل الغذائي لل يتم استقلاب الأدوية عن طريق أيزيمات السيتوكروم P450 التالية: CYP1A1 ، CYP1A2 ، CYP2A6 ، CYP2B6 ، CYP2C8 ، CYP2C9 ، أو CYP2E1. علاوة على ذلك ، أظهرت الدراسات المختبرية في ميكروسومات الكبد البشري أن الإيلوبيريدون لا يحتوي على الإنزيم الخواص ، خاصةً لأنزيمات السيتوكروم P450 التالية: CYP1A2 ، CYP2C8 ، CYP2C9 ، CYP2C19 ، CYP3A4 و CYP3A5.
Dextromethorphan: أظهرت دراسة أجريت على متطوعين أصحاء أن التغييرات في الحرائك الدوائية لل dextromethorphan (جرعة 80 ملغ) عند جرعة 3 ملغ من تمت مشاركة إيلوبيريدون بشكل مشترك ، مما أدى إلى زيادة بنسبة 17٪ في إجمالي التعرض وزيادة بنسبة 26٪ في التركيزات القصوى للبلازما C بحد أقصى دإكسترومثورفن. وبالتالي ، فإن التفاعل بين iloperidone وغيرها من ركائز CYP2D6 أمر غير مرجح.
فلوكستين: لم يكن لجرعة واحدة من 3 ملغ من إيلوبيريدون أي تأثير على الحرائك الدوائية للفلوكستين (20 ملغ مرتين يوميًا).
ميدازولام (ركيزة CYP 3A4 الحساسة): أظهرت دراسة أجريت على مرضى الفصام زيادة أقل من 50 ٪ في إجمالي ميدازولام التعرض في حالة ثبات إيلوبيريدون (14 يومًا من الجرعات عن طريق الفم بحد أقصى 10 ملغ إيلوبيريدون مرتين يوميًا) وليس له تأثير على الميدازولام C كحد أقصى. وبالتالي ، فإن التفاعل بين iloperidone وغيرها من ركائز CYP3A4 أمر غير مرجح.
الأدوية التي تطيل فترة كيو تي لا ينبغي أن تستخدم FANAPT مع أي أدوية أخرى تطيل فترة كيو تي.
أعلى
استخدام في السكان محددة
سجل التعرض للحمل
يوجد سجل لتعرض الحمل يراقب نتائج الحمل لدى النساء المعرضات لـ FANAPT أثناء الحمل. لمزيد من المعلومات ، اتصل بالسجل الوطني للحمل لمضادات الذهان غير التقليدية على الرقم 1-866-961-2388 أو تفضل بزيارة http://womensmentalhealth.org/clinical-and برامج--research / pregnancyregistry /.
ملخص المخاطر
الأطفال حديثي الولادة الذين تتعرض أمهاتهم لعقاقير مضادة للذهان ، بما في ذلك FANAPT ، خلال الأشهر الثلاثة الثالثة من الحمل معرضون لخطر أعراض خارج هرمية و / أو انسحاب بعد الولادة. البيانات المحدودة المتاحة مع FANAPT في النساء الحوامل ليست كافية لإبلاغ المخاطر المرتبطة بالمخدرات عن العيوب الخلقية الرئيسية والإجهاض. لم يكن إيلوبيريدون ماسخًا عند إعطائه عن طريق الفم للفئران الحامل أثناء تكوين الأعضاء بجرعات تصل إلى 26 ضعفًا للجرعة البشرية الموصى بها البالغة 24 ملغ / يوم على أساس ملغم / متر مربع. ومع ذلك ، فإنه يطيل مدة الحمل والولادة ، ويزيد الولادات ، والوفيات المبكرة داخل الرحم ، وزيادة حالات التأخر في النمو ، وانخفاض بقاء الجرو بعد الولادة. لم يكن إيلوبيريدون ماسخًا عند إعطائه عن طريق الفم للأرانب الحوامل أثناء تكوين الأعضاء عند جرعات تصل إلى 20 مرة من MRHD على أساس mg / m2. ومع ذلك ، فقد زاد الوفيات المبكرة داخل الرحم وقلل من صلاحية الجنين على المدى عند أعلى جرعة والتي كانت أيضًا جرعة سامة للأم.
خطر الخلفية من العيوب الخلقية الرئيسية والإجهاض للسكان المشار إليه غير معروف. في عامة السكان في الولايات المتحدة ، يبلغ الخطر الأساسي المقدّر للتشوهات الخلقية والإجهاض في حالات الحمل المعترف بها سريريًا 2-4٪ و 15-20٪ على التوالي.
اعتبارات سريرية
ردود الفعل السلبية للجنين / حديثي الولادة
أعراض خارج هرمية و / أو أعراض انسحاب ، بما في ذلك التحريض وفرط التوتر ونقص التوتر والهدوء والنعاس وضيق التنفس تم الإبلاغ عن اضطراب التغذية عند الولدان الذين تعرضت أمهاتهم للعقاقير المضادة للذهان خلال الثلث الثالث من حمل. وقد تباينت هذه الأعراض في شدتها. تعافى بعض الولدان خلال ساعات أو أيام دون علاج محدد ؛ البعض الآخر يتطلب العلاج لفترات طويلة. رصد حديثي الولادة لأعراض خارج هرمية و / أو الانسحاب وإدارة الأعراض بشكل مناسب.
البيانات
بيانات الحيوانات
في دراسة حول تطور الجنين ، تم إعطاء الفئران الحامل 4 أو 16 أو 64 ملغ / كغ / يوم (1.6 ، 6.5 ، و 26 مرة من الجرعة البشرية الموصى بها (MRHD) القصوى من 24 ملغ / يوم على أساس ملغ / م 2) من الإيلوبيريدون عن طريق الفم خلال فترة توالد. تسببت أعلى جرعة في زيادة الوفيات داخل الرحم ، وانخفاض وزن الجنين وطوله ، انخفاض تعظم الهيكل العظمي الجنين ، وزيادة حالات الشذوذ الهيكل العظمي طفيفة الجنين و الاختلافات. تسببت هذه الجرعة أيضًا في انخفاض استهلاك طعام الأم وزيادة الوزن.
في دراسة حول تطور الجنين ، أعطيت الأرانب الحوامل 4 أو 10 أو 25 مغ / كغ / يوم (3 ، 8 ، و 20 مرة من MRHD على أساس ملغم / م 2) من الإيلوبيريدون خلال فترة التولد العضوي. تسببت أعلى جرعة في زيادة الوفيات المبكرة داخل الرحم وانخفاض صلاحية الجنين على المدى ؛ تسببت هذه الجرعة أيضا سمية الأمهات.
في الدراسات الإضافية التي أعطيت فيها الفئران إيلوبيريدون بجرعات مماثلة لما سبق أعلاه من الحمل أو من اليوم 17 من الحمل والاستمرار في الفطام ، وشملت الآثار التناسلية الضارة الحمل لفترة طويلة والولادة ، وزيادة معدلات الإملاص ، وزيادة حدوث الاختلافات الحشوية في الجنين ، وانخفاض أوزان الجنين والجرو ، وانخفاض الجرو بعد الولادة نجاة. لم تكن هناك آثار المخدرات على تطور السلوك العصبي أو الإنجابية من الجراء الباقين على قيد الحياة. تراوحت جرعات عدم التأثير من 4 إلى 12 مغ / كغ باستثناء الزيادة في معدلات الإملاص التي حدثت عند أقل جرعة تم اختبارها من 4 ملغ / كغ ، أي 1.6 مرة من MRHD على أساس ملغم / م 2. شوهد سمية الأمهات عند تناول جرعات أعلى في هذه الدراسات.
مستقلب iloperidone P95 ، وهو مستقلب رئيسي متداول من iloperidone في البشر ولكنه غير موجود في كميات كبيرة في الفئران ، أعطيت للفئران الحوامل خلال فترة التولد العضوي بجرعات عن طريق الفم من 20 ، 80 ، أو 200 ملغ كغ / يوم. لم يلاحظ أي آثار ماسخة. حدث تأخر الهيكل العظمي في جميع الجرعات. لم يتم إنتاج سمية الأم كبيرة. كانت مستويات البلازما لـ P95 (AUC) عند أعلى جرعة تم اختبارها هي تلك التي لدى البشر الذين يتلقون MRHD من iloperidone.
الرضاعة
ملخص المخاطر
لا توجد معلومات بخصوص وجود الإيلوبيريدون أو مستقلباته في حليب الإنسان آثار ايلوبيريدون على الطفل الذي يرضع ، ولا آثار ايلوبيريدون على حليب الإنسان إنتاج. ايلوبيريدون موجود في حليب الفئران. بسبب احتمالية حدوث ردود فعل سلبية خطيرة عند الرضع الذين يرضعون رضاعة طبيعية ، ننصح المرأة بعدم الإرضاع من الثدي أثناء العلاج باستخدام FANAPT.
البيانات: تم فحص انتقال النشاط الإشعاعي إلى لبن الفئران المرضعة بعد جرعة واحدة من [14C] إيلوبيريدون عند 5 مجم / كجم. كان تركيز النشاط الإشعاعي في الحليب بعد 4 ساعات من الجرعة أكبر بنحو 10 أضعاف من تركيزه في البلازما في نفس الوقت. ومع ذلك ، خلال 24 ساعة بعد الجرعات ، انخفضت تركيزات النشاط الإشعاعي في الحليب إلى قيم أقل قليلاً من البلازما. كانت صورة التمثيل الغذائي في الحليب مماثلة من الناحية النوعية في البلازما.
استخدام الأطفال لم تثبت سلامة وفعالية مرضى الأطفال والمراهقين.
استخدام المسنين
لم الدراسات السريرية لل FANAPT في علاج مرض انفصام الشخصية لا تشمل أعداد كافية من المرضى الذين تبلغ أعمارهم 65 عامًا أو أكثر لتحديد ما إذا كانوا يستجيبون بشكل مختلف عن البالغين الأصغر أم لا المرضى. من بين 3210 مريضًا عولجوا بـ FANAPT في تجارب ما قبل التسويق ، كان 25 (0.5٪) يبلغون 65 عامًا ولم يكن هناك مرضى تبلغ أعمارهم 75 عامًا.
المرضى المسنون المصابون بذهان متعلق بالخرف ويعالجون بـ FANAPT معرضون لخطر متزايد للوفاة مقارنةً بالعلاج الوهمي. لم تتم الموافقة على FANAPT لعلاج المرضى الذين يعانون من الذهان المرتبط بالخرف.
القصور الكلوي
لأن FANAPT مستقلب للغاية ، مع أقل من 1 ٪ من الدواء يفرز دون تغيير ، من غير المحتمل أن يكون لضعف الكلى وحده تأثير كبير على الحرائك الدوائية لـ FANAPT. كان لضعف الكلى (تصفية الكرياتينين أقل من 30 مل / دقيقة) تأثير ضئيل على Cmax من الإيلوبيريدون (يعطى في جرعة واحدة من 3 ملغ) وعناصره الأيضية P88 و P95 في أي من التحليلات الثلاث المقاسة. تمت زيادة AUC0– by بنسبة 24٪ ، وانخفضت بنسبة 6٪ ، وزادت بنسبة 52٪ للأيلوبيريدون ، P88 و P95 ، على التوالي ، في الأشخاص الذين يعانون من اختلال كلوي.
اختلال كبدي
ليس هناك حاجة لتعديل جرعة FANAPT في المرضى الذين يعانون من اختلال كبدي خفيف. المرضى الذين يعانون من اختلال كبدي معتدل قد تتطلب تخفيض الجرعة. لا ينصح FANAPT للمرضى الذين يعانون من اختلال كبدي حاد.
في الأشخاص البالغين الذين يعانون من اختلال كبدي خفيف ، لم يلاحظ أي فارق ذو صلة في الحرائك الدوائية من إيلوبيريدون ، P88 أو P95 (كليًا أو غير ملزم) مقارنةً بضوابط البالغين الأصحاء. في الأشخاص الذين يعانون من اختلال كبدي معتدل ، كان التعرض الحر أكبر (2 أضعاف) ومتغير أكثر للأيضات النشطة P88 لوحظت مقارنة مع الضوابط الصحية ، في حين كان التعرض للأيلوبيريدون و P95 متشابهين بشكل عام (تغير أقل من 50 ٪ مقارنة مع مراقبة). نظرًا لعدم إجراء دراسة على الأشخاص المصابين بضعف حاد في الكبد ، لا ينصح باستخدام FANAPT للمرضى الذين يعانون من اختلال كبدي حاد.
حالة التدخين
استنادًا إلى الدراسات المختبرية التي تستخدم إنزيمات الكبد البشري ، لا يعد FANAPT ركيزة لـ CYP1A2 ؛ لذلك يجب ألا يكون للتدخين تأثير على الحرائك الدوائية لـ FANAPT.
حمل
أعلى
تعاطي المخدرات والاعتماد عليها
المواد الخاضعة للرقابة
FANAPT ليست مادة خاضعة للرقابة.
إساءة
لم تتم دراسة FANAPT بشكل منهجي في الحيوانات أو البشر لاحتمال تعرضها للإيذاء أو التسامح أو الاعتماد الجسدي. في حين أن التجارب السريرية لم تكشف عن أي اتجاه للسلوك الباحث عن المخدرات ، فإن هذه الملاحظات لم تكن منهجية وغير ممكنة للتنبؤ على أساس هذه التجربة ، إلى أي مدى سيتم إساءة استخدام دواء CNS نشط ، FANAPT ، و / أو تحويله و / أو إساءة استخدامه مرة واحدة تسويقها. وبالتالي ، يجب تقييم المرضى بعناية لمعرفة تاريخ تعاطي المخدرات ، ويجب أن يتم تقييم هؤلاء المرضى لوحظ عن كثب بحثًا عن علامات سوء استخدام أو إساءة استخدام FANAPT (مثل تطور التسامح ، والزيادات في الجرعة ، والبحث عن المخدرات سلوك).
أعلى
جرعة زائدة
التجربة الإنسانية
في تجارب ما قبل التسويق التي شملت أكثر من 3210 مريض ، كانت جرعة زائدة عرضية أو متعمدة من FANAPT موثقة في 8 مرضى تتراوح بين 48 ملغ إلى 576 ملغ تؤخذ في وقت واحد و 292 ملغ تؤخذ على مدى 3 أيام فترة. ولم يتم الإبلاغ عن أي وفيات من هذه الحالات. وكان أكبر تناول واحد مؤكد من FANAPT 576 ملغ. لم يلاحظ أي آثار جسدية ضارة لهذا المريض. كان التناول الأكبر التالي المؤكد لـ FANAPT هو 438 مجم خلال فترة 4 أيام ؛ تم الإبلاغ عن أعراض خارج هرمية وفاصل QTc من 507 مللي ثانية لهذا المريض مع أي عقابيل القلب. استأنف هذا المريض علاج FANAPT لمدة 11 شهرًا إضافيًا.
بشكل عام ، كانت العلامات والأعراض المبلغ عنها هي تلك الناتجة عن المبالغة في التأثيرات الدوائية المعروفة (على سبيل المثال ، النعاس والتخدير ، عدم انتظام دقات القلب ، انخفاض ضغط الدم) من FANAPT.
إدارة الجرعة الزائدة
لا يوجد ترياق محدد لـ FANAPT. لذلك ينبغي اتخاذ تدابير داعمة مناسبة. في حالة الجرعة الزائدة الحادة ، يجب على الطبيب إنشاء مجرى الهواء والحفاظ عليه وضمان الأوكسجين والتهوية الكافيين. غسل المعدة (بعد التنبيب ، إذا كان المريض فاقدًا للوعي) ، وينبغي الأخذ في الاعتبار إدارة الفحم المنشط مع ملين. قد تؤدي احتمالية حدوث تطويق أو نوبات أو رد فعل ضعيف في الرأس والرقبة بعد تناول جرعة زائدة إلى خطر الطموح عن طريق التقيؤ المستحث. يجب أن تبدأ مراقبة القلب والأوعية الدموية على الفور ويجب أن تشمل مراقبة ECG المستمرة للكشف عن عدم انتظام ضربات القلب المحتملة. إذا تم إعطاء علاج مضاد لاضطراب النظم ، فلا ينبغي استخدام الديسوبراميد والبروكيناميد والكينيدين ، لأن لديهم إمكانية لإطالة آثار كيو تي التي قد تكون مضافة لآثار FANAPT. وبالمثل ، من المعقول توقع أن تكون خصائص حجب ألفا لـ bretylium مضافة إلى خصائص FANAPT ، مما يؤدي إلى انخفاض ضغط الدم المشكل. يجب معالجة انخفاض ضغط الدم والانهيار الدوري بالتدابير المناسبة مثل السوائل الوريدية أو العوامل الودية. (لا ينبغي استخدام الإيبينيفرين والدوبامين ، لأن تحفيز بيتا قد يزيد من انخفاض ضغط الدم في وضع ألفا الناجم عن FANAPT حصار). في حالات الأعراض خارج الهرمية الوخيمة ، يجب إعطاء الدواء المضاد للكولين. يجب أن يستمر الإشراف الطبي الدقيق حتى يتعافى المريض.
أعلى
وصف
FANAPT هو مضادات الذهان غير التقليدية التي تنتمي إلى الفئة الكيميائية لمشتقات بيبيريدينيل - بنزيسوكسازول. اسمها الكيميائي هو 4 '- [3- [4- (6-فلورو -1 ، 1-بنزيوكسازول-3-ييل) بيبيريدينو] بروبوكسي] -3'-ميثوكسي أسيتوفينون. الصيغة الجزيئية لها هي C24H27FN2O4 ووزنها الجزيئي هو 426.48. الصيغة الهيكلية هي:
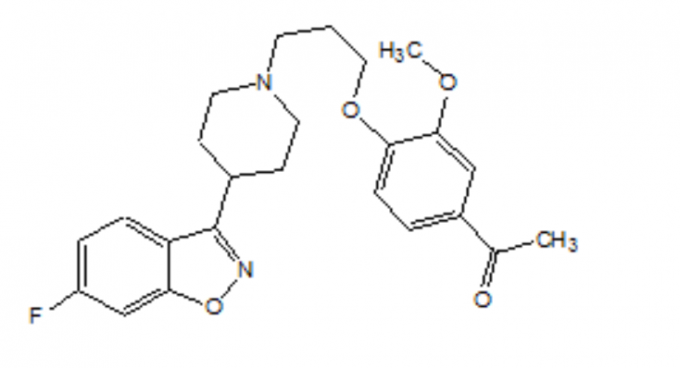
ايلوبيريدون هو مسحوق بلوري أبيض إلى أبيض ناعما. إنه غير قابل للذوبان عملياً في الماء ، قابل للذوبان بشكل طفيف في 0.1 N حمض الهيدروكلوريك وقابل للذوبان بحرية في الكلوروفورم ، الإيثانول ، الميثانول ، والأسيتونيتريل.
أقراص FANAPT مخصصة للإعطاء عن طريق الفم فقط. كل جولة ، غير المصقول
يحتوي القرص على 1 ملغ ، 2 ملغ ، 4 ملغ ، 6 ملغ ، 8 ملغ ، 10 ملغ ، أو 12 ملغ من إيلوبيريدون. المكونات غير النشطة هي: مونوهيدرات اللاكتوز ، السليلوز الجريزوفولفين ، هيدروكسي بروبيل ميثيل السلولوز ، كروسبوفيدون ، ستيرات المغنيزيوم ، السيليكون الغروي
ثاني أكسيد ، والمياه النقية (إزالتها أثناء المعالجة). تكون الأقراص بيضاء ، مستديرة ، مسطحة ، ذات حواف مشطوفة ومحددة بشعار "" تم نقشه على جانب واحد وقوة الكمبيوتر اللوحي "1" ، "2" ، "4" ، "6" ، "8" ، "10" ، أو "12" debossed على الجانب الآخر.
أعلى
علم الصيدلة السريرية
آلية العمل
آلية عمل iloperidone في مرض انفصام الشخصية غير معروف. ومع ذلك ، يمكن التوسط في فعالية الإيلوبيريدون من خلال مزيج من الدوبامين من النوع 2 (D2) والسيروتونين من النوع 2 (5-HT2).
يُشكِّل إيلوبيريدون مستقلبًا نشطًا ، P88 ، وله ملف تعريف ملزم للمستقبلات المختبرية مماثل للعقار الأصل.
الدوائية
يعمل إيلوبيريدون كخصم ذو ارتباط عالي (نانومتر) يرتبط بالسيروتونين 5-HT2A الدوبامين D2 و مستقبلات D3 ، ومستقبلات NEα1 بافراز (قيم Ki تبلغ 5.6 ، 6.3 ، 7.1 ، 0.36 نانومتر ، على التوالي). ايلوبيريدون لديه تقارب معتدل للدوبامين D4 ، ومستقبلات السيروتونين 5-HT6 و 5 -HT7 (قيم كي 25 و 43 و 22 ، نانومتر على التوالي) ، وتقارب منخفض لمستقبلات السيروتونين 5-HT1A ، الدوبامين D1 ، والهستامين H1 (قيم كي من 168 ، 216 و 437 نانومتر ، على التوالي). ايلوبيريدون لا يوجد لديه تقارب ملموس (Ki> 1000 نانومتر) لمستقبلات المسكارين الكوليني. إن تقارب مستقلب iloperidone P88 يساوي عمومًا أو أقل من المركب الأصلي ، بينما المستقلب P95 فقط يظهر تقارب 5-HT2A (قيمة Ki من 3.91) ومستقبلات NEα1A و NEα1B و NEα1D و NEα2C (قيم Ki هي 4.7 و 2.7 و 8.8 و 4.7 nM على التوالي).
الدوائية
العمر النصفي للتخلص من الملحوظ لـ iloperidone و P88 و P95 في المستقلبات المكثفة CYP2D6 (EM) هي 18 و 26 و 23 ساعة على التوالي وفي المستقلبات الضعيفة (PM) هي 33 و 37 و 31 ساعة على التوالي. يتم تحقيق تركيزات الحالة الثابتة خلال 3 - 4 أيام من الجرعات. تراكم الإيلوبيريدون يمكن التنبؤ به من الحرائك الدوائية أحادية الجرعة. الدوائية للأيلوبيريدون أكثر من جرعة متناسبة. يتم التخلص من الإيلوبيريدون بشكل رئيسي من خلال عملية التمثيل الغذائي للكبد والتي تشمل 2 إيزوزيم P450 ، CYP2D6 و CYP3A4.
الامتصاص: يمتص إيلوبيريدون بشكل جيد بعد تناوله للقرص مع تركيزات البلازما القصوى التي تحدث خلال 2 إلى 4 ساعات ؛ في حين أن التوافر الحيوي النسبي لتركيبة الجهاز اللوحي مقارنة بالمحلول الفموي هو 96٪. لم يؤثر تناول عقار إيلوبيريدون مع وجبة غنية بالدهون القياسية بشكل كبير على Cmax أو AUC iloperidone أو P88 أو P95 ، ولكن تم تأخير Tmax لمدة ساعة لمدة iloperidone ، ساعتين لـ P88 و 6 ساعات لـ P95. يمكن أن تدار FANAPT دون النظر إلى وجبات الطعام.
التوزيع: يوجد في إيلوبيريدون خلوص واضح (الخلوص / التوافر البيولوجي) من 47 إلى 102 لتر / ساعة ، مع حجم توزيع واضح من 1340-2800 لتر. في التركيزات العلاجية ، يكون الكسر غير المحدود للأيلوبيريدون في البلازما حوالي 3٪ وكل من مستقلب (P88 و P95) يكون حوالي 8٪.
الأيض والقضاء: يتم استقلاب إيلوبيريدون في المقام الأول عن طريق 3 مسارات للتحول الحيوي: الحد من الكربونيل ، الهيدروكسيل (بوساطة CYP2D6) وإزالة الميثيل بواسطة O (بوساطة CYP3A4). هناك نوعان من الأيضات الأيلوبيريدون السائدة ، P95 و P88. يمثل مستقلب iloperidone P95 47.9 ٪ من AUC من iloperidone وعناصره في البلازما في حالة مستقرة لمركبات الأيض واسعة النطاق (EM) و 25 ٪ لمستقلبات الفقراء (PM). المستقلب النشط P88 يمثل 19.5 ٪ و 34.0 ٪ من إجمالي التعرض للبلازما في EM و PM ، على التوالي.
حوالي 7 ٪ -10 ٪ من القوقازيين و 3 ٪ -8 ٪ من الأمريكيين السود / الأفارقة يفتقرون إلى القدرة على استقلاب CYP2D6 ركائز وتصنف على أنها مستقلبات ضعيفة (PM) ، في حين أن الباقي متوسط ، واسع النطاق أو شديد الرطوبه الأيض. يؤدي التناول المتزامن لـ FANAPT مع مثبطات قوية معروفة للـ CYP2D6 مثل فلوكستين إلى 2.3 أضعاف زيادة في التعرض البلازما iloperidone ، وبالتالي ينبغي أن يكون نصف جرعة FANAPT تدار.
وبالمثل ، فإن PMS من CYP2D6 لديها تعرض أعلى للأيلوبيريدون مقارنةً بالـ EMs ويجب أن تقل جرعة الـ PM بمقدار النصف. الاختبارات المعملية متاحة لتحديد CYP2D6 PMs.
تم استرداد الجزء الأكبر من المواد المشعة في البول (يعني 58.2 ٪ و 45.1 ٪ في EM و PM ، على التوالي) ، مع البراز يمثل 19.9 ٪ (EM) إلى 22.1 ٪ (PM) من النشاط الإشعاعي الجرعات.
تفاعل الناقل: Iloperidone و P88 ليسا ركائز لـ P-gp وإيلوبيريدون هو مثبط P-gp ضعيف.
أعلى
علم السموم غير الإكلينيكي
التسرطن ، الطفرات ، ضعف الخصوبة
التسرطن: أجريت دراسات التسرطن مدى الحياة في الفئران CD-1 وفئران سبراغ داولي. كانت تدار إيلوبيريدون عن طريق الفم بجرعات 2.5 و 5.0 و 10 مغ / كغ / يوم إلى الفئران CD-1 و 4 و 8 و 16 ملغ / كغ / يوم حتى الفئران Sprague Dawley (0.5 ، 1.0 و 2.0 مرة و 1.6 ، 3.2 و 6.5 مرة ، على التوالي ، MRHD 24 ملغ / يوم على ملغ / م 2 أساس). كانت هناك زيادة في حدوث أورام الغدة الثديية الخبيثة في الفئران الأنثوية التي عولجت بأقل جرعة (2.5 مغ / كغ / يوم) فقط. لم تكن هناك زيادات متعلقة بالمعالجة في الأورام لدى الفئران.
الإمكانات المسببة للسرطان لإيلوبريدون المستقلب P95 ، وهو مستقلب رئيسي يدور من الإيلوبيريدون في البشر ولكنه غير موجود بكميات كبيرة في الفئران أو الفئران ، تم تقييمها في دراسة سرطانية مدى الحياة في فئران ويستار بجرعات عن طريق الفم من 25 و 75 و 200 ملغ / كغ / يوم في الذكور و 50 ، 150 ، و 250 (مخفضة من 400) ملغ / كغ / يوم في الإناث. حدثت تغييرات الأورام المرتبطة بالمخدرات في الذكور ، في الغدة النخامية (بارس distalis الورم الحميد) في جميع الجرعات وفي البنكرياس (الورم الحميد خلية جزيرة) بجرعة عالية. كانت مستويات البلازما لـ P95 (AUC) عند الذكور عند الجرعات التي تم اختبارها (25 ، 75 ، و 200 ملغم / كغم / يوم) تقريبًا 0.4 ، 3 ، و 23 مرة ، على التوالي ، تعرض الإنسان لـ P95 عند MRHD لـ iloperidone.
الطفرات: كان إيلوبيريدون سالبًا في اختبار أميس وفي نخاع عظم الفأر الحي واختبار نواة كبد الفئران. ايلوبيريدون الذي يسببه انحرافات الكروموسومات في خلايا الهامستر الصيني المبيض (CHO) في المختبر بتركيزات مما تسبب أيضا في بعض السمية الخلوية.
كان مستقلب iloperidone P95 سالبًا في اختبار Ames ، واختبار انحراف الكروموسوم V79 ، واختبار نواة نخاع عظم الماوس في الجسم الحي.
ضعف الخصوبة: انخفض إيلوبيريدون الخصوبة عند 12 و 36 مغ / كغ في دراسة تم فيها علاج كل من الفئران من الذكور والإناث. كانت الجرعة غير المؤثرة 4 ملغ / كغ ، أي ما يعادل 1.6 ضعف معدل MRHD من 24 ملغ / يوم على أساس ملغ / م 2.
أعلى
الدراسات السريرية
تم دعم فعالية FANAPT في علاج مرض انفصام الشخصية من 2 وهمي تجارب قصيرة المدى (4- و 6 أسابيع) يتم التحكم فيها بشكل نشط وواحدة عشوائية طويلة الأجل يتم التحكم فيها بالعلاج الوهمي محاكمة الانسحاب. سجلت جميع التجارب المرضى الذين استوفوا معايير DSM-III / IV لمرض انفصام الشخصية.
تم استخدام ثلاث أدوات لتقييم العلامات والأعراض النفسية في هذه الدراسات. يعد مقياس المتلازمة الإيجابية والسلبية (PANSS) ومقياس التقييم النفسي الموجز (BPRS) مخزونات متعددة العناصر.
الأمراض النفسية العامة عادة ما تستخدم لتقييم آثار العلاج من تعاطي المخدرات في مرض انفصام الشخصية. يعكس تقييم الانطباع العالمي السريري (CGI) انطباع مراقب ماهر ، على دراية تامة بمظاهر الفصام ، حول الحالة السريرية الشاملة للمريض.
تضمنت تجربة لمدة 6 أسابيع ، وهمي تسيطر عليها (ن = 706) 2 جرعة جرعة مرنة من FANAPT (12-16 ملغ / يوم أو 20-24 ملغ / يوم) مقارنة مع الدواء الوهمي ومراقبة نشطة (ريسبيريدون). بالنسبة للمجموعة 12-16 ملغ / يوم ، كان جدول المعايرة من FANAPT 1 ملغ مرتين يوميًا في الأيام 1 و 2 ، 2 ملغ مرتين يوميًا في الأيام 3 و 4 ، 4 ملغ مرتين يوميًا في الأيام 5 و 6 ، و 6 ملغ مرتين يوميًا في اليوم السابع. بالنسبة للمجموعة 20-24 ملغ / يوم ، كان جدول معايرة FANAPT 1 ملغ مرتين يوميًا في اليوم 1 ، 2 ملغ مرتين يوميًا في اليوم 2 ، 4 ملغ مرتين يوميًا في اليوم 3 و 6 ملغ مرتين يوميًا في أيام 4 و 5 و 8 ملغ مرتين يوميًا في اليوم 6 و 10 ملغ مرتين يوميًا في اليوم 7. كانت نقطة النهاية الأولية هي التغيير من خط الأساس على مجموع نقاط BPRS في نهاية العلاج (اليوم 42). كانت كل من 12-16 ملغ / يوم و 20-24 ملغ / يوم نطاقات من FANAPT متفوقة على الدواء الوهمي على النتيجة الإجمالية BPRS. يبدو أن مضادات الذهان ذات التحكم النشط متفوقة على FANAPT في هذه التجربة خلال أول 2 أسابيع ، والاكتشاف الذي يمكن تفسيره جزئيا بالمعايرة السريعة التي كانت ممكنة لذلك المخدرات. في المرضى في هذه الدراسة الذين ظلوا يتلقون العلاج لمدة أسبوعين على الأقل ، بدا أن إيلوبيريدون كان له فعالية مماثلة للمراقبة الفعالة.
تضمنت تجربة لمدة أسبوعين ، خاضعة للتحكم الوهمي (ن = 604) جرعة واحدة ثابتة من FANAPT (24 ملغ / يوم) مقارنةً بالعلاج الوهمي ومراقبة نشطة (ziprasidone). كان جدول المعايرة لهذه الدراسة مشابهًا لجدول الدراسة 6 أسابيع. شملت هذه الدراسة معايرة FANAPT التي تبدأ من 1 ملغ مرتين يوميًا في اليوم الأول وتزيد إلى 2 و 4 و 6 و 8 و 10 و 12 ملغ مرتين يوميًا في الأيام 2 و 3 و 4 و 5 و 6 و 7. كانت نقطة النهاية الأولية هي التغيير من خط الأساس على النتيجة الإجمالية PANSS في نهاية العلاج (اليوم 28). وكانت جرعة FANAPT 24 ملغ / يوم متفوقة على الدواء الوهمي في النتيجة الإجمالية PANSS. بدا أن FANAPT له فعالية مماثلة لعقار المكافحة الفعالة الذي يحتاج أيضًا إلى معايرة بطيئة للجرعة المستهدفة.
في تجربة طويلة الأجل ، مرضى العيادات الخارجية البالغين المستقر سريريًا (ن = 303) يستوفون معايير DSM-IV لمرض انفصام الشخصية الذي ظل ثابتًا بعد 12 أسبوعًا من تم اختيارهم بصورة عشوائية للعلاج مفتوح التسمية مع جرعات مرنة من FANAPT (8 ملغ / يوم - 24 ملغ / يوم تدار مرتين جرعات يومية) إلى الدواء الوهمي أو الاستمرار في جرعة FANAPT الحالية (8 ملغ / يوم - 24 ملغ / يوم تعطى مرتين كجرعات يومية) لمراقبة احتمال الانتكاس أثناء الانتكاس المزدوج التعمية مرحلة الوقاية. تم تعريف الاستقرار خلال مرحلة فتح الملصقات على أنه موجود على جرعة ثابتة من FANAPT لم يتغير بسبب الفعالية في الأسابيع الأربعة السابقة للعشوائية ، الحصول على درجة خطورة CGI -4 ودرجة PANSS الإجمالية -70 ، درجة -4 على كل عنصر من عناصر PANSS الفردية التالية (الأوهام P1 ، عدم تنظيم المفاهيم P2 ، السلوك المهلوس P3 ، الشبهة / الاضطهاد P6 ، العداوة P7 ، أو عدم تعاون G8) ، وعدم الاستشفاء أو زيادة مستوى الرعاية لعلاج التفاقم. تم تعريف الانتكاس أو الانتكاس الوشيك أثناء مرحلة منع الانتكاس المزدوج التعمية على أنه أي من التالي: دخول المستشفى بسبب تفاقم مرض انفصام الشخصية ، زيادة (تفاقم) النتيجة الكلية PANSS ≥ 30 ٪ ، المجموعة الاستشارية لاندونيسيا
درجة التحسن ≥6 ، كان لدى المريض سلوك انتحاري ، أو قتل ، أو عدواني ، أو يحتاج إلى أي أدوية أخرى مضادة للذهان.

بناءً على التحليل المؤقت ، قررت لجنة مراقبة البيانات المستقلة وقف الدراسة مبكراً بسبب وجود دليل على الفعالية. بناءً على نتائج التحليل المؤقت ، الذي تم تأكيده بواسطة مجموعة بيانات التحليل النهائي ، تم علاج المرضى الذين تم علاجهم شهدت FANAPT وقتا أطول إحصائيا لفترة طويلة للانتكاس أو الانتكاس وشيكة من المرضى الذين تلقوا الوهمي. يعرض الشكل 1 النسبة التراكمية التقديرية للمرضى الذين يعانون من الانتكاس أو الانتكاس الوشيك بناءً على مجموعة البيانات النهائية.
أعلى
كيف زودت / التخزين والمناولة
أقراص FANAPT بيضاء ، وهي مستديرة ومحددة بشعار منقوش على جانب واحد وقوة الكمبيوتر اللوحي "1" أو "2" أو "4" أو "6" أو "8" أو "10" أو "12" من الجهة الأخرى. جانب. يتم توفير الأجهزة اللوحية في نقاط القوة وتكوينات الحزمة التالية:
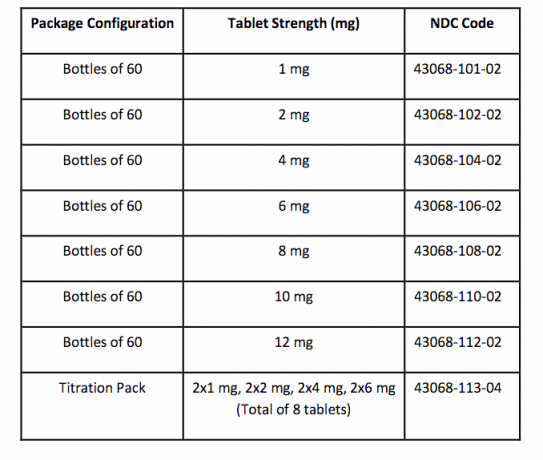
تخزين
تخزين أقراص FANAPT في درجة حرارة الغرفة التي تسيطر عليها ، 25 درجة مئوية (77 درجة فهرنهايت) ؛ الرحلات المسموح بها إلى 15 درجة إلى 30 درجة مئوية (59 درجة إلى 86 درجة فهرنهايت) [انظر درجة حرارة الغرفة التي تسيطر عليها جامعة جنوب المحيط الهادئ]. حماية أقراص FANAPT من التعرض للضوء والرطوبة.
معلومات استشارة المريض
يُنصح الأطباء بمناقشة المشكلات التالية مع المرضى الذين يصفون FANAPT:
إطالة الفاصل الزمني QT
يجب أن ينصح المرضى باستشارة الطبيب فورًا إذا شعروا بالإغماء أو فقدوا الوعي أو خفقان القلب. يجب نصح المرضى بعدم تناول FANAPT مع الأدوية الأخرى التي تسبب إطالة فترة QT. يجب إخبار المرضى بإبلاغ الأطباء بأنهم يتناولون FANAPT قبل تناول أي دواء جديد.
متلازمة الخبيثة العصبية
يجب تقديم المشورة للمرضى ومقدمي الرعاية أن مجمع أعراض قاتل يحتمل الإشارة إليه أحيانًا كما تم الإبلاغ عن NMS بالتعاون مع إدارة العقاقير المضادة للذهان ، بما في ذلك FANAPT. علامات وأعراض NMS تشمل فرط تأكسج الدم ، صلابة العضلات ، تغير الحالة العقلية ، ودليل على اللاإرادي
عدم الاستقرار (نبض غير منتظم أو ضغط الدم ، عدم انتظام دقات القلب ، الحجاب الحاجز ، واضطراب النظم القلبي).
التغييرات الأيضية
يجب أن يكون المرضى على دراية بأعراض ارتفاع السكر في الدم (ارتفاع السكر في الدم) ومرض السكري. المرضى الذين يتم تشخيصهم بمرض السكري أو أولئك الذين لديهم عوامل خطر لمرض السكري أو أولئك الذين يصابون به الأعراض أثناء العلاج يجب أن يتم مراقبة نسبة الجلوكوز في الدم لديهم في بداية الدورة الشهرية وأثناءها علاج او معاملة. يجب نصح المرضى بأن زيادة الوزن قد حدثت أثناء العلاج باستخدام FANAPT. ينصح الرصد السريري للوزن.
هبوط ضغط الدم الانتصابي
يجب إخطار المرضى بخطر انخفاض ضغط الدم الانتصابي ، خاصة في وقت بدء العلاج ، أو إعادة بدء العلاج ، أو زيادة الجرعة.
التدخل في الأداء المعرفي والحركي
نظرًا لأن FANAPT قد يكون له القدرة على إضعاف الحكم أو التفكير أو المهارات الحركية ، يجب الحذر من المرضى تشغيل الآلات الخطرة ، بما في ذلك السيارات ، حتى تكون على يقين معقول من أن علاج FANAPT لا يؤثر عليهم سلبا.
حمل
تقديم المشورة للمرضى أن استخدام الثلث الثالث من الفانابت قد يسبب أعراض خارج هرمية و / أو انسحاب في حديثي الولادة. تقديم المشورة للمرضى لإخطار مقدم الرعاية الصحية مع الحمل المعروفة أو المشتبه فيها.
سجل الحمل
تقديم المشورة للمرضى أن هناك سجل التعرض للحمل الذي يراقب نتائج الحمل في النساء المعرضات ل FANAPT أثناء الحمل
الرضاعة
نصح النساء بعدم الإرضاع من الثدي أثناء العلاج باستخدام FANAPT.
الأدوية المصاحبة
يجب أن يُنصح المرضى بإبلاغ أطبائهم إذا كانوا يتناولون أو يخططون لأخذ أي وصفة طبية أو أدوية بدون وصفة طبية ، لأن هناك إمكانية للتفاعلات.
كحول
يجب أن ينصح المرضى بتجنب الكحول أثناء تناول FANAPT.
التعرض للحرارة والجفاف
يجب نصح المرضى بخصوص الرعاية المناسبة في تجنب ارتفاع درجة الحرارة والجفاف.
موزع من قبل:
فاندا للصناعات الدوائية
واشنطن العاصمة 20037 الولايات المتحدة الأمريكية
Vanda و Fanapt® هي علامات تجارية مسجلة لشركة Vanda Pharmaceuticals Inc. في الولايات المتحدة وبلدان أخرى.
العودة إلى الأعلى
Fanapt (إيلوبيريدون) دليل وصف (بي دي إف)
لا تهدف المعلومات الواردة في هذه الدراسة إلى تغطية جميع الاستخدامات أو الاتجاهات أو الاحتياطات الممكنة أو التفاعلات الدوائية أو الآثار الضارة. هذه المعلومات معممة ولا تهدف إلى تقديم المشورة الطبية المحددة. إذا كانت لديك أسئلة حول الأدوية التي تتناولها أو ترغب في مزيد من المعلومات ، فاستشر طبيبك أو الصيدلي أو الممرض.
آخر تحديث 07/13
ارجع الى: الأدوية الدوائية



