اكتوس لمرض السكري من النوع 2
اسم العلامة التجارية: Actos
الاسم العام: بيوغليتازون هيدروكلوريد
محتويات:
وصف
علم العقاقير
المؤشرات والاستخدام
موانع
تحذيرات
الاحتياطات
ردود الفعل السلبية
جرعة مفرطة
الجرعة والإدارة
كيف زودت
Actos ، بيوجليتازون hcl ، معلومات المريض (في سهل الانجليزية)
تحذير: فشل القلب الاحتقاني
- الثيازيدونينيون ، بما في ذلك الأكتوس ، يسبب أو يؤدي إلى تفاقم قصور القلب الاحتقاني لدى بعض المرضى (انظر تحذيرات). بعد بدء Actos ، وبعد زيادة الجرعة ، لاحظ المرضى بعناية بحثًا عن علامات وأعراض قصور القلب (بما في ذلك زيادة الوزن الزائدة السريعة ، وضيق التنفس ، و / أو الوذمة). إذا تطورت هذه العلامات والأعراض ، فيجب إدارة قصور القلب وفقًا لمعايير الرعاية الحالية. وعلاوة على ذلك ، يجب النظر في وقف أو تخفيض جرعة من Actos.
- الأكتوس لا ينصح به في المرضى الذين يعانون من قصور القلب العرضي. هو بطلان بدء Actos في المرضى الذين يعانون من فشل القلب NYHA من الدرجة الثالثة أو الرابعة (انظر موانع و تحذيرات).
وصف
Actos (بيوجليتازون هيدروكلوريد) هو عامل مضاد لمرض السكر عن طريق الفم يعمل بشكل أساسي عن طريق تقليل مقاومة الأنسولين. يستخدم Actos في إدارة داء السكري من النوع 2 (المعروف أيضًا باسم داء السكري غير المعتمد على الأنسولين [NIDDM] أو مرض السكري الذي يصيب البالغين). تشير الدراسات الدوائية إلى أن الأكتوس يحسن الحساسية للأنسولين في الأنسجة الدهنية والعضلية ويمنع تكوين السكر في الكبد. Actos يحسن السيطرة على نسبة السكر في الدم مع تقليل مستويات الانسولين المتداولة.
البيوجليتازون [(±) -5 - [[4- [2- (2- (5-إيثيل 2-بيريدينيل) إيثوكسي] فينيل] ميثيل] -2،4-] ثيازيدوليدين مونوهيدروكلوريد ينتمي إلى فئة كيميائية مختلفة ولها تأثير دوائي مختلف عن السلفونيل يوريا ، الميتفورمين ، أو gl ±-glucosidase مثبطات. يحتوي الجزيء على كربون غير متماثل واحد ، ويتم تصنيع المركب واستخدامه كخليط راسيمي. التمامين اثنين من بيوجليتازون interconvert في الجسم الحي. لم يتم العثور على اختلافات في النشاط الدوائي بين اثنين من التناقضات. الصيغة الهيكلية كما هو موضح:
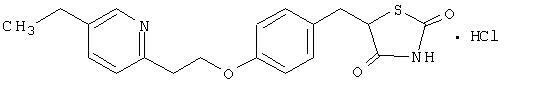
بيوغليتازون هيدروكلوريد هو مسحوق بلوري أبيض عديم الرائحة يحتوي على صيغة جزيئية من C19H20ن2O3S-HCl ويبلغ الوزن الجزيئي 392.90 دالتون. وهو قابل للذوبان في N ، ثنائي ميثيل فورماميد N ، قابل للذوبان قليلاً في الإيثانول اللامائي ، قابل للذوبان قليلاً في الأسيتون والأسيتونيتريل ، غير قابل للذوبان عملياً في الماء ، وغير قابل للذوبان في الأثير.
يتوفر Actos على شكل قرص للإعطاء عن طريق الفم يحتوي على 15 ملغ أو 30 ملغ أو 45 ملغ من البيوجليتازون (كقاعدة) مصاغة مع السواغات التالية: lActose monohydrate NF ، hydroxypropylcellulose NF ، carboxymethylcellulose calcium NF ، وستيرات المغنيسيوم NF.
أعلى
علم الصيدلة السريرية
آلية العمل
Actos هو عامل مضاد لمرض السكر الثيازيدوليدين الذي يعتمد على وجود الأنسولين لآلية عملها. الأكتوس يقلل من مقاومة الأنسولين في المحيط وفي الكبد مما يؤدي إلى زيادة التخلص من الجلوكوز المعتمد على الأنسولين وانخفاض إنتاج الجلوكوز الكبدي. على عكس السلفونيل يوريا ، فإن البيوجليتازون ليس إفرازًا للأنسولين. البيوجليتازون هو ناهض قوي لمستقبلات غاما المنشط بالبيروكسيسوم (PPARγ). تم العثور على مستقبلات PPAR في الأنسجة المهمة لعمل الأنسولين مثل الأنسجة الدهنية والعضلات الهيكلية والكبد. يؤدي تنشيط مستقبلات PPARγ النووية إلى تعديل نسخ عدد من الجينات المستجيبة للأنسولين التي تشارك في التحكم في استقلاب الجلوكوز والدهون.
في النماذج الحيوانية لمرض السكري ، يقلل البيوجليتازون من ارتفاع السكر في الدم ، فرط الأنسولين في الدم ، وفرط الدهون الثلاثية في الحالات المقاومة للأنسولين مثل السكري من النوع 2. التغييرات الأيضية الناتجة عن بيوجليتازون تؤدي إلى زيادة استجابة الأنسجة التي تعتمد على الأنسولين ولوحظت في العديد من النماذج الحيوانية من مقاومة الأنسولين.
نظرًا لأن البيوجليتازون يعزز من آثار تعميم الأنسولين (عن طريق تقليل مقاومة الأنسولين) ، فإنه لا يخفض نسبة الجلوكوز في الدم في النماذج الحيوانية التي تفتقر إلى الأنسولين الداخلي.
الدوائية والأيض المخدرات
لا تزال تركيزات مصل البيوجليتازون الكلي (بيوجليتازون بالإضافة إلى المستقلبات النشطة) مرتفعة بعد 24 ساعة من الجرعات مرة واحدة يوميًا. يتم تحقيق تركيزات مصل الحالة الثابتة لكل من البيوجليتازون والبيوجليتازون الكلي خلال 7 أيام. في الحالة المستقرة ، يصل اثنان من المستقلبات النشطة دوائيا من البيوجليتازون ، المستقلبات الثالث (M-III) و IV (M-IV) إلى تركيزات مصل مساوية أو أكبر من البيوجليتازون. في كل من المتطوعين الأصحاء والمرضى الذين يعانون من مرض السكري من النوع 2 ، بيوغليتازون تضم حوالي 30 ٪ إلى 50 ٪ من ذروة إجمالي تركيزات مصل البيوجليتازون و 20 ٪ إلى 25 ٪ من المساحة الكلية تحت منحنى تركيز وقت المصل (AUC).
تركيز المصل الأقصى (Cماكس) ، AUC ، وتركيزات مصل الحوض (Cدقيقة) لكل من البيوجليتازون والبيوجليتازون الكلي يزداد تناسبيًا عند تناول جرعات تبلغ 15 ملغ و 30 ملغ يوميًا. هناك زيادة أقل بقليل عن بيوجليتازون والبيوجليتازون الكلي بجرعة 60 ملغ في اليوم.
الامتصاص: بعد تناوله عن طريق الفم ، في حالة الصيام ، يمكن قياس البيوجليتازون لأول مرة في المصل خلال 30 دقيقة ، مع ملاحظة تركيزات الذروة خلال ساعتين. يؤخر الطعام قليلاً من الوقت لذروة تركيز المصل إلى 3 إلى 4 ساعات ، لكنه لا يغير مدى الامتصاص.
التوزيع: متوسط الحجم الظاهري للتوزيع (Vd / F) للبيوجليتازون بعد إعطاء جرعة واحدة هو 0.63 ± 0.41 (متوسط ± SD) L / كجم من وزن الجسم.
البيوجليتازون مرتبط على نطاق واسع بالبروتين (> 99 ٪) في مصل الإنسان ، وبشكل أساسي إلى مصل الزلال. يرتبط البيوجليتازون أيضًا ببروتينات المصل الأخرى ، ولكن مع تقارب أقل. الأيض M-III و M-IV مرتبطان على نطاق واسع (> 98 ٪) إلى ألبومين المصل.
التمثيل الغذائي: يتم استقلاب البيوجليتازون على نطاق واسع عن طريق الهيدروكسيل والأكسدة ؛ تتحول المستقلبات جزئيًا أيضًا إلى اتحادات الجلوكورونيد أو الكبريتات. الأيض M-II و M-IV (مشتقات الهيدروكسي من البيوجليتازون) و M-III (مشتق كيتو من البيوجليتازون) تنشط دوائيا في النماذج الحيوانية لمرض السكري من النوع 2. بالإضافة إلى البيوجليتازون ، M-III و M-IV هي الأنواع الرئيسية ذات الصلة بالمخدرات الموجودة في مصل الإنسان بعد الجرعات المتعددة. في حالة مستقرة ، في كل من المتطوعين الأصحاء والمرضى الذين يعانون من مرض السكري من النوع 2 ، بيوجليتازون تضم حوالي 30 ٪ إلى 50 ٪ من إجمالي تركيزات مصل الذروة و 20 ٪ إلى 25 ٪ من مجموع الجامعة الأمريكية.
في البيانات المختبرية تبين أن العديد من الأشكال الإسوية CYP تشارك في عملية التمثيل الغذائي للبيوجليتازون. السيتوكروم P450 الأشكال المشاركة هي CYP2C8 ، وبدرجة أقل ، CYP3A4 مع مساهمات إضافية من مجموعة متنوعة من الأشكال الإسوية الأخرى بما في ذلك CYP1A1 خارج الكبد بشكل رئيسي. في الدراسات المجراة للبيوجليتازون بالاشتراك مع مثبطات P450 والركائز التي أجريت (انظر تفاعل الأدوية). أظهرت نسب البول 6-هيدروكسي كورتيزول / كورتيزول المقاسة في المرضى الذين عولجوا مع أكتوس أن البيوجليتازون ليس محفزًا قويًا لإنزيم CYP3A4.
إفراز وإزالة: بعد تناوله عن طريق الفم ، يتم استرداد ما يقرب من 15 ٪ إلى 30 ٪ من جرعة البيوجليتازون في البول. التخلص الكلوي من البيوجليتازون لا يكاد يذكر ، ويتم إفراز الدواء في المقام الأول كنواتج أيضية ومقارناتها. يفترض أن معظم جرعة الفم يتم إفرازها في الصفراء إما دون تغيير أو كمادة أيضية ويتم التخلص منها في البراز.
يتراوح متوسط عمر النصف للمصل للبيوجليتازون والبيوجليتازون الكلي من 3 إلى 7 ساعات ومن 16 إلى 24 ساعة على التوالي. تتمتع البيوجليتازون بمسح واضح ، CL / F ، محسوب من 5 إلى 7 لتر / ساعة.
السكان الخاصة
القصور الكلوي: يبقى نصف عمر التخلص من المصل للبيوجليتازون و M-III و M-IV بدون تغيير في المرضى الذين يعانون من معتدلة (تصفية الكرياتينين 30 إلى 60 مل / دقيقة) إلى اختلال كلوي حاد (إزالة الكرياتينين أقل من 30 مل / دقيقة) بالمقارنة مع المعدل الطبيعي المواضيع. لا ينصح بتعديل الجرعة عند مرضى القصور الكلوي (انظر الجرعة والإدارة).
القصور الكبدي: بالمقارنة مع الضوابط الطبيعية ، فإن الأشخاص الذين يعانون من اختلال وظيفي في وظائف الكبد (تشايلد- بوغ الصف ب / ج) انخفاض تقريبي 45 ٪ في بيوجليتازون والبيوجليتازون الكلي يعني تركيزات الذروة ولكن لا تغيير في متوسط AUC القيم.
لا ينبغي أن يبدأ العلاج بالآكتوس إذا أظهر المريض أدلة سريرية على مرض الكبد النشط أو مستويات ترانساميناز المصل (ALT) تتجاوز 2.5 مرة الحد الأعلى الطبيعي (انظر احتياطات، آثار الكبد).
كبار السن: في الأشخاص المسنين الأصحاء ، لا توجد تركيزات مصل الذروة في البيوجليتازون والبيوجليتازون الكلي. تختلف اختلافًا كبيرًا ، لكن قيم AUC أعلى قليلاً وقيم نصف العمر الطرفية أطول قليلاً من أجل المواضيع الأصغر سنا. لم تكن هذه التغييرات من الحجم الذي سيعتبر سريريا.
طب الأطفال: البيانات الدوائية في السكان الأطفال غير متوفرة.
الجنس: الوسط جماكس وزادت القيم AUC 20 ٪ إلى 60 ٪ في الإناث. كعلاج وحيد وبالتزامن مع السلفونيل يوريا ، الميتفورمين ، أو الأنسولين ، حسّن اكتوس السيطرة على نسبة السكر في الدم في كل من الذكور والإناث. في التجارب السريرية التي تسيطر عليها ، الهيموغلوبين A1C (HBA1C) النقصان من خط الأساس كان أكبر بشكل عام بالنسبة للإناث عنه بالنسبة للذكور (متوسط الفرق في معدل HbA1C 0.5%). نظرًا لأن العلاج يجب أن يكون فرديًا لكل مريض لتحقيق التحكم في نسبة السكر في الدم ، لا ينصح بأي تعديل للجرعة على أساس الجنس وحده.
العرق: البيانات الدوائية بين المجموعات العرقية المختلفة غير متوفرة.
المخدرات المخدرات التفاعلات
تمت دراسة الأدوية التالية في المتطوعين الأصحاء مع إدارة مشتركة من Actos 45 ملغ مرة واحدة يوميًا. المدرجة أدناه هي النتائج:
موانع الحمل الفموية: الإدارة المشتركة للأكتوس (45 ملغ مرة واحدة يوميًا) وموانع الحمل الفموية (1 ملغ نوريثيندرون زائد 0.035 ملغ إيثينيل استراديول مرة واحدة يوميًا) لمدة 21 يومًا ، مما أدى إلى انخفاض بنسبة 11٪ و 11-14٪ في إيثينيل استراديول AUC (0-24 ساعة) و Cماكس على التوالي. لم تكن هناك تغييرات كبيرة في norethindrone AUC (0-24h) و Cماكس. في ضوء التباين الكبير في الحرائك الدوائية للإيثينيل ، فإن الأهمية السريرية لهذا الاكتشاف غير معروفة.
Fexofenadine حمض الهيدروكلوريك: شارك في إدارة Actos لمدة 7 أيام مع 60 ملغ fexofenadine تدار عن طريق الفم مرتين يوميا أدى إلى أي تأثير كبير على الدوائية pioglitazone. لم يكن Actos له تأثير كبير على الدوائية fexofenadine.
Glipizide: المشاركة في إدارة Actos و 5 mg glipizide التي تدار عن طريق الفم مرة واحدة يوميًا لمدة 7 أيام لم يغير من الحالة الدوائية للحالة المستقرة للجليبيزيد.
الديجوكسين: المشاركة في إدارة Actos مع 0.25 ملغ من الديجوكسين التي يتم تناولها عن طريق الفم مرة واحدة يوميًا لمدة 7 أيام لم تغير من الحالة الدوائية للحالة الثابتة للديجوكسين.
الوارفارين: المشاركة في إدارة Actos لمدة 7 أيام مع الوارفارين لم يغير الدوائية الحالة المستقرة من الوارفارين. ليس لـ Actos أي تأثير كبير سريريًا على وقت البروثرومبين عند تناوله للمرضى الذين يتلقون علاج الوارفارين المزمن.
الميتفورمين: شارك في تناول جرعة واحدة من الميتفورمين (1000 ملغ) و Actos بعد 7 أيام من Actos لم يغير الدوائية من جرعة واحدة من الميتفورمين.
Midazolam: تناولت Actos لمدة 15 يومًا تليها جرعة واحدة 7.5 ملغ من شراب midazolam مما أدى إلى انخفاض بنسبة 26 ٪ في الميدازولام Cماكس و AUC.
رانيتيدين حمض الهيدروكلوريك: شارك في إدارة Actos لمدة 7 أيام مع رانيتيدين تدار عن طريق الفم مرتين يوميا لمدة 4 أو 7 أيام أسفرت عن أي تأثير كبير على الدوائية بيوغليتازون. أظهرت Actos أي تأثير كبير على الدوائية رانيتيدين.
Nifedipine ER: المشاركة في إدارة Actos لمدة 7 أيام مع 30 ملغ Nifedipine ER تعطى عن طريق الفم مرة واحدة يوميًا لمدة 4 أيام إلى أدى المتطوعون من الذكور والإناث إلى القيم المتوسطة على الأقل (90٪ CI) للنيفيديبين دون تغيير عند 0.83 (0.73 - 0.95) لـ Cماكس و 0.88 (0.80 - 0.96) للجامعة الأمريكية بالقاهرة. في ضوء التباين العالي في الدوائية نيفيديبين ، أهمية السريرية لهذا الاكتشاف غير معروف.
الكيتوكونازول: شارك في إدارة Actos لمدة 7 أيام مع الكيتوكونازول 200 ملغ تدار مرتين نتج عن القيم المتوسطة المربعة (90٪ CI) للبيوجليتازون بدون تغيير عند 1.14 (1.06 - 1.23) ل Cماكس، 1.34 (1.26 - 1.41) لـ AUC و 1.87 (1.71 - 2.04) لـ Cدقيقة.
أتورفاستاتين الكالسيوم: المشاركة في إدارة Actos لمدة 7 أيام مع أتورفاستاتين الكالسيوم (LIPITOR®) 80 ملغ مرة واحدة يوميًا ، نتج عن القيم المتوسطة على الأقل (90٪ CI) للبيوجليتازون بدون تغيير عند 0.69 (0.57 - 0.85) ل Cماكس، 0.76 (0.65 - 0.88) لـ AUC و 0.96 (0.87 - 1.05) لـ Cدقيقة. بالنسبة إلى أتورفاستاتين بدون تغيير ، كانت قيم المتوسط الأدنى (90٪ CI) هي 0.77 (0.66 - 0.90) لـ Cماكس، 0.86 (0.78 - 0.94) لـ AUC و 0.92 (0.82 - 1.02) لـ Cدقيقة.
الثيوفيلين: المشاركة في إدارة Actos لمدة 7 أيام مع الثيوفيلين 400 ملغ تدار مرتين يوميا لم تسفر عن أي تغيير في الدوائية لأي من المخدرات.
السيتوكروم P450: انظر احتياطات
Gemfibrozil: تناول مصاحب لـ gemfibrozil (عن طريق الفم 600 ملغ مرتين يوميًا) ، وهو مثبط لـ CYP2C8 ، مع بيوجليتازون (عن طريق الفم 30 ملغ) في 10 متطوعين أصحاء يعالجون مسبقًا لمدة يومين قبل تناول الجيمفيبروزيل (عن طريق الفم 600 ملغ مرتين يوميًا) أدى التعرض للبيوجليتازون (AUC0-24) إلى 226 ٪ من التعرض للبيوجليتازون في غياب الجيمفيبروزيل (نرى احتياطات).
ريفامبين: تناول مصاحب للريفامبين (600 ملغ عن طريق الفم مرة واحدة يوميًا) ، وهو محفز لـ CYP2C8 مع بيوجليتازون (عن طريق الفم 30 ملغ) في 10 صحي نتج عن المتطوعين الذين عولجوا قبل 5 أيام قبل تناول الريفامبين (عن طريق الفم 600 ملغ مرة واحدة يوميًا) انخفاض في الـ AUC للبيوجليتازون بنسبة 54٪ (انظر احتياطات).
الديناميكا الدوائية والآثار السريرية
الدراسات السريرية تثبت أن Actos يحسن حساسية الأنسولين لدى المرضى المقاومين للأنسولين. Actos يعزز الاستجابة الخلوية للأنسولين ، ويزيد من التخلص من الجلوكوز المعتمد على الأنسولين ، ويحسن حساسية الكبد للأنسولين ، ويحسن توازن الجلوكوز المختل وظيفيًا. في مرضى السكري من النوع 2 ، تؤدي مقاومة الأنسولين المنخفضة الناتجة عن Actos إلى انخفاض تركيز الجلوكوز في البلازما ، وانخفاض مستويات الأنسولين في البلازما ، وخفض نسبة HbA1C القيم. استنادًا إلى النتائج التي توصلت إليها دراسة التمديد المفتوح ، يبدو أن تأثيرات خفض الجلوكوز لـ Actos تستمر لمدة عام واحد على الأقل. في التجارب السريرية الخاضعة للرقابة ، كان لـ Actos مع السلفونيل يوريا أو الميتفورمين أو الأنسولين تأثير إضافي على التحكم في نسبة السكر في الدم.
تم تضمين المرضى الذين يعانون من تشوهات الدهون في التجارب السريرية مع Actos. بشكل عام ، كان لدى المرضى الذين عولجوا بـ Actos انخفاضات في الدهون الثلاثية ، يعني زيادة في نسبة الكوليسترول الحميد ، وأي تغييرات متوسطة ثابتة في LDL والكوليسترول الكلي.
في دراسة مدتها 26 أسبوعًا ، تم التحكم فيها بالعلاج الوهمي والجرعة ، انخفض متوسط مستويات الدهون الثلاثية في مجموعات جرعة 15 ملغ و 30 ملغ و 45 ملغ من أكتوس مقارنة بزيادة متوسطة في مجموعة العلاج الوهمي. زيادة متوسط مستويات HDL في المرضى الذين عولجوا بـ Actos أكثر من المرضى الذين عولجوا بدواء وهمي. لم تكن هناك اختلافات ثابتة ل LDL والكوليسترول الكلي في المرضى الذين عولجوا مع Actos مقارنة مع الدواء الوهمي (الجدول 1).
الجدول 1 الدهون في دراسة الجرعة الوهمي الخاضعة للرقابة لمدة 26 أسبوعًا
| الوهمي | أكتوس 15 ملغ ذات مرة اليومي |
أكتوس 30 ملغ ذات مرة اليومي |
أكتوس 45 ملغ ذات مرة اليومي |
|
| الدهون الثلاثية (ملغ / دل) | N = 79 | N = 79 | N = 84 | N = 77 |
| خط الأساس (الوسط) | 262.8 | 283.8 | 261.1 | 259.7 |
| نسبة التغيير من خط الأساس (الوسط) | 4.8% | -9.0% | -9.6% | -9.3% |
| الكوليسترول الحميد (مجم / ديسيلتر) | N = 79 | N = 79 | N = 83 | N = 77 |
| خط الأساس (الوسط) | 41.7 | 40.4 | 40.8 | 40.7 |
| نسبة التغيير من خط الأساس (الوسط) | 8.1% | 14.1% | 12.2% | 19.1% |
| LDL الكوليسترول (ملغ / ديسيلتر) | N = 65 | N = 63 | N = 74 | N = 62 |
| خط الأساس (الوسط) | 138.8 | 131.9 | 135.6 | 126.8 |
| نسبة التغيير من خط الأساس (الوسط) | 4.8% | 7.2% | 5.2% | 6.0% |
| الكوليسترول الكلي (mg / dL) | N = 79 | N = 79 | N = 84 | N = 77 |
| خط الأساس (الوسط) | 224.6 | 220.0 | 222.7 | 213.7 |
| نسبة التغيير من خط الأساس (الوسط) | 4.4% | 4.6% | 3.3% | 6.4% |
في دراستي العلاج الأحادي الأخريين (24 أسبوعًا و 16 أسبوعًا) وفي دراسات العلاج المركب مع السلفونيل يوريا (24 أسبوعًا و 16 أسبوعًا) والميتفورمين (24 أسبوعًا و 16 أسبوعًا) ، كانت النتائج متسقة بشكل عام مع البيانات في الاعلى. في التجارب التي يسيطر عليها الدواء الوهمي ، انخفض متوسط التغييرات المصحوبة بالغفل من خط الأساس بنسبة 5 ٪ إلى 26 ٪ بالنسبة للدهون الثلاثية وزاد من 6 ٪ إلى 13 ٪ ل HDL في المرضى الذين عولجوا بـ Actos. وشوهد نمط مماثل من النتائج في دراسات العلاج المركب لمدة 24 أسبوعًا من Actos مع السلفونيل يوريا أو الميتفورمين.
في دراسة للعلاج المركب مع الأنسولين (16 أسبوعًا) ، انخفض أيضًا متوسط النسبة المئوية لتصحيح الغفل من خط الأساس في قيم الدهون الثلاثية للمرضى الذين عولجوا بـ Actos. ولوحظ وجود تغيير يعني تصحيح الخطأ الوهمي من خط الأساس في الكوليسترول LDL من 7 ٪ لمجموعة جرعة 15 ملغ. وقد لوحظت نتائج مماثلة لتلك المذكورة أعلاه ل HDL والكوليسترول الكلي. وشوهد نمط مماثل من النتائج في دراسة علاجية مدمجة استمرت 24 أسبوعًا مع Actos مع الأنسولين.
الدراسات السريرية
وحيد
في الولايات المتحدة ، أجريت ثلاث تجارب عشوائية مزدوجة التعمية ، وهمي تسيطر عليها مع فترات من 16 إلى 26 أسبوعا لتقييم استخدام Actos كعلاج وحيد في مرضى السكري من النوع 2. درست هذه الدراسات اكتوس بجرعات تصل إلى 45 ملغ أو وهمي مرة واحدة يوميا في 865 مريضا.
في دراسة مدتها 26 أسبوعًا ، تم اختيار عشوائي 408 مريضًا مصابين بداء السكري من النوع 2 لتلقي 7.5 ملغ أو 15 ملغ أو 30 ملغ أو 45 ملغ من أكتوس أو دواء وهمي مرة واحدة يوميًا. تم إيقاف العلاج مع أي عامل مضاد لمرض السكر السابق قبل 8 أسابيع من فترة التعمية المزدوجة. المعاملة مع 15 ملغ ، 30 ملغ ، و 45 ملغ من Actos أنتجت تحسينات ذات دلالة إحصائية في HbA1c والصيام الجلوكوز في البلازما (FPG) في نقطة النهاية مقارنة مع الدواء الوهمي (الشكل 1 ، الجدول 2).
يوضح الشكل 1 الدورة الزمنية للتغييرات في FPG و HbA1c لكامل مجتمع الدراسة في هذه الدراسة التي استمرت 26 أسبوعًا.
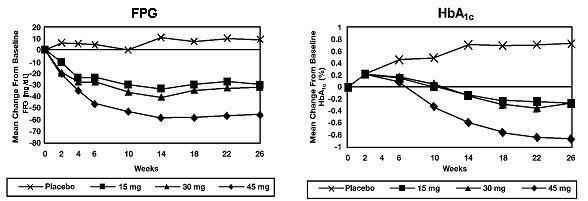
ويبين الجدول 2 HbA1C و FPG القيم لكامل مجتمع الدراسة.
الجدول 2 معلمات نسبة السكر في الدم في دراسة الجرعة تتراوح بين 26 أسبوع وهمي تسيطر عليها
| الوهمي | أكتوس 15 ملغ ذات مرة اليومي |
أكتوس 30 ملغ ذات مرة اليومي |
أكتوس 45 ملغ ذات مرة اليومي |
|
| مجموع السكان | ||||
| HBA1C (%) | N = 79 | N = 79 | N = 85 | N = 76 |
| خط الأساس (الوسط) | 10.4 | 10.2 | 10.2 | 10.3 |
| التغيير من الأساس (المعدل المعدل)+) | 0.7 | -0.3 | -0.3 | -0.9 |
| الفرق من الدواء الوهمي (المعدل المعدل)+) | -1.0* | -1.0* | -1.6* | |
| FPG (mg / dL) | N = 79 | N = 79 | N = 84 | N = 77 |
| خط الأساس (الوسط) | 268 | 267 | 269 | 276 |
| التغيير من الأساس (المعدل المعدل)+) | 9 | -30 | -32 | -56 |
| الفرق من الدواء الوهمي (المعدل المعدل)+) | -39* | -41* | -65* | |
|
+ ضبط الأساس ، مركز المجمعة ، ومركز المجمعة عن طريق التفاعل العلاج * ع ¤ 50 0.050 مقابل الوهمي |
شمل مجتمع الدراسة المرضى الذين لم يعالجوا سابقًا بالأدوية المضادة للسكري (السذاجة) ؛ 31 ٪) والمرضى الذين كانوا يتلقون الأدوية المضادة للسكري في وقت التسجيل في الدراسة (سبق علاجه ؛ 69%). يتم عرض البيانات الخاصة بمجموعات فرعية المريض والمعالجة سابقًا في الجدول 3. دخل جميع المرضى لفترة غسيل لمدة 8 أسابيع قبل العلاج المزدوج التعمية. ارتبطت فترة التشغيل هذه بتغير بسيط في نسبة HbA1C وقيم FPG من الفحص إلى الأساس للمرضى الساذجين ؛ ومع ذلك ، بالنسبة للمجموعة التي تم علاجها سابقًا ، نتج عن غسل الدواء المضاد لمرض السكر السابق تدهور التحكم في نسبة السكر في الدم وزيادة في نسبة HbA1C و FPG. على الرغم من أن معظم المرضى في المجموعة التي سبق علاجها كان لديهم انخفاض من خط الأساس في HbA1C و FPG مع Actos ، في كثير من الحالات ، لم تعد القيم إلى مستويات الفحص بنهاية الدراسة. لم يسمح تصميم الدراسة بتقييم المرضى الذين تحولوا مباشرة إلى أكتو من عامل مضاد لمرض السكر آخر.
الجدول 3 معلمات نسبة السكر في الدم في دراسة الجرعة تتراوح بين 26 أسبوع وهمي تسيطر عليها
| الوهمي | أكتوس 15 ملغ ذات مرة اليومي |
أكتوس 30 ملغ ذات مرة اليومي |
أكتوس 45 ملغ ذات مرة اليومي |
|
| نذهب إلى العلاج HBA1C (%) |
N = 25 | N = 26 | N = 26 | N = 21 |
| الفحص (الوسط) | 9.3 | 10.0 | 9.5 | 9.8 |
| خط الأساس (الوسط) | 9.0 | 9.9 | 9.3 | 10.0 |
| التغيير من الأساس (المعدل المعدل *) | 0.6 | -0.8 | -0.6 | -1.9 |
| الفرق من الدواء الوهمي (المعدل المعدل *) | -1.4 | -1.3 | -2.6 | |
| FPG (mg / dL) | N = 25 | N = 26 | N = 26 | N = 21 |
| الفحص (الوسط) | 223 | 245 | 239 | 239 |
| خط الأساس (الوسط) | 229 | 251 | 225 | 235 |
| التغيير من الأساس (المعدل المعدل *) | 16 | -37 | -41 | -64 |
| الفرق من الدواء الوهمي (المعدل المعدل *) | -52 | -56 | -80 | |
| سبق معالجتها HBA1C (%) |
N = 54 | N = 53 | N = 59 | N = 55 |
| الفحص (الوسط) | 9.3 | 9.0 | 9.1 | 9.0 |
| خط الأساس (الوسط) | 10.9 | 10.4 | 10.4 | 10.6 |
| التغيير من الأساس (المعدل المعدل *) | 0.8 | -0.1 | -0.0 | -0.6 |
| الفرق من الدواء الوهمي (المعدل المعدل *) | -1.0 | -0.9 | -1.4 | |
| FPG (mg / dL) | N = 54 | N = 53 | N = 58 | N = 56 |
| الفحص (الوسط) | 222 | 209 | 230 | 215 |
| خط الأساس (الوسط) | 285 | 275 | 286 | 292 |
| التغيير من الأساس (المعدل المعدل *) | 4 | -32 | -27 | -55 |
| الفرق من الدواء الوهمي (المعدل المعدل *) | -36 | -31 | -59 | |
| * ضبط لخط الأساس ومركز المجمعة |
في دراسة استمرت 24 أسبوعًا تم التحكم فيها بالعلاج الوهمي ، تم اختيارهم بصورة عشوائية على 260 مريضًا مصابون بداء السكري من النوع 2 في واحدة من مجموعتي علاج أكتو بالمعايرة القسرية أو مجموعة غفل وهمية. تم إيقاف العلاج مع أي عامل مضاد لمرض السكر السابق قبل 6 أسابيع من فترة التعمية المزدوجة. في إحدى مجموعات علاج Actos ، تلقى المرضى جرعة مبدئية قدرها 7.5 ملغ مرة واحدة يوميًا. بعد أربعة أسابيع ، تم زيادة الجرعة إلى 15 ملغ مرة واحدة يوميًا وبعد أربعة أسابيع أخرى ، تم زيادة الجرعة إلى 30 ملغ مرة واحدة يوميًا للفترة المتبقية من الدراسة (16 أسبوعًا). في مجموعة العلاج Actos الثانية ، تلقى المرضى جرعة أولية من 15 ملغ مرة واحدة يوميًا وتم معايرتها إلى 30 ملغ مرة واحدة يوميًا و 45 ملغ مرة واحدة يوميًا بطريقة مماثلة. العلاج مع Actos ، كما هو موضح ، أنتجت تحسينات ذات دلالة إحصائية في HbA1C و FPG في نقطة النهاية مقارنة مع الدواء الوهمي (الجدول 4).
الجدول 4 معلمات نسبة السكر في الدم في دراسة الإكراه القسري لمدة 24 أسبوعا التي تسيطر عليها وهمي
| الوهمي | أكتوس 30 ملغ+ مرة واحدة يوميا |
أكتوس 45 ملغ+ مرة واحدة يوميا |
|
| مجموع السكان HBA1C (%) |
N = 83 | N = 85 | N = 85 |
| خط الأساس (الوسط) | 10.8 | 10.3 | 10.8 |
| التغيير من الأساس (المعدل المعدل)++) | 0.9 | -0.6 | -0.6 |
| الفرق من الدواء الوهمي (المعدل المعدل)++) | -1.5* | -1.5* | |
| FPG (mg / dL) | N = 78 | N = 82 | N = 85 |
| خط الأساس (الوسط) | 279 | 268 | 281 |
| التغيير من الأساس (المعدل المعدل)++) | 18 | -44 | -50 |
| الفرق من الدواء الوهمي (المعدل المعدل)++) | -62* | -68* | |
|
+ الجرعة النهائية في المعايرة القسرية ++ ضبط الأساس ، مركز المجمعة ، ومركز المجمعة عن طريق التفاعل العلاج * ع ¤ 50 0.050 مقابل الوهمي |
بالنسبة للمرضى الذين لم يعالجوا سابقًا بالأدوية المضادة للسكري (24٪) ، كانت القيم المتوسطة عند الفحص 10.1٪ لـ HbA1C و 238 ملغ / ديسيلتر ل FPG. في الأساس ، يعني HBA1C كان 10.2 ٪ ويعني FPG كان 243 ملغ / ديسيلتر. مقارنة مع الدواء الوهمي ، أدى العلاج بالـ Actos إلى الجرعة النهائية البالغة 30 ملغ و 45 ملغ إلى تخفيضات من خط الأساس في متوسط HbA1C من 2.3 ٪ و 2.6 ٪ ويعني FPG من 63 ملغ / ديسيلتر و 95 ملغ / ديسيلتر ، على التوالي. بالنسبة للمرضى الذين سبق علاجهم بالأدوية المضادة لمرض السكر (76٪) ، توقف هذا الدواء عند الفحص. وكانت القيم يعني في الفحص 9.4 ٪ ل HbA1C و 216 ملغ / ديسيلتر ل FPG. في الأساس ، يعني HBA1C كان 10.7 ٪ ويعني FPG كان 290 ملغ / ديسيلتر. مقارنة مع الدواء الوهمي ، أدى العلاج بالـ Actos إلى الجرعة النهائية البالغة 30 ملغ و 45 ملغ إلى تخفيضات من خط الأساس في متوسط HbA1C من 1.3 ٪ و 1.4 ٪ ويعني FPG من 55 ملغ / ديسيلتر و 60 ملغ / ديسيلتر ، على التوالي. لكثير من المرضى الذين عولجوا سابقا ، HbA1C و FPG لم يعد إلى مستويات الفحص بنهاية الدراسة.
في دراسة استمرت 16 أسبوعًا ، تم اختيارهم بصورة عشوائية 197 مريضًا يعانون من مرض السكري من النوع 2 للعلاج مع 30 ملغ من الأكتوس أو الغفل مرة واحدة يوميًا. تم إيقاف العلاج مع أي عامل مضاد لمرض السكر السابق قبل 6 أسابيع من فترة التعمية المزدوجة. العلاج مع 30 ملغ من Actos أنتجت تحسينات ذات دلالة إحصائية في HbA1C و FPG في نقطة النهاية مقارنة مع الدواء الوهمي (الجدول 5).
الجدول 5 معلمات نسبة السكر في الدم في دراسة وهمي تسيطر عليها لمدة 16 أسبوعا
| الوهمي | Actos 30 ملغ مرة واحدة يوميا |
|
| مجموع السكان HBA1C (%) |
N = 93 | N = 100 |
| خط الأساس (الوسط) | 10.3 | 10.5 |
| التغيير من الأساس (المعدل المعدل)+) | 0.8 | -0.6 |
| الفرق من الدواء الوهمي (المعدل المعدل)+) | -1.4* | |
| FPG (mg / dL) | N = 91 | N = 99 |
| خط الأساس (الوسط) | 270 | 273 |
| التغيير من الأساس (المعدل المعدل)+) | 8 | -50 |
| الفرق من الدواء الوهمي (المعدل المعدل)+) | -58* | |
|
+ ضبط الأساس ، مركز المجمعة ، ومركز المجمعة عن طريق التفاعل العلاج * ع ¤ 50 0.050 مقابل الوهمي |
بالنسبة للمرضى الذين لم يعالجوا سابقًا بالأدوية المضادة لمرض السكر (40٪) ، كانت القيم المتوسطة عند الفحص هي 10.3٪ لـ HbA1c و 240 mg / dL لـ FPG. في الأساس ، يعني HBA1C كان 10.4 ٪ وكان متوسط FPG 254 ملغ / ديسيلتر. مقارنة مع الدواء الوهمي ، نتج عن العلاج باستخدام Actos 30 mg انخفاضات من خط الأساس في متوسط HbA1C من 1.0 ٪ ويعني FPG من 62 ملغ / ديسيلتر. بالنسبة للمرضى الذين سبق علاجهم بالأدوية المضادة لمرض السكر (60 ٪) ، توقف هذا الدواء عند الفحص. وكانت القيم يعني في الفحص 9.4 ٪ ل HbA1C و 216 ملغ / ديسيلتر ل FPG. في الأساس ، يعني HBA1C كان 10.6 ٪ ويعني FPG كان 287 ملغ / ديسيلتر. مقارنة مع الدواء الوهمي ، نتج عن العلاج باستخدام Actos 30 mg انخفاضات من خط الأساس في متوسط HbA1C من 1.3 ٪ ويعني FPG من 46 ملغ / ديسيلتر. لكثير من المرضى الذين عولجوا سابقا ، HbA1C و FPG لم يعد إلى مستويات الفحص بنهاية الدراسة.
الجمع بين العلاج
ثلاثة ، 16 ، والعشوائية ، مزدوجة التعمية ، الدراسات السريرية التي تسيطر عليها وهمي وثلاثة 24 أسبوعا ، العشوائية ، مزدوجة التعمية ، التي تسيطر عليها الجرعة أجريت دراسات سريرية لتقييم آثار اكتوس على السيطرة على نسبة السكر في الدم في المرضى الذين يعانون من مرض السكري من النوع 2 الذين كانوا غير كافيين تسيطر (HBA1C • 8 ٪) على الرغم من العلاج الحالي مع السلفونيل يوريا ، الميتفورمين ، أو الأنسولين. قد يكون علاج مرض السكري السابق علاج أحادي أو مركب.
Actos Plus دراسات السلفونيل يوريا
أجريت دراستان سريريتان مع أكتوس بالاشتراك مع سلفونيل يوريا. شملت كلتا الدراستين مرضى السكري من النوع 2 على سلفونيل يوريا ، إما بمفردهم أو بالاشتراك مع عامل مضاد لمرض السكر آخر. تم سحب جميع العوامل المضادة لمرض السكر قبل بدء دراسة العلاج. في الدراسة الأولى ، تم اختيارهم بصورة عشوائية 560 مريضا لتلقي 15 ملغ أو 30 ملغ من Actos أو وهمي مرة واحدة يوميا لمدة 16 أسبوعا بالإضافة إلى نظام السلفونيل يوريا الحالي. عند مقارنة الدواء الوهمي في الأسبوع 16 ، فإن إضافة Actos إلى السلفونيل يوريا قللت بشكل كبير من متوسط HbA1C بنسبة 0.9 ٪ و 1.3 ٪ ويعني FPG بنسبة 39 ملغ / ديسيلتر و 58 ملغ / ديسيلتر للجرعة 15 ملغ و 30 ملغ ، على التوالي.
في الدراسة الثانية ، تم اختيارهم بصورة عشوائية 702 مريضا لتلقي 30 ملغ أو 45 ملغ من Actos مرة واحدة يوميا لمدة 24 أسبوعا بالإضافة إلى نظام السلفونيل يوريا الحالي. التخفيضات المتوسطة من خط الأساس في الأسبوع 24 في HbA1C كانت 1.55 ٪ و 1.67 ٪ للجرعات 30 ملغ و 45 ملغ ، على التوالي. وكان متوسط التخفيضات من خط الأساس في FPG 51.5 ملغ / ديسيلتر و 56.1 ملغ / ديسيلتر.
لوحظ التأثير العلاجي لـ Actos مع السلفونيل يوريا في المرضى بغض النظر عما إذا كان المرضى يتلقون جرعات منخفضة أو متوسطة أو عالية من السلفونيل يوريا.
اكتوس بلس دراسات الميتفورمين
أجريت دراستان سريريتان مع أكتوس بالاشتراك مع الميتفورمين. شملت كلتا الدراستين مرضى السكري من النوع 2 على الميتفورمين ، إما بمفردهم أو مع عامل مضاد لمرض السكر آخر. تم سحب جميع العوامل المضادة لمرض السكر قبل بدء دراسة العلاج. في الدراسة الأولى ، تم اختيارهم بصورة عشوائية 328 مريضا لتلقي إما 30 ملغ من Actos أو وهمي مرة واحدة يوميا لمدة 16 أسبوعا بالإضافة إلى نظام الميتفورمين الحالي. عند مقارنة الدواء الوهمي في الأسبوع 16 ، فإن إضافة Actos إلى الميتفورمين قد قللت بشكل كبير متوسط HbA1C بنسبة 0.8 ٪ وانخفض متوسط FPG بنسبة 38 ملغ / ديسيلتر.
في الدراسة الثانية ، تم اختيارهم بصورة عشوائية 827 مريضا لتلقي إما 30 ملغ أو 45 ملغ من Actos مرة واحدة يوميا لمدة 24 أسبوعا بالإضافة إلى نظام الميتفورمين الحالي. التخفيضات المتوسطة من خط الأساس في الأسبوع 24 في HbA1C كانت 0.80 ٪ و 1.01 ٪ للجرعات 30 ملغ و 45 ملغ ، على التوالي. وكان متوسط التخفيضات من خط الأساس في FPG 38.2 ملغ / ديسيلتر و 50.7 ملغ / ديسيلتر.
لوحظ التأثير العلاجي لـ Actos بالاشتراك مع الميتفورمين في المرضى بغض النظر عما إذا كان المرضى يتلقون جرعات منخفضة أو أعلى من الميتفورمين.
Actos Plus دراسات الأنسولين
أجريت دراستان سريريتان مع أكتوس بالاشتراك مع الأنسولين. شملت كلتا الدراستين مرضى السكري من النوع 2 على الأنسولين ، إما بمفردهم أو مع عامل مضاد لمرض السكر آخر. تم سحب جميع العوامل المضادة لمرض السكر قبل بدء دراسة العلاج. في الدراسة الأولى ، تم اختيارهم بصورة عشوائية 566 مريضا تلقي وسيط من 60.5 وحدة من الأنسولين يوميا احصل على 15 ملغ أو 30 ملغ من أكتوس أو دواء وهمي مرة واحدة يوميًا لمدة 16 أسبوعًا بالإضافة إلى الأنسولين حمية. عند مقارنة الدواء الوهمي في الأسبوع 16 ، فإن إضافة Actos إلى الأنسولين قللت بشكل كبير كلا HbA1C بنسبة 0.7 ٪ و 1.0 ٪ و FPG بنسبة 35 ملغ / ديسيلتر و 49 ملغ / ديسيلتر للجرعة 15 ملغ و 30 ملغ ، على التوالي.
في الدراسة الثانية ، تلقى 690 مريضًا يتلقون معدل 60.0 وحدة يوميًا من الأنسولين إما 30 ملغ أو 45 ملغ من الأكتوس مرة واحدة يوميًا لمدة 24 أسبوعًا بالإضافة إلى نظام الأنسولين الحالي. التخفيضات المتوسطة من خط الأساس في الأسبوع 24 في HbA1C كانت 1.17 ٪ و 1.46 ٪ للجرعات 30 ملغ و 45 ملغ ، على التوالي. وكان متوسط التخفيضات من خط الأساس في FPG 31.9 ملغ / ديسيلتر و 45.8 ملغ / ديسيلتر. رافق تحسن السيطرة على نسبة السكر في الدم من انخفاض متوسط من خط الأساس في متطلبات جرعة الأنسولين من 6.0 ٪ و 9.4 ٪ في اليوم لجرعة 30 ملغ و 45 ملغ ، على التوالي.
لوحظ التأثير العلاجي لـ Actos بالاقتران مع الأنسولين لدى المرضى بغض النظر عما إذا كان المرضى يتلقون جرعات منخفضة أو أعلى من الأنسولين.
أعلى
المؤشرات والاستخدام
يشار إلى Actos كعامل مساعد في النظام الغذائي وممارسة التمارين الرياضية لتحسين السيطرة على نسبة السكر في الدم لدى البالغين الذين يعانون من داء السكري من النوع 2.
أعلى
موانع
هو بطلان الشروع في اكتوس في المرضى الذين يعانون من فشل القلب المنشأة في نيويورك جمعية القلب (NYHA) من الدرجة الثالثة أو الرابعة (انظر تحذير محاصر).
موانع الأكتوس في المرضى الذين يعانون من فرط الحساسية المعروف لهذا المنتج أو أي من مكوناته.
أعلى
تحذيرات
فشل القلب والآثار القلبية الأخرى
الأكتوز ، مثل الثيازيدوليدينونات الأخرى ، يمكن أن يسبب احتباس السوائل عند استخدامه بمفرده أو بالاشتراك مع عوامل أخرى مضادة لمرض السكر ، بما في ذلك الأنسولين. احتباس السوائل قد يؤدي إلى أو يؤدي إلى تفاقم قصور القلب. يجب مراعاة المرضى للعلامات وأعراض قصور القلب. إذا تطورت هذه العلامات والأعراض ، فيجب إدارة قصور القلب وفقًا للمعايير الحالية للرعاية. وعلاوة على ذلك ، يجب النظر في وقف أو تخفيض جرعة من Actos (انظر تحذير محاصر). لم تتم دراسة المرضى الذين يعانون من حالة القلب NYHA من الدرجة الثالثة والرابعة خلال تجارب سريرية قبل الموافقة ولم ينصح Actos في هؤلاء المرضى (انظر تحذير محاصر و موانع).
في تجربة واحدة استمرت 16 أسبوعًا في الولايات المتحدة ، تم إجراء تجربة سريرية مزدوجة التعمية وهمي تسيطر عليها الولايات المتحدة ، شملت 566 مريضًا من النوع الثاني تم مقارنة مرض السكري ، اكتوس بجرعات 15 ملغ و 30 ملغ في تركيبة مع الأنسولين لعلاج الأنسولين وحده. شملت هذه التجربة المرضى الذين يعانون من مرض السكري منذ فترة طويلة وارتفاع معدل انتشار الحالات الطبية الموجودة على النحو التالي: ارتفاع ضغط الدم الشرياني (57.2 ٪) ، الاعتلال العصبي المحيطي (22.6 ٪) ، وأمراض القلب التاجية (19.6 ٪) ، اعتلال الشبكية (13.1 ٪) ، عضلة القلب احتشاء (8.8 ٪) ، مرض الأوعية الدموية (6.4 ٪) ، الذبحة الصدرية (4.4 ٪) ، والسكتة الدماغية و / أو نوبة نقص تروية عابرة (4.1 ٪) ، واحتقان فشل القلب (2.3 ٪).
في هذه الدراسة ، اثنان من 191 مريضًا تلقوا 15 ملغ من أكتوس بالإضافة إلى الأنسولين (1.1٪) واثنان من بين 188 مريضًا تلقوا 30 ملغ طور اكتوس بلس الأنسولين (1.1 ٪) قصور القلب الاحتقاني مقارنة مع أي من مرضى الـ 187 الذين تناولوا العلاج بالأنسولين وحده. كل هؤلاء المرضى الأربعة لديهم تاريخ سابق في أمراض القلب والأوعية الدموية بما في ذلك مرض الشريان التاجي ، وإجراءات CABG السابقة ، واحتشاء عضلة القلب. في دراسة استمرت 24 أسبوعًا ، تم فيها التحكم في الجرعة ، والتي تم فيها تناول أكستوس مع الأنسولين ، أبلغ 0.3٪ من المرضى (1/345) على 30 مجم و 0.9٪ (3/345) من المرضى على 45 مجم عن CHF كحدث ضار خطير .
لم يحدد تحليل البيانات المستقاة من هذه الدراسات عوامل محددة تتنبأ بزيادة خطر الإصابة بفشل القلب الاحتقاني عند الجمع بين العلاج بالأنسولين.
في النوع 2 من مرض السكري وفشل القلب الاحتقاني (ضعف الانقباضي)
تم إجراء دراسة أمان بعد التسويق مدتها 24 أسبوعًا لمقارنة Actos (n = 262) إلى glyburide (n = 256) في مرضى السكري غير المنضبطين (يعني HbA)1C 8.8 ٪ في الأساس) مع فشل NYHA من الدرجة الثانية والثالثة في القلب وكسر طرد أقل من 40 ٪ (يعني EF 30 ٪ في الأساس). على مدار الدراسة ، تم الإبلاغ عن ليلة وضحاها في المستشفى لفشل القلب الاحتقاني في 9.9 ٪ من المرضى على Actos مقارنة مع 4.7 ٪ من المرضى على glyburide مع وجود اختلاف في العلاج لوحظ من 6 أسابيع. تم تمييز هذا الحدث الضار المرتبط بالإكتوس في المرضى الذين يستخدمون الأنسولين في الأساس وفي المرضى الذين تزيد أعمارهم عن 64 عامًا. لم يلاحظ أي اختلاف في وفيات القلب والأوعية الدموية بين مجموعات العلاج.
يجب أن تبدأ الأكتوس بأقل جرعة معتمدة إذا تم وصفه للمرضى المصابين بالسكري من النوع الثاني وفشل القلب الانقباضي (NYHA Class II). إذا كان تصاعد الجرعة اللاحق ضروريًا ، فينبغي زيادة الجرعة تدريجياً فقط بعد عدة جرعات أشهر من العلاج مع مراقبة دقيقة لزيادة الوزن ، وذمة ، أو علامات وأعراض فرنك سويسري تفاقم.
المحتملين تجربة بيوجليتازون السريرية في أحداث الأوعية الدموية (استباقية)
في PROactive ، عولج 5238 مريضًا من النوع 2 من مرض السكري وتاريخ سابق من مرض الأوعية الدموية الكبيرة بالاكتوز (ن = 2605) ، ومعايرهم بقوة تصل إلى 45 ملغ مرة واحدة يوميًا ، أو وهمي (ن = 2633) (انظر ردود الفعل الضارة). كانت النسبة المئوية للمرضى الذين أصيبوا بقصور قلبي خطير أعلى للمرضى الذين عولجوا بـ Actos (5.7٪ ، n = 149) مقارنة بالمرضى الذين عولجوا بدواء وهمي (4.1٪ ، ن = 108). كانت نسبة الوفاة التي أعقبت الإبلاغ عن فشل خطير في القلب 1.5 ٪ (ن = 40) في المرضى الذين عولجوا مع Actos و 1.4 ٪ (ن = 37) في المرضى الذين عولجوا بالدواء الوهمي. في المرضى الذين عولجوا بنظام يحتوي على الأنسولين في الأساس ، كانت نسبة الإصابة بفشل القلب الخطير 6.3 ٪ (ن = 54/864) مع اكتوس و 5.2 ٪ (ن = 47/896) مع الدواء الوهمي. بالنسبة لأولئك المرضى الذين عولجوا بنظام يحتوي على السلفونيل يوريا في الأساس ، كان معدل الإصابة بفشل القلب الخطير 5.8 ٪ (ن = 94/1624) مع اكتوس و 4.4 ٪ (ن = 71/1626) مع الدواء الوهمي.
أعلى
الاحتياطات
جنرال لواء
Actos يمارس تأثيره الخافض لنسبة السكر في الدم فقط في وجود الأنسولين. لذلك ، لا ينبغي أن تستخدم Actos في المرضى الذين يعانون من مرض السكري من النوع 1 أو لعلاج الحماض الكيتوني السكري.
نقص السكر في الدم: قد يتعرض المرضى الذين يتلقون أكتوس بالاقتران مع الأنسولين أو عوامل نقص السكر في الدم عن طريق الفم لخطر الإصابة بنقص السكر في الدم ، وقد يكون من الضروري تخفيض جرعة العامل المصاحب.
القلب والأوعية الدموية: في التجارب السريرية التي تسيطر عليها وهمي الولايات المتحدة التي استبعدت المرضى الذين يعانون من حالة القلب من الدرجة الثالثة والرابع جمعية نيويورك (NYHA) الرابع ، وقوع لم يتم زيادة الأحداث السلبية الخطيرة في القلب المرتبطة بزيادة حجم في المرضى الذين عولجوا مع Actos كعلاج وحيد أو بالاشتراك مع السلفونيل يوريا أو الميتفورمين ضد. مرضى العلاج الوهمي. في دراسات تركيبة الأنسولين ، يوجد عدد قليل من المرضى الذين لديهم تاريخ سابق مرض القلب تطور قصور القلب الاحتقاني عند علاجه مع أكتوس بالاشتراك مع الأنسولين (نرى تحذيرات). لم تتم دراسة المرضى الذين يعانون من حالة القلب NYHA من الدرجة الثالثة والرابعة في هذه التجارب السريرية Actos. لا يشار إلى Actos في المرضى الذين يعانون من حالة القلب NYHA من الدرجة الثالثة أو الرابع.
في تجربة ما بعد البيع مع Actos ، تم الإبلاغ عن حالات قصور القلب الاحتقاني في المرضى الذين يعانون من أو بدون أمراض القلب المعروفة سابقًا.
الوذمة: يجب استخدام أكتو بحذر في المرضى الذين يعانون من الوذمة. في جميع التجارب السريرية في الولايات المتحدة ، تم الإبلاغ عن الوذمة في كثير من الأحيان في المرضى الذين عولجوا بـ Actos أكثر من المرضى الذين عولجوا بالعلاج الوهمي ويبدو أنهم مرتبطون بالجرعة (انظر ردود الفعل الضارة). في تجربة ما بعد التسويق ، تم تلقي تقارير عن بدء أو تفاقم الوذمة. نظرًا لأن الثيازيدوليديون ، بما في ذلك Actos ، يمكن أن يسبب احتباس السوائل ، والذي يمكن أن يؤدي إلى تفاقم أو يؤدي إلى قصور القلب الاحتقاني ، يجب استخدام Actos بحذر في المرضى المعرضين لخطر قصور القلب. يجب مراقبة المرضى بحثًا عن علامات وأعراض قصور القلب (انظر تحذير محاصر, تحذيراتو احتياطات).
زيادة الوزن: شوهد زيادة الوزن المرتبطة بالجرعة مع أكتوس وحده وبالاقتران مع عوامل سكر الدم الأخرى (الجدول 6). آلية زيادة الوزن غير واضحة ولكن ربما تتضمن مجموعة من احتباس السوائل وتراكم الدهون.
الجدول 6 التغييرات في الوزن (كلغ) من خط الأساس خلال التجارب السريرية مزدوجة التعمية مع Actos
| مجموعة التحكم (الوهمي) |
أكتوس 15 ملغ |
أكتوس 30 ملغ |
أكتوس 45 ملغ |
||
| الوسيط (25العاشر/75العاشر المئوية) |
الوسيط (25العاشر/75العاشر المئوية) |
الوسيط (25العاشر/75العاشر المئوية) |
الوسيط (25العاشر/75العاشر المئوية) |
||
| وحيد | -1.4 (-2.7/0.0) ن = 256 |
0.9(-0.5/3.4) ن = 79 |
1.0(-0.9/3.4) ن = 188 |
2.6 (0.2/5.4) ن = 79 |
|
| الجمع بين العلاج | السلفونيل يوريا | -0.5 (-1.8/0.7) ن = 187 |
2.0 (0.2/3.2) ن = 183 |
3.1 (1.1/5.4) ن = 528 |
4.1 (1.8/7.3) ن = 333 |
| ميتفورمين | -1.4 (-3.2/0.3) ن = 160 |
N / A | 0.9(-0.3/3.2) ن = 567 |
1.8(-0.9/5.0) ن = 407 |
|
| الأنسولين | 0.2 (-1.4/1.4) ن = 182 |
2.3 (0.5/4.3) ن = 190 |
3.3 (0.9/6.3) ن = 522 |
4.1 (1.4/6.8) ن = 338 |
|
| ملاحظة: فترات المحاكمة من 16 إلى 26 أسبوعا |
الإباضة: قد يؤدي العلاج بالاكتوز ، مثل الثيازيدوليدينينات الأخرى ، إلى الإباضة في بعض النساء اللاتي يسبن انقطاع الطمث. نتيجة لذلك ، قد يكون هؤلاء المرضى في خطر متزايد للحمل أثناء تناولهم Actos. وبالتالي ، ينبغي التوصية وسائل منع الحمل المناسبة في النساء قبل انقطاع الطمث. لم يتم التحقيق في هذا التأثير المحتمل في الدراسات السريرية ، وبالتالي فإن تواتر حدوث هذا غير معروف.
أمراض الدم: الأكتوس قد يسبب انخفاضا في الهيموغلوبين والهيماتوكريت. في جميع الدراسات السريرية ، يعني انخفاض قيم الهيموغلوبين بنسبة 2 ٪ إلى 4 ٪ في المرضى الذين عولجوا مع Actos. حدثت هذه التغييرات في المقام الأول خلال أول 4 إلى 12 أسبوعًا من العلاج وظلت ثابتة نسبيًا بعد ذلك. قد تكون هذه التغييرات مرتبطة بزيادة حجم البلازما ونادرا ما ترتبط بأي آثار سريرية دموية كبيرة (انظر ردود الفعل الضارةتشوهات المختبر.
التأثيرات الكبدية: في الدراسات السريرية التي تمت الموافقة عليها مسبقًا في جميع أنحاء العالم ، تم علاج أكثر من 4500 شخصًا باستخدام أكتوس. في الدراسات السريرية الأمريكية ، تلقى أكثر من 4700 مريض يعانون من مرض السكري من النوع 2 Actos. لم يكن هناك دليل على تسمم الكبد الناجم عن المخدرات أو ارتفاع مستويات ALT في الدراسات السريرية.
أثناء التجارب السريرية التي يتم التحكم فيها مسبقًا عن طريق الدواء الوهمي في الولايات المتحدة ، أي ما مجموعه 4 من 1526 (0.26٪) من المرضى تعامل مع Actos وكان 2 من 793 (0.25 ٪) من المرضى الذين عولجوا بالدواء الوهمي قيم ALT - 3 أضعاف الحد العلوي لل عادي. كانت ارتفاعات ALT في المرضى الذين عولجوا بـ Actos قابلة للانعكاس ولم تكن مرتبطة بشكل واضح بالعلاج مع Actos.
في تجربة ما بعد البيع مع Actos ، تم تلقي تقارير عن التهاب الكبد وارتفاع الإنزيمات الكبدية إلى 3 أضعاف مرات الحد الأعلى الطبيعي. نادرًا ما تتضمن هذه التقارير فشل كبدي مع أو بدون نتيجة مميتة ، على الرغم من عدم وجود علاقة سببية.
في انتظار توافر نتائج تجارب سريرية إضافية كبيرة وطويلة الأجل ومضبوطة بيانات السلامة لما بعد التسويق ، فمن المستحسن أن يخضع المرضى الذين عولجوا بـ Actos لمراقبة دورية للكبد الانزيمات.
يجب تقييم مستويات مصل ALT (alanine aminotransferase) قبل بدء العلاج مع اكتوس في جميع المرضى وبشكل دوري بعد ذلك حسب الحكم السريري للرعاية الصحية المحترفين. يجب أيضًا إجراء اختبارات وظائف الكبد للمرضى في حالة حدوث أعراض توحي بخلل وظيفي كبدي ، مثل الغثيان أو القيء أو آلام في البطن أو التعب أو فقدان الشهية أو البول الداكن. ينبغي أن يسترشد قرار ما إذا كان ينبغي مواصلة المريض على العلاج مع Actos بالحكم السريري في انتظار التقييمات المختبرية. إذا لوحظت اليرقان ، يجب التوقف عن العلاج بالعقاقير.
لا ينبغي البدء بالعلاج باستخدام Actos إذا أظهر المريض أدلة سريرية على مرض الكبد النشط أو تجاوزت مستويات ALT 2.5 مرة الحد الأعلى الطبيعي. المرضى الذين يعانون من إنزيمات الكبد المرتفعة بشكل معتدل (مستويات ALT بمعدل يتراوح بين 1 و 2.5 ضعف الحد الطبيعي الطبيعي) يجب تقييم خط الأساس أو في أي وقت أثناء العلاج مع Actos لتحديد سبب إنزيم الكبد ارتفاع. يجب البدء في بدء العلاج أو استمراره مع أكتوس في المرضى الذين يعانون من أنزيمات الكبد المرتفعة بشكل خفيف بحذر وتشمل المتابعة السريرية المناسبة التي قد تشمل أنزيم الكبد أكثر تواترا الرصد. إذا تم زيادة مستويات المصل الترانساميناز في المصل (ALT> 2.5 أضعاف الحد الأعلى الطبيعي) ، الكبد يجب تقييم اختبارات الوظيفة بشكل أكثر تواترا حتى تعود المستويات إلى طبيعتها أو قبل المعالجة القيم. إذا تجاوزت مستويات ALT 3 أضعاف الحد الأعلى الطبيعي ، فيجب تكرار الاختبار في أقرب وقت ممكن. إذا بقيت مستويات ALT> 3 أضعاف الحد الأعلى الطبيعي أو إذا كان المريض مصابًا باليرقان ، فيجب إيقاف علاج Actos.
وذمة البقعة الصفراء: تم الإبلاغ عن وذمة البقعة الصفراء في تجربة ما بعد التسويق في مرضى السكري الذين كانوا يتناولون البيوجليتازون أو ثيازيدوليدين آخر. بعض المرضى الذين يعانون من عدم وضوح الرؤية أو انخفاض حدة البصر ، ولكن يبدو أن بعض المرضى قد تم تشخيصهم في فحص طب العيون الروتيني. وكان بعض المرضى وذمة محيطية في وقت تم تشخيص وذمة البقعة الصفراء. كان بعض المرضى تحسنا في وذمة البقعة الصفراء بعد التوقف عن ثيازوليدينيوني بهم. من غير المعروف ما إذا كانت هناك علاقة سببية بين البيوجليتازون وذمة البقعة الصفراء أم لا. يجب على مرضى السكري إجراء فحوصات منتظمة للعين من قبل طبيب عيون ، وفقًا لمعايير الرعاية التابعة للجمعية الأمريكية للسكري. بالإضافة إلى ذلك ، يجب إحالة أي مرض السكري الذي يبلغ عن أي نوع من الأعراض البصرية على الفور إلى طبيب عيون ، بغض النظر عن الأدوية الأساسية للمريض أو غيرها من النتائج الجسدية (انظر ردود الفعل الضارة).
الكسور: في تجربة عشوائية (استباقية) في المرضى الذين يعانون من مرض السكري من النوع 2 (متوسط مدة داء السكري 9.5 سنوات) ، لوحظ حدوث زيادة في كسر العظام لدى النساء اللائي يتناولن بيوجليتازوني. خلال فترة المتابعة المتوسطة البالغة 34.5 شهرًا ، كانت نسبة حدوث كسر العظام عند الإناث 5.1٪ (44/870) للبيوجليتازون مقابل 2.5٪ (23/905) للعلاج الوهمي. وقد لوحظ هذا الاختلاف بعد السنة الأولى من العلاج وبقي خلال فترة الدراسة. وكانت غالبية الكسور التي لوحظت في المرضى الإناث كسور غير فقارية بما في ذلك الطرف السفلي والطرف العلوي البعيد. لم يلاحظ أي زيادة في معدلات الكسر في الرجال الذين عولجوا بيوجليتازون 1.7 ٪ (30/1735) مقابل الدواء الوهمي 2.1 ٪ (37/1728). يجب مراعاة خطر الكسر في رعاية المرضى ، وخاصة المرضى الإناث ، الذين تم علاجهم به ينبغي إعطاء البيوجليتازون والاهتمام لتقييم صحة العظام والحفاظ عليها وفقًا للمعايير الحالية الرعاية.
نتائج الأوعية الدموية الكبرى: لم تكن هناك دراسات سريرية تثبت وجود أدلة قاطعة على الحد من مخاطر الأوعية الدموية الكبيرة مع الأكتوس أو أي أدوية أخرى لمكافحة مرض السكري.
اختبارات المعمل
FPG و HbA1C يجب إجراء القياسات بشكل دوري لمراقبة مراقبة نسبة السكر في الدم والاستجابة العلاجية ل Actos.
يوصى بمراقبة إنزيم الكبد قبل الشروع في العلاج باستخدام الأكتوس في جميع المرضى وبعد ذلك بشكل دوري وفقًا للحكم السريري لأخصائي الرعاية الصحية (انظر احتياطات، عام ، آثار الكبد و ردود الفعل الضارةمستويات مصل الترانساميناز).
معلومات للمرضى
من المهم أن نطلب من المرضى الالتزام بالتعليمات الغذائية وأن يتم فحص نسبة الجلوكوز في الدم والهيموغلوبين الغليكوزيلاتي بانتظام. خلال فترات التوتر مثل الحمى أو الصدمة أو العدوى أو الجراحة ، قد تتغير متطلبات الدواء ويجب تذكير المرضى بطلب المشورة الطبية على الفور.
المرضى الذين يعانون من زيادة سريعة أو غير عادية في الوزن أو الوذمة أو الذين يعانون من ضيق في التنفس أو غيرها من أعراض قصور القلب بينما على Actos ينبغي على الفور الإبلاغ عن هذه الأعراض لهم الطبيب المعالج.
يجب إخبار المرضى أنه سيتم إجراء اختبارات الدم الخاصة بوظيفة الكبد قبل بدء العلاج وبعد ذلك بشكل دوري وفقًا للحكم السريري لأخصائي الرعاية الصحية. يجب إخبار المرضى بطلب المشورة الطبية الفورية بشأن الغثيان أو القيء أو آلام البطن أو التعب أو فقدان الشهية أو البول الداكن.
يجب إخبار المرضى بتناول أكتوس مرة يوميًا. يمكن أن تؤخذ Actos مع أو بدون وجبات الطعام. إذا فاتت جرعة في يوم واحد ، لا ينبغي مضاعفة الجرعة في اليوم التالي.
عند استخدام العلاج المركب مع الأنسولين أو عوامل سكر الدم عن طريق الفم ، فإن مخاطر نقص السكر في الدم وأعراضه و العلاج ، والظروف التي تهيئ لتطويره يجب أن تشرح للمرضى وأسرهم أفراد.
قد يؤدي العلاج بالاكتوز ، مثل الثيازيدوليدينينات الأخرى ، إلى الإباضة في بعض النساء اللاتي يسبن انقطاع الطمث. نتيجة لذلك ، قد يكون هؤلاء المرضى في خطر متزايد للحمل أثناء تناولهم Actos. وبالتالي ، ينبغي التوصية وسائل منع الحمل المناسبة في النساء قبل انقطاع الطمث. لم يتم التحقيق في هذا التأثير المحتمل في الدراسات السريرية ، وبالتالي فإن تواتر حدوث هذا غير معروف.
تفاعل الأدوية
في دراسات التفاعل بين الدواء والعقار في الجسم الحي ، اقترحت أن البيوجليتازون قد يكون محفزًا ضعيفًا للركيزة CYP 450 isoform 3A4 (انظر صيدلية سريريةالأيض و المخدرات المخدرات التفاعلات).
مثبط الإنزيم لـ CYP2C8 (مثل جيمفيبروزيل) قد يزيد بشكل كبير من البيوجليتازون ومحفز الإنزيم لـ CYP2C8 (مثل ريفامبين) قد يقلل بشكل كبير من بيوجليتازوني. لذلك ، إذا تم بدء أو إيقاف مثبط أو محفز CYP2C8 أثناء العلاج بالبيوجليتازون ، فقد تكون هناك حاجة إلى تغييرات في علاج مرض السكري بناءً على الاستجابة السريرية (انظر صيدلية سريرية, المخدرات المخدرات التفاعلات).
التسرطن ، الطفرات ، ضعف الخصوبة
أجريت دراسة سرطانية مدتها سنتان على فئران ذكور وإناث عند جرعات عن طريق الفم تصل إلى 63 مغ / كغ (حوالي 14 ضعف الحد الأقصى الموصى به للجرعة الفموية البشرية البالغة 45 ملغ بناءً على ملغم / م 2). لم يلاحظ وجود أورام مستحثة بالعقاقير في أي عضو باستثناء المثانة البولية. لوحظت أورام الخلايا الانتقالية الحميدة و / أو الخبيثة في فئران ذكور عند 4 مغ / كغ / يوم وما فوق (مساوية تقريبًا للجرعة الفموية القصوى الموصى بها على أساس ملغم / م 2). أجريت دراسة سرطانية مدتها سنتان على الفئران من الذكور والإناث بجرعات تصل إلى 100 ملغ / كغ / يوم (حوالي 11 ضعفًا الجرعة البشرية الموصى بها عن طريق الفم بناءً على mg / m2). لم يلاحظ أي الأورام التي يسببها المخدرات في أي عضو.
أثناء التقييم المستقبلي للخلايا البولية التي تشمل أكثر من 1800 مريض يتلقون اكتوس في تجارب سريرية تصل إلى سنة واحدة في المدة ، لم يتم تحديد أي حالات جديدة من أورام المثانة. في دراستين مدتهما 3 سنوات تم فيها مقارنة البيوجليتازون بالغفل أو الغليبيريد ، كان هناك 16/3656 (0.44٪) تقارير عن سرطان المثانة في المرضى الذين يتناولون البيوجليتازون مقارنة بـ 5/3679 (0.14٪) في المرضى الذين لا يتناولون بيوجليتازوني. بعد استبعاد المرضى الذين كان التعرض لدراسة المخدرات أقل من عام واحد في وقت تشخيص سرطان المثانة ، كانت هناك ست حالات (0.16 ٪) على البيوجليتازون وحالتين (0.05 ٪) على الدواء الوهمي.
لم يكن بيوغليتازون حمض الهيدروكلوريك طفرات في مجموعة من دراسات علم السموم الوراثية ، بما في ذلك اختبار البكتريا الخاص بـ Ames ، وهو جين أمام خلية الثدييات فحص الطفرة (CHO / HPRT و AS52 / XPRT) ، مقايسة الوراثة الخلوية المختبرية باستخدام خلايا CHL ، مقايسة توليف الحمض النووي غير المجدولة ، ونواة في الجسم الحي فحص.
لم تلاحظ أي آثار ضارة على الخصوبة لدى فئران ذكور وإناث عند الجرعات الفموية التي تصل إلى 40 ميلي غرام لكل كيلوغرام من البيوجليتازون حمض الهيدروكلوريك يومياً قبل وطوال التزاوج والحمل (حوالي 9 أضعاف الحد الأقصى الموصى به للجرعة عن طريق الفم البشرية على أساس ملغ / م 2).
علم السموم الحيوانية
لوحظ تضخم القلب في الفئران (100 ملغ / كلغ) ، الفئران (4 ملغ / كلغ وما فوق) والكلاب (3 ملغ / كلغ) تعامل شفويا بيوجليتازون حمض الهيدروكلوريك (حوالي 11 ، 1 ، و 2 أضعاف الجرعة البشرية الموصى بها عن طريق الفم للفئران والجرذان والكلاب ، على التوالي ، على أساس ملغ / م2). في دراسة أجريت على الفئران لمدة عام واحد ، حدثت الوفاة المبكرة ذات الصلة بالمخدرات بسبب اختلال وظيفي في القلب جرعة عن طريق الفم من 160 ملغ / كغ / يوم (حوالي 35 مرة الحد الأقصى للجرعة الفموية الموصى بها على أساس الإنسان ملغ / م2). شوهد تضخم القلب في دراسة استمرت 13 أسبوعًا على القرود بجرعات عن طريق الفم بلغت 8.9 ملغم / كغم وما فوق (حوالي 4 أضعاف الحد الأقصى الموصى به للجرعة عن طريق الفم البشرية بناءً على ملغم / م2) ، ولكن ليس في دراسة مدتها 52 أسبوعًا على جرعات فموية تصل إلى 32 مجم / كجم (حوالي 13 ضعف الحد الأقصى الموصى به للجرعة الفموية البشرية على أساس ملغم / م2).
حمل
فئة الحمل C. لم يكن البيوجليتازون ماسخًا في الفئران بجرعات تصل إلى 80 مجم / كجم أو في الأرانب التي أعطيت حتى 160 ملغم / كغم أثناء تكوين الأعضاء (حوالي 17 و 40 مرة كحد أقصى الجرعة الفموية الموصى بها على أساس الإنسان على ملغ / م2، على التوالي). تأخر الولادة والسمية الجنينية (كما يتضح من زيادة فقدان ما بعد الزرع وتأخر النمو وانخفاض أوزان الجنين) وقد لوحظت في الفئران بجرعات عن طريق الفم من 40 ملغ / كغ / يوم وما فوق (حوالي 10 أضعاف الجرعة القصوى البشرية عن طريق الفم الموصى بها على أساس ملغ / م2). لم يلاحظ أي سمية وظيفية أو سلوكية في ذرية الفئران. في الأرانب ، لوحظ تسمم الأجنة بجرعة فموية تبلغ 160 ميلي غرام لكل كيلوغرام (حوالي 40 ضعف الحد الأقصى الموصى به للجرعة البشرية عن طريق الفم بناءً على ملغم / م2). ولوحظ تأخر نمو ما بعد الولادة ، ويعزى ذلك إلى انخفاض وزن الجسم ، في نسل الفئران بجرعات عن طريق الفم قدرها 10 ملغ / كغ وفوق ذلك خلال فترات الحمل والرضاعة المتأخرة (تقريبًا ضعف الحد الأقصى الموصى به من الجرعة عن طريق الفم عند الإنسان ملغ / م2).
لا توجد دراسات كافية وتسيطر عليها بشكل جيد في النساء الحوامل. لا ينبغي استخدام Actos أثناء الحمل إلا إذا كانت الفائدة المحتملة تبرر الخطر المحتمل على الجنين.
لأن المعلومات الحالية تشير بقوة إلى أن مستويات الجلوكوز في الدم غير الطبيعية أثناء الحمل ترتبط بارتفاع معدل حدوث الحالات الشاذة الخلقية ، وكذلك مع زيادة مراضة ووفيات الأطفال حديثي الولادة ، يوصي معظم الخبراء باستخدام الأنسولين أثناء الحمل للحفاظ على مستويات الجلوكوز في الدم قريبة من المعدل الطبيعي مثل ممكن.
الأمهات المرضعات
يفرز البيوجليتازون في حليب الفئران المرضعة. من غير المعروف ما إذا كان Actos يفرز في حليب الإنسان. لأن العديد من الأدوية تفرز في لبن الإنسان ، لا ينبغي أن تدار Actos إلى امرأة ترضع.
استخدام الأطفال
لم تثبت سلامة وفعالية Actos في مرضى الأطفال.
استخدام المسنين
كان ما يقرب من 500 مريض في التجارب السريرية التي تسيطر عليها وهمي من Actos 65 وأكثر. لم يلاحظ أي فروق ذات دلالة إحصائية في فعالية وسلامة بين هؤلاء المرضى والمرضى الأصغر سنا.
أعلى
ردود الفعل السلبية
تم علاج أكثر من 8500 مريض يعانون من مرض السكري من النوع 2 بالأكوس في تجارب سريرية عشوائية مزدوجة التعمية. وهذا يشمل 2605 من المرضى المعرضين لمخاطر عالية مع مرض السكري من النوع 2 تعامل مع Actos من تجربة سريرية استباقية. تم علاج أكثر من 6000 مريض لمدة 6 أشهر أو أكثر ، وأكثر من 4500 مريض لمدة عام أو أكثر. تلقى أكثر من 3000 مريض Actos لمدة سنتين على الأقل.
يوضح الجدول 7 حالات الإصابة الشاملة وأنواع الأحداث الضائرة المبلغ عنها في التجارب السريرية التي يسيطر عليها العلاج الوهمي للعلاج الأحادي Actos بجرعات 7.5 ملغ أو 15 ملغ أو 30 ملغ أو 45 ملغ مرة واحدة يوميًا.
الجدول 7 الدراسات السريرية التي تسيطر عليها وهمي من حيد اكتوس: الأحداث السلبية التي أبلغ عنها على تردد - 5 ٪ من المرضى الذين عولجوا مع اكتوس
| (٪ من المرضى) | ||
| الوهمي N = 259 |
أكتوس N = 606 |
|
| عدوى الجهاز التنفسي العلوي | 8.5 | 13.2 |
| صداع الراس | 6.9 | 9.1 |
| إلتهاب الجيب | 4.6 | 6.3 |
| ألم عضلي | 2.7 | 5.4 |
| اضطراب الأسنان | 2.3 | 5.3 |
| مرض السكري تفاقمت | 8.1 | 5.1 |
| إلتهاب البلعوم | 0.8 | 5.1 |
بالنسبة لمعظم الأحداث السلبية السريرية ، كانت الإصابة مماثلة للمجموعات التي عولجت بعلاج أكتوس الأحادي والذين عولجوا مع السلفونيل يوريا والميتفورمين والأنسولين. كانت هناك زيادة في حدوث وذمة في المرضى الذين عولجوا مع Actos والأنسولين مقارنة بالأنسولين وحده.
في 16 أسبوعًا ، تجربة الأنسوس التي تم التحكم فيها بواسطة الدواء الوهمي ، بالإضافة إلى تجربة الأنسولين (ن = 379) ، تم علاج 10 مرضى باستخدام أكتوس بلس تطور الأنسولين ضيق التنفس وكذلك ، في مرحلة ما أثناء العلاج ، وضعت إما تغيير الوزن أو الوذمة. تلقى سبعة من هؤلاء المرضى 10 مدرات البول لعلاج هذه الأعراض. لم يتم الإبلاغ عن ذلك في مجموعة الأنسولين بالإضافة إلى الدواء الوهمي.
كانت نسبة حالات الانسحاب من التجارب السريرية التي تسيطر عليها وهمي بسبب حدث سلبي آخر من ارتفاع السكر في الدم مماثلة للمرضى الذين عولجوا بالدواء الوهمي (2.8 ٪) أو Actos (3.3 ٪).
في دراسات العلاج المركب التي يتم التحكم فيها إما مع سلفونيل يوريا أو الأنسولين ، تم الإبلاغ عن نقص سكر الدم الخفيف إلى المتوسط ، والذي يبدو أنه مرتبط بالجرعة ، (انظر احتياطات، العام ، نقص السكر في الدم و الجرعة والإدارة، الجمع بين العلاج).
في الدراسات الأمريكية مزدوجة التعمية ، تم الإبلاغ عن فقر الدم في حوالي 2٪ من المرضى الذين عولجوا بـ Actos plus سلفونيل يوريا أو ميتفورمين أو أنسولين (انظر احتياطات، العام ، أمراض الدم).
في الدراسات أحادية ، تم الإبلاغ عن وذمة 4.8 ٪ (مع جرعات من 7.5 ملغ إلى 45 ملغ) من المرضى الذين عولجوا مع Actos مقابل 1.2 ٪ من المرضى الذين عولجوا بالدواء الوهمي. في دراسات العلاج المركب ، تم الإبلاغ عن وذمة لـ 7.2٪ من المرضى الذين عولجوا بـ Actos والسلفونيل يوريا مقارنة بـ 2.1٪ من المرضى على السلفونيل يوريا وحدهم. في دراسات العلاج المركب مع الميتفورمين ، تم الإبلاغ عن وذمة في 6.0٪ من المرضى الذين خضعوا للعلاج المركب مقابل 2.5٪ من المرضى على الميتفورمين وحدهم. في دراسات العلاج المركب مع الأنسولين ، تم الإبلاغ عن ذمة في 15.3 ٪ من المرضى على العلاج المركب مقارنة مع 7.0 ٪ من المرضى على الأنسولين وحده. واعتبرت معظم هذه الأحداث خفيفة أو معتدلة في شدتها (انظر احتياطات، الجنرال ، وذمة).
في تجربة سريرية دامت 16 أسبوعًا للعلاج المركب من الأنسولين بالإضافة إلى Actos ، أصيب عدد أكبر من المرضى بفشل القلب الاحتقاني على العلاج المركب (1.1٪) مقارنةً بعدم إجراء أي علاج على الأنسولين وحده (انظر تحذيراتقصور القلب والآثار القلبية الأخرى.
المحتملين تجربة بيوجليتازون السريرية في أحداث الأوعية الدموية (استباقية)
في استباقية ، كان 5238 مريضا يعانون من مرض السكري من النوع 2 وتاريخ سابق من مرض الأوعية الدموية الكبرى تعامل مع Actos (ن = 2605) ، قوة المعايرة تصل إلى 45 ملغ يوميا أو وهمي (ن = 2633) بالإضافة إلى معيار الرعاية. تقريبا جميع المواضيع (95 ٪) كانوا يتلقون أدوية القلب والأوعية الدموية (حاصرات بيتا ، مثبطات ACE ، ARBs ، حاصرات قنوات الكالسيوم ، النترات ، مدرات البول ، الأسبرين ، الستاتين ، الفيبات). كان لدى المرضى متوسط عمر 61.8 عامًا ، متوسط مدة الإصابة بمرض السكري 9.5 عام ، ونسبة HbA1c 8.1٪. كان متوسط مدة المتابعة 34.5 أشهر. كان الهدف الأساسي من هذه التجربة هو دراسة تأثير Actos على الوفيات و اعتلال الأوعية الدموية في المرضى الذين يعانون من داء السكري من النوع 2 الذين كانوا في خطر كبير ل أحداث الأوعية الدموية الكبرى. كان متغير الفعالية الأساسي هو الوقت المناسب لأول ظهور لأي حدث في نقطة نهاية مركب القلب والأوعية الدموية (انظر الجدول 8 أدناه). على الرغم من عدم وجود فروق ذات دلالة إحصائية بين Actos وهمي لحدوث 3 سنوات من حدث أول داخل هذا المركب ، لم يكن هناك زيادة في معدل الوفيات أو في مجموع الأحداث الأوعية الدموية الكبرى مع أكتوس.
الجدول 8 عدد الأحداث الأولى والإجمالية لكل مكون داخل نقطة نهاية مركب القلب والأوعية الدموية
| الوهمي N = 2633 |
أكتوس N = 2605 |
|||
| أحداث القلب والأوعية الدموية | الأحداث الأولى (ن) |
مجموع الأحداث (ن) |
الأحداث الأولى (ن) |
مجموع الأحداث (ن) |
| أي حدث | 572 | 900 | 514 | 803 |
| جميع أسباب الوفاة | 122 | 186 | 110 | 177 |
| غير قاتلة MI | 118 | 157 | 105 | 131 |
| السكتة الدماغية | 96 | 119 | 76 | 92 |
| ACS | 63 | 78 | 42 | 65 |
| تدخل القلب | 101 | 240 | 101 | 195 |
| بتر الساق الكبرى | 15 | 28 | 9 | 28 |
| إعادة تنشيط الساق | 57 | 92 | 71 | 115 |
كما تم تلقي تقارير ما بعد التسويق عن ظهور الوذمة البقعة الصفراء السكري الجديدة أو تفاقم حدة حدة البصر (انظر احتياطات، العام ، البقعة الصفراء وذمة).
تشوهات المختبر
أمراض الدم: الأكتوس قد يسبب انخفاضا في الهيموغلوبين والهيماتوكريت. يبدو أن سقوط الهيموغلوبين والهيماتوكريت مع أكتو له علاقة بالجرعة. في جميع الدراسات السريرية ، يعني انخفاض قيم الهيموغلوبين بنسبة 2 ٪ إلى 4 ٪ في المرضى الذين عولجوا مع Actos. حدثت هذه التغييرات بشكل عام خلال أول 4 إلى 12 أسبوعًا من العلاج وظلت مستقرة نسبيًا بعد ذلك. قد تكون مرتبطة هذه التغييرات إلى زيادة حجم البلازما المرتبطة العلاج Actos ونادرا ما ترتبط مع أي آثار سريرية الدم.
مستويات ترانساميناز المصل: خلال جميع الدراسات السريرية في الولايات المتحدة ، 14 من 4780 (0.30 ٪) من المرضى الذين عولجوا مع Actos لديهم قيم ALT - 3 أضعاف الحد الأعلى الطبيعي خلال العلاج. كان جميع المرضى الذين يعانون من قيم المتابعة ارتفاعات عكسية في ALT. في السكان من المرضى الذين عولجوا مع Actos ، تم تخفيض القيم المتوسطة للبيليروبين ، AST ، ALT ، الفوسفاتيز القلوي ، و GGT في الزيارة الأخيرة مقارنة مع خط الأساس. تم سحب أقل من 0.9 ٪ من المرضى الذين عولجوا بـ Actos من التجارب السريرية في الولايات المتحدة بسبب اختبارات وظائف الكبد غير الطبيعية.
في التجارب السريرية المسبقة الموافقة ، لم تكن هناك حالات من ردود الفعل المخدرات الخصية مما يؤدي إلى الفشل الكبدي (انظر احتياطات، عام ، آثار الكبد).
مستويات CPK: خلال الاختبارات المعملية المطلوبة في التجارب السريرية ، لوحظت ارتفاعات متقطعة وعابرة في مستويات فسفوكيناز الكرياتين (CPK). لوحظ ارتفاع معزول إلى أكثر من 10 أضعاف الحد العلوي الطبيعي في 9 مرضى (قيم 2150 حتي 11400 وحدة دولية / لتر). واصل ستة من هؤلاء المرضى لتلقي Actos ، واثنين من المرضى قد أكملت تلقي الدراسة الدواء في وقت القيمة المرتفعة وموقف مريض واحد دراسة الدواء بسبب ارتفاع. هذه الارتفاعات حلها دون أي عقابيل سريرية واضحة. العلاقة بين هذه الأحداث والعلاج Actos غير معروف.
أعلى
جرعة مفرطة
خلال التجارب السريرية التي تسيطر عليها ، تم الإبلاغ عن حالة واحدة من جرعة زائدة من Actos. تناول المريض الذكور 120 ملغ يوميا لمدة أربعة أيام ، ثم 180 ملغ يوميا لمدة سبعة أيام. نفى المريض أي أعراض سريرية خلال هذه الفترة.
في حالة الجرعة الزائدة ، يجب بدء العلاج الداعم المناسب وفقًا للعلامات والأعراض السريرية للمريض.
أعلى
الجرعة والإدارة
ينبغي أن تؤخذ Actos مرة واحدة يوميا دون النظر إلى وجبات الطعام.
يجب أن تكون إدارة العلاج المضاد لمرض السكر فردية. من الناحية المثالية ، ينبغي تقييم الاستجابة للعلاج باستخدام HbA1C وهو مؤشر أفضل للسيطرة على نسبة السكر في الدم على المدى الطويل من FPG وحدها. HBA1C يعكس نسبة السكر في الدم على مدى الشهرين أو الثلاثة أشهر الماضية. في الاستخدام السريري ، يوصى بمعالجة المرضى بالـ Actos لفترة زمنية كافية لتقييم التغير في HbA1C (ثلاثة أشهر) ما لم تتدهور السيطرة على نسبة السكر في الدم. بعد بدء Actos أو مع زيادة الجرعة ، يجب مراقبة المرضى بعناية للأحداث السلبية المتعلقة بالاحتفاظ بالسوائل (انظر تحذير محاصر و تحذيرات).
وحيد
قد يبدأ العلاج الأحادي اكتوس في المرضى الذين لا تسيطر عليهم بشكل كاف مع اتباع نظام غذائي وممارسة الرياضة في 15 ملغ أو 30 ملغ مرة واحدة يوميا. بالنسبة للمرضى الذين يستجيبون بشكل غير كاف للجرعة الأولية من Actos ، يمكن زيادة الجرعة بزيادات تصل إلى 45 ملغ مرة واحدة يوميًا. بالنسبة للمرضى الذين لا يستجيبون بشكل كافٍ للعلاج الأحادي ، يجب مراعاة العلاج المركب.
الجمع بين العلاج
السلفونيل يوريا: يمكن البدء بالاكتوس مع السلفونيل يوريا عند 15 ملغ أو 30 ملغ مرة واحدة يوميًا. يمكن استمرار جرعة السلفونيل يوريا الحالية عند بدء العلاج أكتوس. إذا أبلغ المرضى عن نقص السكر في الدم ، فيجب تقليل جرعة السلفونيل يوريا.
الميتفورمين: يمكن البدء بالإكتوس مع الميتفورمين عند 15 ملغ أو 30 ملغ مرة واحدة يوميًا. يمكن أن تستمر جرعة الميتفورمين الحالية عند بدء علاج Actos. من غير المرجح أن تتطلب جرعة الميتفورمين تعديل بسبب نقص السكر في الدم أثناء الجمع بين العلاج مع Actos.
الأنسولين: يمكن البدء بالاكتوز مع الأنسولين عند 15 ملغ أو 30 ملغ مرة واحدة يوميًا. يمكن أن تستمر جرعة الأنسولين الحالية عند بدء العلاج Actos. في المرضى الذين يتلقون Actos والأنسولين ، يمكن تقليل جرعة الأنسولين بنسبة 10 ٪ إلى 25 ٪ إذا أبلغ المريض عن نقص السكر في الدم أو إذا انخفضت تركيزات الجلوكوز في البلازما إلى أقل من 100 ملغ / ديسيلتر. يجب إجراء تعديلات إضافية على أساس استجابة خفض الجلوكوز.
الجرعة الموصى بها القصوى
يجب ألا تتجاوز جرعة أكتوس 45 ملغ مرة واحدة يوميًا في علاج أحادي أو مع سلفونيل يوريا أو ميتفورمين أو أنسولين.
لا ينصح تعديل الجرعة في المرضى الذين يعانون من قصور كلوي (انظر صيدلية سريرية، الدوائية والأيض المخدرات).
لا ينبغي أن يبدأ العلاج بـ Actos إذا أظهر المريض أدلة سريرية على مرض الكبد النشط أو زيادة مستويات الترانساميناز في المصل (البديل أكبر من 2.5 أضعاف الحد الأعلى الطبيعي) في بداية العلاج (نرى احتياطات، عام ، آثار الكبد و صيدلية سريرية، السكان الخاصة ، قصور الكبد). يوصى بمراقبة إنزيم الكبد في جميع المرضى قبل بدء العلاج باستخدام الأكتوس وبعد ذلك بشكل دوري (انظر احتياطات، عام ، آثار الكبد).
لا توجد بيانات عن استخدام Actos في المرضى الذين تقل أعمارهم عن 18 عامًا ؛ لذلك ، لا ينصح باستخدام Actos في مرضى الأطفال.
لا توجد بيانات متاحة عن استخدام Actos بالاشتراك مع thiazolidinedione آخر.
أعلى
كيف زودت
يتوفر Actos في 15 ملغ و 30 ملغ و 45 ملغ على النحو التالي:
15 mg Tablet: أبيض إلى أبيض باهت ، دائري ، محدب ، غير مسجل مع "Actos" على جانب واحد ، و "15" على الجانب الآخر ، متوفر في:
NDC 64764-151-04 زجاجات من 30
NDC 64764-151-05 زجاجات من 90
NDC 64764-151-06 زجاجات من 500
قرص بحجم 30 ملغ: قرص أبيض إلى أبيض ، مستدير ، مُسطح ، بدون سجل مع "Actos" على جانب ، و "30" من جهة أخرى ، متاح في:
NDC 64764-301-14 زجاجات من 30
NDC 64764-301-15 زجاجات من 90
NDC 64764-301-16 زجاجات من 500
45 ملغ: قرص من الأبيض إلى الأبيض ، دائري ، مسطح ، غير مسجل مع "Actos" على جانب واحد ، و "45" على الجانب الآخر ، متوفر في:
NDC 64764-451-24 زجاجات من 30
NDC 64764-451-25 زجاجات من 90
NDC 64764-451-26 زجاجات من 500
تخزين
متجر في 25 درجة مئوية (77 درجة فهرنهايت) ؛ الرحلات المسموح بها إلى 15-30 درجة مئوية (59-86 درجة فهرنهايت) [انظر درجة حرارة الغرفة التي تسيطر عليها جامعة جنوب المحيط الهادئ]. الحفاظ على حاوية مغلقة بإحكام ، وحماية من الرطوبة والرطوبة.
أعلى
المراجع
- دينغ ، إل جيه ، وآخرون. تأثير gemfibrozil على الدوائية للبيوجليتازون. Eur J Clin Pharmacol 2005؛ 61: 831-836 ، الجدول 1.
2. Jaakkola ، T ، وآخرون. تأثير ريفامبيسين على الدوائية للبيوجليتازون. Clin Pharmacol Brit Jour 2006؛ 61:1 70-78.
آر إكس فقط
صنع بواسطة:
شركة تاكيدا للصناعات الدوائية المحدودة
أوساكا، اليابان
تسويق بواسطة:
شركة تاكيدا لصناعة الأدوية الأمريكية
واحد تاكيدا باركواي
ديرفيلد ، IL 60015
أكتوس® هي علامة تجارية مسجلة لشركة Takeda Pharmaceutical Company Limited وتستخدم بموجب ترخيص من شركة Takeda Pharmaceuticals America، Inc.
جميع أسماء العلامات التجارية الأخرى هي ملك لأصحابها.
آخر تحديث: 08/09
Actos ، بيوجليتازون hcl ، معلومات المريض (في سهل الانجليزية)
معلومات مفصلة عن العلامات والأعراض والأسباب والعلاج من مرض السكري
لا تهدف المعلومات الواردة في هذه الدراسة إلى تغطية جميع الاستخدامات أو الاتجاهات أو الاحتياطات الممكنة أو التفاعلات الدوائية أو الآثار الضارة. هذه المعلومات معممة وليس المقصود بها تقديم المشورة الطبية المحددة. إذا كانت لديك أسئلة حول الأدوية التي تتناولها أو ترغب في مزيد من المعلومات ، فاستشر طبيبك أو الصيدلي أو الممرض.
ارجع الى: تصفح جميع الأدوية لمرض السكري

