Apidra لعلاج مرض السكري
اسم العلامة التجارية: Apidra
الاسم العام: الأنسولين Glulisine
Apidra (الأنسولين glulisine) هو منتج من صنع الإنسان مطابق تقريبا للأنسولين البشري. يستخدم لعلاج داء السكري. الاستخدام ، الجرعة ، الآثار الجانبية.
محتويات:
مؤشرات والاستخدام
الجرعة والإدارة
موانع
المحاذير والإحتياطات
ردود الفعل السلبية
تفاعل الأدوية
استخدام في السكان محددة
جرعة زائدة
وصف
علم الصيدلة السريرية
علم السموم غير الإكلينيكي
الدراسات السريرية
كيف زودت
Apidra ، الأنسولين glusine ، معلومات المريض (في سهل الانجليزية)
دواعي الإستعمال
Apidra هو تمثيلي سريع للأنسولين البشري تم الإشارة إليه لتحسين التحكم في نسبة السكر في الدم لدى البالغين والأطفال المصابين بداء السكري.
أعلى
الجرعة والإدارة
اعتبارات الجرعة
APIDRA هو نظير للأنسولين المؤتلف يكافئ الأنسولين البشري (بمعنى أن وحدة واحدة من APIDRA لها نفس تأثير خفض الجلوكوز مثل وحدة واحدة من الأنسولين البشري العادي) عند إعطاءها عن طريق الوريد. عندما يعطى تحت الجلد ، يكون لدى APIDRA بداية أكثر سرعة ومدة عمل أقصر من الأنسولين البشري العادي.
يجب أن تكون جرعة APIDRA فردية. مراقبة نسبة الجلوكوز في الدم أمر ضروري في جميع المرضى الذين يتلقون العلاج بالأنسولين.
قد يختلف إجمالي متطلبات الأنسولين اليومية وعادة ما يتراوح بين 0.5 إلى 1 وحدة / كجم / يوم. قد يتم تغيير متطلبات الأنسولين أثناء الإجهاد أو المرض الشديد أو مع تغييرات في التمرينات أو أنماط الوجبات أو العقاقير المختلطة.
الإدارة تحت الجلد
يجب أن تعطى APIDRA في غضون 15 دقيقة قبل وجبة أو في غضون 20 دقيقة بعد بدء الوجبة.
يجب أن تستخدم APIDRA عن طريق الحقن تحت الجلد بشكل عام في الأنظمة ذات الأنسولين الوسيط أو طويل المفعول.
يجب أن تدار APIDRA عن طريق الحقن تحت الجلد في جدار البطن أو الفخذ أو الذراع العلوي. يجب تدوير مواقع الحقن داخل نفس المنطقة (البطن ، الفخذ أو الذراع العلوي) من حقنة إلى أخرى لتقليل خطر الحثل الشحمي [انظر ردود الفعل الضارة].
التسريب تحت الجلد المستمر (مضخة الأنسولين)
يمكن إعطاء APIDRA بالتسريب تحت الجلد المستمر في جدار البطن. لا تستخدم الأنسولين المخفف أو المختلط في مضخات الأنسولين الخارجية. يجب تدوير مواقع التسريب داخل نفس المنطقة لتقليل خطر الحثل الشحمي [انظر ردود الفعل الضارة]. يجب أن تستند البرمجة الأولية لمضخة ضخ الأنسولين الخارجية إلى إجمالي جرعة الأنسولين اليومية في النظام السابق.
تم استخدام مضخات الأنسولين التالية في تجارب APIDRA السريرية التي أجرتها شركة Sanofi-aventis ، الشركة المصنعة لـ APIDRA:
- Disetronic® H-Tron® plus V100 و D-Tron® مع القسطرة Disetronic (Rapid ™ و Rapid C ™ و Rapid D ™ و Tender ™)
- الطرازات MiniMed® 506 و 507 و 507 c و 508 مع القسطرة MiniMed (Sof-set Ultimate QR ™ و Quick-set ™).
قبل استخدام مضخة الأنسولين المختلفة مع APIDRA ، اقرأ ملصق المضخة للتأكد من تقييم المضخة باستخدام APIDRA.
يجب على الأطباء والمرضى إجراء تقييم دقيق للمعلومات حول استخدام المضخة في معلومات وصف APIDRA ، ونشرة معلومات المريض ، ودليل الشركة المصنعة للمضخة. يجب اتباع المعلومات الخاصة بـ APIDRA للوقت قيد الاستخدام ، وتواتر مجموعات التسريب المتغيرة ، أو غيرها تفاصيل خاصة باستخدام APIDRA ، لأن المعلومات الخاصة بـ APIDRA قد تختلف عن دليل المضخة العام تعليمات.
استنادا إلى الدراسات المختبرية التي أظهرت فقدان التحلل ، metacresol وتدهور الأنسولين ، يجب تغيير APIDRA في الخزان كل 48 ساعة على الأقل. لا ينبغي أن يتعرض APIDRA في الاستخدام السريري لدرجات حرارة أكبر من 98.6 درجة فهرنهايت (37 درجة مئوية). [نرى المحاذير والإحتياطات و كيف زودت / التخزين والمناولة].
الوريد
يمكن إعطاء APIDRA عن طريق الوريد تحت إشراف طبي للسيطرة على نسبة السكر في الدم من خلال المراقبة الدقيقة لنسبة السكر في الدم والبوتاسيوم في الدم لتجنب نقص السكر في الدم ونقص بوتاسيوم الدم. للاستخدام في الوريد ، يجب استخدام APIDRA بتركيزات من 0.05 وحدة / مل إلى 1 وحدة / مل من الأنسولين glulisine في أنظمة التسريب باستخدام أكياس كلوريد البوليفينيل (PVC). ثبت أن APIDRA مستقر فقط في محلول ملحي طبيعي (0.9٪ كلوريد الصوديوم). يجب فحص المنتجات الدوائية عن طريق الحقن بصريًا بحثًا عن الجسيمات وتغير اللون قبل تناولها ، كلما سمح المحلول والحاوية بذلك. لا تدير مخاليط الأنسولين عن طريق الوريد.
أشكال الجرعات ونقاط القوة
تتوفر وحدات Apidra 100 لكل مل (U-100) على النحو التالي:
- 10 مل قارورة
- 3 مل من خراطيش للاستخدام في OptiClik® جهاز توصيل الأنسولين
- 3 مل SoloStar القلم مملوءة مسبقا
أعلى
موانع
هو بطلان Apidra:
- خلال نوبات نقص السكر في الدم
- في المرضى الذين يعانون من حساسية شديدة لأبيدرا أو لأي من سواغها
عند استخدامه في المرضى الذين يعانون من فرط الحساسية المعروف لأبيدرا أو سواغها ، يمكن للمرضى تطوير تفاعلات فرط الحساسية الموضعية أو المعممة [انظر ردود الفعل السلبية].
أعلى
المحاذير والإحتياطات
تعديل الجرعة والمراقبة
مراقبة الجلوكوز ضرورية للمرضى الذين يتلقون العلاج بالأنسولين. يجب إجراء التغييرات في نظام الأنسولين بحذر وفقط تحت إشراف طبي. قد تؤدي التغييرات في قوة الأنسولين أو الشركة المصنعة أو النوع أو طريقة الإعطاء إلى الحاجة إلى تغيير جرعة الأنسولين. قد تكون هناك حاجة لتعديل العلاج المصاحب لمرض السكر عن طريق الفم.
كما هو الحال مع جميع الاستعدادات للأنسولين ، قد يختلف مسار العمل لأبيدرا في أفراد مختلفين أو في أوقات مختلفة الشخص نفسه ويعتمد على العديد من الحالات ، بما في ذلك موقع الحقن أو مصدر الدم المحلي أو المحلي درجة الحرارة. قد يحتاج المرضى الذين يغيرون مستوى نشاطهم البدني أو خطة الوجبات إلى تعديل جرعات الأنسولين.
نقص سكر الدم
نقص السكر في الدم هو رد الفعل السلبي الأكثر شيوعا من العلاج بالأنسولين ، بما في ذلك Apidra. خطر نقص السكر في الدم يزيد مع تشديد مراقبة نسبة السكر في الدم. يجب تثقيف المرضى للتعرف على نقص السكر في الدم وإدارته. نقص السكر في الدم الحاد قد يؤدي إلى فقدان الوعي و / أو التشنجات وقد يؤدي إلى اختلال مؤقت أو دائم في وظائف المخ أو موته. نقص السكر في الدم الشديد التي تتطلب مساعدة من شخص آخر و / أو ضخ الجلوكوز بالحقن أو وقد لوحظت إدارة الجلوكاجون في التجارب السريرية مع الأنسولين ، بما في ذلك التجارب مع أبيدرا.
توقيت نقص السكر في الدم عادة ما يعكس الشخصية وقت العمل من تركيبات الأنسولين تدار. عوامل أخرى مثل التغيرات في تناول الطعام (على سبيل المثال ، كمية الطعام أو توقيت الوجبات) ، وموقع الحقن ، وممارسة الرياضة ، والأدوية المصاحبة لها قد تؤدي أيضًا إلى تغيير خطر نقص السكر في الدم [انظر تفاعل الأدوية].
كما هو الحال مع جميع الأنسولين ، توخي الحذر في المرضى الذين يعانون من نقص السكر في الدم وعي المرضى الذين قد يكونون يؤهب لنقص السكر في الدم (على سبيل المثال ، عدد الأطفال والمرضى الذين يصومون أو يعانون من عدم انتظام الطعام تناول). قد تتأثر قدرة المريض على التركيز والتفاعل نتيجة لنقص السكر في الدم. قد يمثل هذا خطراً في الحالات التي تكون فيها هذه القدرات ذات أهمية خاصة ، مثل القيادة أو تشغيل الآلات الأخرى.
قد تؤدي التغيرات السريعة في مستويات الجلوكوز في الدم إلى ظهور أعراض مشابهة لنقص السكر في الدم لدى الأشخاص المصابين بداء السكري ، بغض النظر عن قيمة الجلوكوز. قد تكون أعراض الإنذار المبكر لنقص السكر في الدم مختلفة أو أقل وضوحا في ظل ظروف معينة ، مثل مرض السكري منذ فترة طويلة ، ومرض الأعصاب السكري ، واستخدام الأدوية مثل حاصرات بيتا [انظر تفاعل الأدوية] ، أو تكثيف السيطرة على مرض السكري. قد تؤدي هذه الحالات إلى نقص السكر في الدم الشديد (وربما فقدان الوعي) قبل إدراك المريض لنقص السكر في الدم.
يحتوي الأنسولين الذي يتم إدارته عن طريق الوريد على نشاط أسرع من الأنسولين الذي يتم إدارته تحت الجلد ، مما يتطلب مراقبة دقيقة لنقص السكر في الدم.
فرط الحساسية والحساسية
قد تحدث الحساسية الشديدة والمهددة للحياة ، بما في ذلك الحساسية المفرطة ، مع منتجات الأنسولين ، بما في ذلك Apidra [انظر ردود الفعل السلبية].
نقص بوتاسيوم الدم
تتسبب جميع منتجات الأنسولين ، بما في ذلك Apidra ، في تحول البوتاسيوم من الفضاء خارج الخلية إلى الفضاء داخل الخلايا ، مما قد يؤدي إلى نقص بوتاسيوم الدم. نقص بوتاسيوم الدم غير المعالج قد يسبب شلل في الجهاز التنفسي ، عدم انتظام ضربات القلب البطيني ، والموت. توخي الحذر في المرضى الذين قد يكونون عرضة لخطر نقص بوتاسيوم الدم (على سبيل المثال ، المرضى الذين يستخدمون أدوية خفض البوتاسيوم ، والمرضى الذين يتناولون أدوية حساسة لتركيزات البوتاسيوم في الدم). مراقبة الجلوكوز والبوتاسيوم بشكل متكرر عندما تدار Apidra عن طريق الوريد.
القصور الكلوي أو الكبدي
قد تكون هناك حاجة لرصد الجلوكوز بشكل متكرر وتخفيض جرعة الأنسولين في المرضى الذين يعانون من قصور كلوي أو كبدي [انظر علم الصيدلة السريرية].
خلط الأنسولين
لا ينبغي خلط Apidra للحقن تحت الجلد مع مستحضرات الأنسولين غير الأنسولين NPH. إذا تم خلط Apidra مع الأنسولين NPH ، فيجب وضع Apidra في المحقنة أولاً. يجب أن يحدث الحقن مباشرة بعد الخلط.
لا تخلط Apidra مع غيرها من الأنسولين للإعطاء عن طريق الوريد أو للاستخدام في مضخة التسريب تحت الجلد المستمرة.
لا ينبغي تخفيف أبيدرا عن طريق الحقن في الوريد بمحلول آخر غير 0.9٪ كلوريد الصوديوم (محلول ملحي طبيعي). لم تثبت فعالية وسلامة خلط Apidra مع المواد المخففة أو غيرها من الأنسولين للاستخدام في مضخات التسريب تحت الجلد الخارجية.
مضخات ضخ الأنسولين تحت الجلد
عند استخدامه في مضخة الأنسولين الخارجية للتسريب تحت الجلد ، لا ينبغي تخفيف Apidra أو خلطه بأي الأنسولين الآخر. يجب تغيير Apidra في الخزان كل 48 ساعة على الأقل. لا ينبغي أن يتعرض أبيدرا لدرجات حرارة أكبر من 98.6 درجة فهرنهايت (37 درجة مئوية).
خلل في مضخة الأنسولين أو مجموعة ضخ أو تدهور الأنسولين يمكن أن يؤدي بسرعة إلى ارتفاع السكر في الدم والكيتوزيه. من الضروري تحديد وتصحيح سبب ارتفاع السكر في الدم أو الكيتوزية. قد تكون هناك حاجة للحقن تحت الجلد المؤقتة مع Apidra. يجب تدريب المرضى الذين يستخدمون العلاج المستمر بمضخة تسريب الأنسولين تحت الجلد على إعطاء الأنسولين عن طريق الحقن والحصول على علاج الأنسولين البديل في حالة تعطل المضخة. [نرى الجرعة والإدارة, كيف زودت / التخزين والمناولة].
الوريد
عندما يتم إعطاء Apidra عن طريق الوريد ، يجب مراقبة مستويات الجلوكوز والبوتاسيوم عن كثب لتجنب نقص السكر في الدم الذي يحتمل أن يكون قاتلاً.
لا تخلط Apidra مع غيرها من الأنسولين للإعطاء عن طريق الوريد. يمكن تخفيف أبيدرا فقط في محلول ملحي طبيعي.
تفاعل الأدوية
بعض الأدوية قد تغير من متطلبات الأنسولين وخطر نقص السكر في الدم أو ارتفاع السكر في الدم [انظر تفاعل الأدوية].
أعلى
ردود الفعل السلبية
وتناقش ردود الفعل السلبية التالية في مكان آخر:
- نقص السكر في الدم [انظر المحاذير والإحتياطات]
- نقص بوتاسيوم الدم [انظر المحاذير والإحتياطات]
تجربة التجارب السريرية
نظرًا لأن التجارب السريرية تجرى تحت تصميمات متباينة على نطاق واسع ، فإن معدلات التفاعلات السلبية التي أبلغ عنها في تجربة سريرية واحدة قد لا تفعل ذلك يمكن مقارنتها بسهولة مع تلك المعدلات المبلغ عنها في تجربة سريرية أخرى ، وقد لا تعكس المعدلات التي لوحظت فعليًا في التجارب السريرية ممارسة.
وترد في الجدول أدناه تواتر ردود الفعل الدوائية الضارة خلال التجارب السريرية Apidra في المرضى الذين يعانون من داء السكري من النوع 1 ومرض السكري من النوع 2.
الجدول 1: الأحداث السلبية الناشئة عن العلاج في الدراسات المجمعة للبالغين المصابين بداء السكري من النوع 1 (الأحداث الضائرة ذات التردد â٪٪ 5٪)
| APIDRA ، ٪ (ن = 950) |
جميع المقارنةأ, % (ن = 641) |
|
| البلعوم الأنفي | 10.6 | 12.9 |
| نقص سكر الدمب | 6.8 | 6.7 |
| عدوى الجهاز التنفسي العلوي | 6.6 | 5.6 |
| إنفلونزا | 4.0 | 5.0 |
|
أ الأنسولين lispro ، الأنسولين البشري العادي ، الأنسولين aspart ب فقط نقص السكر في الدم أعراض شديدة |
الجدول 2: الأحداث السلبية الناشئة عن العلاج في الدراسات المجمعة للبالغين المصابين بداء السكري من النوع 2 (الأحداث الضائرة ذات التردد â ‰٪ 5٪)
| APIDRA ، ٪ (ن = 883) |
الأنسولين البشري العادي ، ٪ (ن = 883) |
|
| عدوى الجهاز التنفسي العلوي | 10.5 | 7.7 |
| البلعوم الأنفي | 7.6 | 8.2 |
| وذمة محيطية | 7.5 | 7.8 |
| إنفلونزا | 6.2 | 4.2 |
| ألم مفصلي | 5.9 | 6.3 |
| ارتفاع ضغط الدم | 3.9 | 5. |
- طب الأطفال
يلخص الجدول 3 ردود الفعل السلبية التي تحدث مع تردد أعلى من 5 ٪ في دراسة سريرية في الأطفال والمراهقين الذين يعانون من مرض السكري من النوع 1 تعامل مع APIDRA (ن = 277) أو الأنسولين ليسبرو (ن = 295).
الجدول 3: الأحداث السلبية الناشئة عن العلاج في الأطفال والمراهقين المصابين بداء السكري من النوع 1 (ردود الفعل السلبية بتردد 5٪)
| APIDRA ، ٪ (ن = 277) |
ليسبرو ، ٪ (ن = 295) |
|
| البلعوم الأنفي | 9.0 | 9.5 |
| عدوى الجهاز التنفسي العلوي | 8.3 | 10.8 |
| صداع الراس | 6.9 | 11.2 |
| نوبة سكر الدم | 6.1 | 4.7 |
- نقص السكر في الدم أعراض شديدة
نقص السكر في الدم هو رد الفعل السلبي الأكثر شيوعًا في المرضى الذين يستخدمون الأنسولين ، بما في ذلك Apidra [See المحاذير والإحتياطات]. كانت معدلات وحدوث نقص السكر في الدم الحاد في الأعراض ، والمعروفة باسم نقص السكر في الدم التي تتطلب تدخلًا من طرف ثالث ، مماثلة لجميع نظم العلاج (انظر الجدول 4). في المرحلة 3 من التجارب السريرية ، كان معدل الإصابة بين الأطفال والمراهقين المصابين بداء السكري من النوع 1 من نقص السكر في الدم أعراض شديدة في مجموعات العلاج اثنين مقارنة مع البالغين مع نوع 1 داء السكري. (انظر الجدول 4) [انظر الدراسات السريرية].
الجدول 4: نقص السكر في الدم الحاد في الأعراض *
| مرض السكر النوع 1 الكبار 12 أسبوع مع الأنسولين glargine |
مرض السكري من النوع 1 للبالغين 26 أسبوع مع الأنسولين glargine |
داء السكري من النوع 2 الكبار 26 أسبوع مع الأنسولين البشري NPH |
داء السكري من النوع الأول 26 أسبوع |
||||||
|---|---|---|---|---|---|---|---|---|---|
| أبيدرا قبل وجبة |
أبيدرا بعد وجبة |
الأنسولين البشري العادي | أبيدرا | الأنسولين ليسبرو | أبيدرا | الأنسولين البشري العادي | أبيدرا | الأنسولين | |
| * نقص السكر في الدم أعراض شديد يعرف بأنه حدث سكر الدم تتطلب مساعدة من شخص آخر استوفى أحد المعايير التالية: ارتبط الحدث بكامل الدم المشار إليه في الدم إلى نسبة الجلوكوز في الدم أقل من 36 ملجم / ديسيلتر أو كان مرتبطًا بالشفاء العاجل بعد الكربوهيدرات عن طريق الفم أو الجلوكوز في الوريد أو إعطاء الجلوكاجون. | |||||||||
| أحداث شهريا لكل مريض | 0.05 | 0.05 | 0.13 | 0.02 | 0.02 | 0.00 | 0.00 | 0.09 | 0.08 |
| النسبة المئوية للمرضى (ن / المجموع الكلي) | 8.4% (24/286) | 8.4% (25/296) | 10.1% (28/278) | 4.8% (16/339) |
4.0% (13/333) |
1.4% (6/416) |
1.2% (5/420) |
16.2% (45/277) |
19.3% (57/295) |
- بدء الأنسولين وتكثيف السيطرة على الجلوكوز
ارتبط التكثيف أو التحسن السريع في السيطرة على الجلوكوز بالانتقال العكسي اضطراب الانكسار البصري ، تفاقم اعتلال الشبكية السكري ، والألم المحيطي الحاد المؤلم الاعتلال العصبي. ومع ذلك ، يقلل التحكم في نسبة السكر في الدم على المدى الطويل من خطر اعتلال الشبكية السكري واعتلال الأعصاب.
- الحثل الشحمي
الاستخدام طويل الأجل للأنسولين ، بما في ذلك Apidra ، يمكن أن يسبب الحثل الشحمي في موقع الحقن أو التسريب المتكرر للأنسولين. يشمل الحثل الشحمي ضمور شحمي (سماكة الأنسجة الدهنية) وضمور الدهون (ترقق الأنسجة الدهنية) ، وقد يؤثر على امتصاص الأنسولين. قم بتدوير مواقع حقن أو حقن الأنسولين داخل نفس المنطقة لتقليل خطر الحثل الشحمي. [نرى الجرعة والإدارة].
- زيادة الوزن
يمكن أن يحدث زيادة في الوزن مع العلاج بالأنسولين ، بما في ذلك Apidra ، ويعزى ذلك إلى التأثيرات الابتنائية للأنسولين وانخفاض السكر في البول.
- وذمة محيطية
قد يتسبب الأنسولين ، بما في ذلك Apidra ، في احتباس الصوديوم والوذمة ، خاصة إذا تم تحسين التحكم في التمثيل الغذائي في السابق عن طريق العلاج المكثف بالأنسولين.
- ردود الفعل السلبية مع التسريب المستمر للأنسولين تحت الجلد (CSII)
في دراسة عشوائية لمدة 12 أسبوعا في المرضى الذين يعانون من مرض السكري من النوع 1 (ن = 59) ، ومعدلات القسطرة كانت انسداد وردود الفعل موقع التسريب مماثلة لأبيدرا والأنسولين aspart المرضى الذين عولجوا (الجدول 5).
الجدول 5: انسداد القسطرة وردود الفعل موقع التسريب.
| أبيدرا (ن = 29) |
الأنسولين الأسبارت (ن = 30) |
|
|---|---|---|
| انسداد القسطرة / الشهر | 0.08 | 0.15 |
| ردود الفعل موقع التسريب | 10.3% (3/29) | 13.3% (4/30) |
- الحساسية
الحساسية المحلية
كما هو الحال مع أي علاج للأنسولين ، قد يتعرض المرضى الذين يتناولون Apidra للاحمرار أو التورم أو الحكة في موقع الحقن. عادة ما يتم حل ردود الفعل البسيطة هذه في غضون بضعة أيام إلى بضعة أسابيع ، ولكن في بعض الحالات قد تتطلب وقف Apidra. في بعض الحالات ، قد تكون هذه التفاعلات مرتبطة بعوامل أخرى غير الأنسولين ، مثل المهيجات في عامل تطهير الجلد أو تقنية الحقن الضعيف.
الحساسية الجهازية
قد تحدث الحساسية الشديدة والمهددة للحياة ، بما في ذلك الحساسية المفرطة ، مع أي الأنسولين ، بما في ذلك Apidra. قد تتسبب الحساسية المعممة للأنسولين في حدوث طفح كامل في الجسم (بما في ذلك الحكة) أو ضيق التنفس أو الصفير أو انخفاض ضغط الدم أو عدم انتظام دقات القلب أو الحجاب الحاجز.
في التجارب السريرية التي تسيطر عليها لمدة تصل إلى 12 شهرا ، تم الإبلاغ عن ردود فعل تحسسية الجهازية المحتملة في 79 من 1833 مريضا (4.3 ٪) الذين تلقوا Apidra و 58 من 1524 مريضا (3.8 ٪) الذين تلقوا المقارنة قصيرة المفعول الأنسولين. خلال هذه التجارب ، توقف العلاج مع Apidra بشكل دائم في 1 من 1833 مريض بسبب رد الفعل التحسسي الجهازية المحتملة.
تم الإبلاغ عن ردود الفعل الموضعية وألم عضلي معمم باستخدام metacresol ، وهو أحد سواغات Apidra.
إنتاج الأجسام المضادة
في دراسة أجريت على مرضى السكري من النوع 1 (ن = 333) ، تركيزات الأجسام المضادة للأنسولين التي تتفاعل مع كل من الأنسولين البشري والأنسولين بقي جلوليزين (الأجسام المضادة للأنسولين المتفاعلة) بالقرب من خط الأساس خلال الستة أشهر الأولى من الدراسة في المرضى الذين عولجوا أبيدرا. وقد لوحظ انخفاض في تركيز الأجسام المضادة خلال 6 أشهر التالية من الدراسة. في دراسة أجريت على مرضى السكري من النوع 2 (ن = 411) ، كانت هناك زيادة مماثلة في تركيز الجسم المضاد للأنسولين التفاعلي لوحظ في المرضى الذين عولجوا بأبيدرا وفي المرضى الذين عولجوا بالأنسولين البشري خلال الأشهر التسعة الأولى من دراسة. بعد ذلك انخفض تركيز الأجسام المضادة في مرضى Apidra وظل مستقراً عند مرضى الأنسولين البشري. لم يكن هناك ارتباط بين تركيز الجسم المضاد للأنسولين التفاعلي والتغيرات في HbA1c ، جرعات الأنسولين ، أو حدوث نقص السكر في الدم. الأهمية السريرية لهذه الأجسام المضادة غير معروفة.
لم تثير Apidra استجابة كبيرة من الأجسام المضادة في دراسة للأطفال والمراهقين المصابين بداء السكري من النوع 1.
تجربة ما بعد البيع
تم تحديد ردود الفعل السلبية التالية أثناء استخدام Apidra بعد الموافقة عليها.
نظرًا لأن ردود الفعل هذه يتم الإبلاغ عنها طوعًا من مجموعة سكانية ذات حجم غير مؤكد ، فهي ليست كذلك من الممكن دائمًا تقدير تواترها بشكل موثوق أو إنشاء علاقة سببية بالمخدرات مكشوف.
تم الإبلاغ عن الأخطاء الدوائية التي تدار فيها الأنسولين ، وخاصة الأنسولين طويل المفعول ، عن طريق الخطأ بدلاً من Apidra.
أعلى
تفاعل الأدوية
هناك عدد من الأدوية التي تؤثر على استقلاب الجلوكوز وقد تستلزم تعديل جرعة الأنسولين ومراقبة دقيقة بشكل خاص.
الأدوية التي قد تزيد من تأثير خفض نسبة الجلوكوز في الدم للأنسولين بما في ذلك Apidra ، وبالتالي تزيد من خطر نقص السكر في الدم ، وتشمل المنتجات المضادة لمرض السكر عن طريق الفم ، براملينتيد ، مثبطات الإنزيم المحول للأنجيوتنسين ، ديسبيراميد ، فايبريت ، فلوكستين ، مثبطات أوكسيديز أحادي الأمين ، بروبوكسيفين ، بنتوكسيفيلين ، الساليسيلات ، نظير السوماتوستاتين ، وسلفوناميد مضادات حيوية.
تشمل الأدوية التي قد تقلل من تأثير خفض نسبة الجلوكوز في الدم في الأبيدرا الكورتيكوستيرويدات ، النياسين ، دانازول ، مدرات البول ، عوامل محاكية الودي (على سبيل المثال ، الإيبينيفرين ، ألبوتيرول ، تيربوتالين) ، الجلوكاجون ، أيزونيازيد ، مشتقات الفينوثيازين ، السوماتروبين ، هرمونات الغدة الدرقية ، هرمون الاستروجين ، بروجستيرونية المفعول (على سبيل المثال ، في موانع الحمل الفموية) ، مثبطات الأنزيم البروتيني مضادات الذهان.
حاصرات بيتا ، الكلونيدين ، أملاح الليثيوم ، والكحول قد تزيد أو تقلل من تأثير خفض نسبة الجلوكوز في الدم للأنسولين.
قد يسبب البنتاميدين نقص السكر في الدم ، والذي قد يتبعه أحيانًا ارتفاع السكر في الدم.
قد تنخفض أو تنقص علامات نقص السكر في الدم لدى المرضى الذين يتناولون الأدوية المضادة للأدرين مثل حاصرات بيتا ، الكلونيدين ، غوانيثيدين ، وريسبيربين.
أعلى
استخدام في السكان محددة
حمل
الحمل الفئة C: أجريت دراسات التكاثر وعلم الفيروسات باستخدام الأنسولين glulisine في الفئران والأرانب باستخدام الأنسولين البشري العادي كمقارن. أعطيت الأنسولين glulisine للفئران أثناء الحمل بجرعات تحت الجلد تصل إلى 10 وحدات / كجم مرة واحدة يوميًا (الجرعة الناتجة عن التعرض مرتين في الجرعة البشرية المتوسطة ، بناءً على مقارنة مساحة سطح الجسم) ولم يكن له أي آثار سامة ملحوظة على الجنين الجنيني تطوير.
أعطيت الأنسولين glulisine للأرانب الإناث طوال فترة الحمل بجرعات تحت الجلد تصل إلى 1.5 الوحدات / كجم / يوم (الجرعة الناتجة عن التعرض 0.5 أضعاف متوسط الجرعة البشرية ، على أساس مساحة سطح الجسم مقارنة). شوهدت التأثيرات الضائرة على تطور الجنين فقط عند مستويات الجرعة السامة للأم التي تسبب نقص السكر في الدم. لوحظت زيادة في حالات فقدان ما بعد الزرع والعيوب الهيكلية عند مستوى جرعة 1.5 وحدة / كجم مرة واحدة يوميًا (الجرعة مما أدى إلى التعرض 0.5 أضعاف متوسط الجرعة البشرية ، استنادا إلى مقارنة مساحة سطح الجسم) التي تسببت أيضا في وفيات السدود. لوحظ حدوث زيادة طفيفة في خسائر ما بعد الزرع عند مستوى الجرعة الأدنى التالي البالغ 0.5 وحدة / كجم مرة واحدة يوميًا (الجرعة الناتجة عن التعرض 0.2 أضعاف الجرعة البشرية المتوسطة ، بناءً على مقارنة مساحة سطح الجسم) والتي ارتبطت أيضًا بنقص السكر في الدم الحاد ولكن لم تكن هناك عيوب في ذلك جرعة. لم تلاحظ أي آثار على الأرانب بجرعة 0.25 وحدة / كغم مرة واحدة يوميًا (الجرعة الناتجة عن التعرض 0.1 ضعف متوسط الجرعة البشرية ، بناءً على مقارنة مساحة سطح الجسم). لم تختلف آثار الأنسولين glulisine عن تلك التي لوحظت مع الأنسولين البشري العادي تحت الجلد بنفس الجرعات وعزت إلى الآثار الثانوية لنقص السكر في الدم لدى الأمهات.
لا توجد دراسات سريرية جيدة السيطرة على استخدام الأبيدرا عند النساء الحوامل. نظرًا لأن دراسات تكاثر الحيوانات لا تنبئ دائمًا بالاستجابة البشرية ، يجب ألا يستخدم هذا الدواء أثناء الحمل إلا إذا كانت الفائدة المحتملة تبرر الخطر المحتمل على الجنين. من الضروري للمرضى الذين يعانون من مرض السكري أو تاريخ من سكري الحمل الحفاظ على السيطرة الأيضية الجيدة قبل الحمل وطوال فترة الحمل. قد تنخفض متطلبات الأنسولين خلال الأشهر الثلاثة الأولى ، وتزيد بشكل عام خلال الثلث الثاني والثالث ، وتنخفض بسرعة بعد الولادة. المراقبة الدقيقة للسيطرة على الجلوكوز ضرورية في هؤلاء المرضى.
الأمهات المرضعات
من غير المعروف ما إذا كان يتم إفراز الأنسولين glulisine في اللبن البشري. نظرًا لإفراز العديد من الأدوية في اللبن البشري ، يجب توخي الحذر عند إعطاء Apidra لمرضعة. استخدام Apidra متوافق مع الرضاعة الطبيعية ، لكن النساء المصابات بمرض السكري اللائي يُرضعن قد يتطلبن إجراء تعديلات على جرعات الأنسولين.
استخدام الأطفال
تم تأسيس سلامة وفعالية الحقن تحت الجلد لأبيدرا في مرضى الأطفال (من عمر 4 إلى 17 عامًا) المصابين بالنوع الأول من مرض السكري [انظر الدراسات السريرية]. لم تدرس Apidra في مرضى الأطفال المصابين بداء السكري من النوع 1 الذين تقل أعمارهم عن 4 سنوات وفي مرضى الأطفال المصابين بداء السكري من النوع 2.
كما هو الحال في البالغين ، يجب أن تكون جرعة Apidra فردية في مرضى الأطفال على أساس الاحتياجات الأيضية والرصد المتكرر لنسبة السكر في الدم.
استخدام المسنين
في التجارب السريرية (ن = 2408) ، كانت تدار Apidra إلى 147 مريضا ¥ ¥ 65 سنة و 27 مريضا ¥ ¥ 75 سنة من العمر. كانت غالبية هذه المجموعة الصغيرة من المرضى المسنين من النوع الثاني من السكري. لم يختلف التغير في قيم HbA1c وترددات السكر في الدم حسب العمر. ومع ذلك ، يجب توخي الحذر عند إعطاء Apidra لمرضى الشيخوخة.
أعلى
جرعة زائدة
الأنسولين الزائد قد يسبب نقص السكر في الدم ، وخاصة عندما يعطى عن طريق الوريد ، نقص بوتاسيوم الدم. نوبات خفيفة من نقص السكر في الدم يمكن علاجها عادة بالجلوكوز عن طريق الفم. قد يلزم إجراء تعديلات في جرعة الدواء أو أنماط الوجبة أو التمرين. يمكن علاج نوبات نقص السكر في الدم الأكثر شدة مع الغيبوبة أو النوبات العصبية أو الخلل العصبي بواسطة الجلوكاجون العضلي / تحت الجلد أو الجلوكوز المركز في الوريد. قد تكون كمية الكربوهيدرات المستديمة والملاحظة ضرورية لأن نقص السكر في الدم قد يتكرر بعد الشفاء السريري الظاهر. يجب تصحيح نقص بوتاسيوم الدم بشكل مناسب.
وصف
Apidra® (حقن الأنسولين glulisine [منشأ rDNA]) هو تمثيلي سريع للأنسولين البشري يستخدم لخفض نسبة الجلوكوز في الدم. يتم إنتاج الأنسولين glulisine بواسطة تقنية الحمض النووي المؤتلف باستخدام سلالة معملية غير مسببة للأمراض من الإشريكية القولونية (K12). يختلف الأنسولين glulisine عن الأنسولين البشري ، حيث يتم استبدال الهليون الحمضي الأميني في الموضع B3 بالليسين ، ويتم استبدال الليسين الموجود في الموضع B29 بحمض الجلوتاميك. كيميائيا ، الأنسولين glulisine هو 3B-lysine-29B-glutamic acid-insulin ، له الصيغة التجريبية C258H384N64O78S6 ويبلغ الوزن الجزيئي 5823 وله الصيغة الهيكلية التالية:
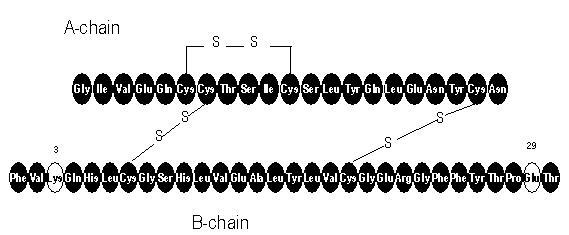
Apidra هو حل معقم ، مائي ، واضح ، عديم اللون. يحتوي كل ملليلتر من Apidra على 100 وحدة (3.49 مجم) من الأنسولين glulisine و 3.15 mg metacresol و 6 mg tromethamine و 5 مجم من كلوريد الصوديوم و 0.01 mg polysorbate 20 وماء للحقن. Apidra لديه درجة الحموضة حوالي 7.3. يتم ضبط درجة الحموضة عن طريق إضافة المحاليل المائية من حمض الهيدروكلوريك و / أو هيدروكسيد الصوديوم.
أعلى
علم الصيدلة السريرية
آلية العمل
تنظيم استقلاب الجلوكوز هو النشاط الأساسي للأنسولين ونظائر الأنسولين ، بما في ذلك الأنسولين الجلوليزين. تعمل الإنسولين على خفض نسبة الجلوكوز في الدم عن طريق تحفيز امتصاص الجلوكوز المحيطي عن طريق العضلات والدهون الهيكلية ، وعن طريق تثبيط إنتاج الجلوكوز الكبدي. تمنع الإنسولين تحلل الدهون والبروتينات ، وتعزز تخليق البروتين.
تكون أنشطة خفض نسبة الجلوكوز في Apidra والأنسولين البشري المنتظم متوازنة عند إعطائها عن طريق الوريد. بعد الإعطاء تحت الجلد ، يكون تأثير أبيدرا أسرع في بدايته وأقصر مدة مقارنةً بالأنسولين البشري العادي. [انظر الديناميكا الدوائية].
الدوائية
أظهرت الدراسات التي أجريت على متطوعين أصحاء ومرضى السكري أن Apidra لديه سرعة أكبر بداية النشاط ومدة نشاط أقصر من الأنسولين البشري العادي عند تناوله تحت الجلد.
في دراسة أجريت على مرضى السكري من النوع 1 (ن = 20) ، لمحات خفض الجلوكوز من Apidra و تم تقييم الأنسولين البشري العادي في أوقات مختلفة فيما يتعلق بوجبة قياسية بجرعة 0.15 وحدة / كغ. (شكل 1.)
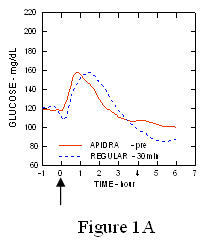
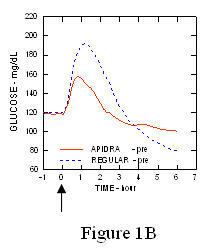
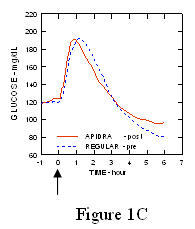
أقصى رحلة الجلوكوز في الدم (Î "GLUmax ؛ خط الأساس تركيز الجلوكوز المخصوم) لحقن الأبيدرا قبل دقيقتين من الوجبة كان 65 ملغ / ديسيلتر مقارنة بـ 64 ملغ / ديسيلتر للإنسان العادي حقن الأنسولين قبل الوجبة بثلاثين دقيقة (انظر الشكل 1 أ) ، و 84 ملغ / ديسيلتر للإنسولين البشري العادي الذي يتم حقنه قبل دقيقتين من الوجبة (انظر الشكل 1B). كان الحد الأقصى لرحلة الجلوكوز في الدم لأبيدرا الذي تم حقنه بعد 15 دقيقة من بدء الوجبة هو 85 ملغ / ديسيلتر مقارنة مع 84 ملغ / ديسيلتر للأنسولين البشري العادي حقن 2 دقيقة قبل وجبة (انظر الشكل 1C).
شكل 1. المسلسل يعني نسبة الجلوكوز في الدم التي تم جمعها لمدة تصل إلى 6 ساعات بعد جرعة واحدة من Apidra والأنسولين البشري العادي. يعطى Apidra دقيقتين (Apidra - قبل) قبل بدء الوجبة مقارنةً بالأنسولين البشري العادي المعطى لمدة 30 دقيقة (منتظم - 30 دقيقة) قبل بدء الوجبة (الشكل 1 أ) ومقارنتها بالأنسولين البشري العادي (منتظم - قبل) المعطى قبل دقيقتين من الوجبة (الشكل 1B). يعطى Apidra 15 دقيقة (Apidra - post) بعد بدء الوجبة مقارنة بالأنسولين البشري العادي (منتظم - قبل) يعطى قبل دقيقتين من الوجبة (الشكل 1C). على المحور السيني الصفر (0) هو بداية وجبة لمدة 15 دقيقة.
 |
 |
 |
 |
في دراسة عشوائية متفتحة ذات علامات ثنائية ، تلقى 16 رجلاً ذكور يتمتعون بصحة جيدة عن طريق الوريد تسريب Apidra أو الأنسولين البشري العادي بمحلول ملحي بمعدل 0.8 ملل / وحدة / دقيقة لشخصين ساعات. التسريب من نفس جرعة Apidra أو الأنسولين البشري المنتظم ينتج ما يعادل التخلص من الجلوكوز في حالة مستقرة.
الدوائية
الامتصاص والتوافر الحيوي
أظهرت ملامح الحركية الدوائية لدى المتطوعين الأصحاء والمرضى الذين يعانون من مرض السكري (النوع 1 أو النوع 2) أن امتصاص الأنسولين glulisine كان أسرع من الأنسولين البشري العادي.
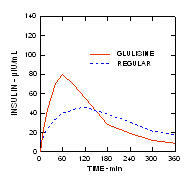
في دراسة أجريت على مرضى السكري من النوع 1 (ن = 20) بعد إعطاء تحت الجلد 0.15 وحدة / كجم ، متوسط الوقت إلى أقصى تركيز (Tmax) كان 60 دقيقة (المدى من 40 إلى 120 دقيقة) وكان تركيز الذروة (Cmax) 83 ميكرونيت / مل (نطاق 40 إلى 131 ميكرونيت / مل) للأنسولين glulisine مقارنة بمتوسط Tmax يبلغ 120 دقيقة (يتراوح من 60 إلى 239 دقيقة) و Cmax من 50 وحدة صغيرة / مل (نطاق من 35 إلى 71 وحدة صغيرة / مل) للإنسان العادي الأنسولين. (الشكل 2)
الشكل 2. الملامح الدوائية للأنسولين glulisine والأنسولين البشري المنتظم لدى مرضى السكري من النوع 1 بعد جرعة مقدارها 0.15 وحدة / كجم.
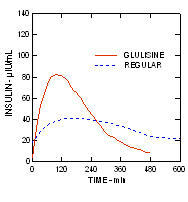
الأنسولين glulisine والأنسولين البشري العادي كانت تدار تحت الجلد بجرعة 0.2 وحدة / كيلوغرام في دراسة المشبك النابض في مرضى السكري من النوع 2 (ن = 24) ومؤشر كتلة الجسم (BMI) بين 20 و 36 كجم / M2. متوسط الوقت إلى أقصى تركيز (Tmax) كان 100 دقيقة (المدى من 40 إلى 120 دقيقة) وكان متوسط تركيز الذروة (Cmax) 84 ميكرونيت / مل (المدى 53 إلى 165 ميكرونيت / مل) للجلوليولين الأنسولين مقارنة مع متوسط Tmax من 240 دقيقة (المدى من 80 إلى 360 دقيقة) ومتوسط Cmax من 41 ميكرونيت / مل (مدى 33 إلى 61 ميكرونيت / مل) للأنسولين البشري العادي. (الشكل 3.)
الشكل 3. الملامح الدوائية للأنسولين glulisine والأنسولين البشري المنتظم لدى مرضى السكري من النوع 2 بعد جرعة تحت الجلد تبلغ 0.2 وحدة / كجم.
عندما تم حقن Apidra تحت الجلد في مناطق مختلفة من الجسم ، كانت ملامح تركيز الوقت متشابهة. التوافر الحيوي المطلق للجلوليولين الأنسولين بعد إعطاء تحت الجلد حوالي 70 ٪ ، بغض النظر عن منطقة الحقن (البطن 73 ٪ ، الدالية 71 ٪ ، الفخذ 68 ٪).
في دراسة سريرية على متطوعين أصحاء (ن = 32) كان التوافر البيولوجي الكلي للأنسولين glulisine مشابهًا بعد الجلد حقن الأنسولين glulisine والأنسولين NPH (المخلوط مسبقًا في المحاقن) وبعد الجلد تحت الجلد في وقت واحد منفصل الحقن. كان هناك 27 ٪ من توهين الحد الأقصى للتركيز (Cmax) من Apidra بعد الخلط ؛ ومع ذلك ، لم يتأثر الوقت الأقصى للتركيز (Tmax). لا توجد بيانات متاحة حول خلط Apidra مع مستحضرات الأنسولين غير الأنسولين NPH. [نرى الدراسات السريرية].
التوزيع والقضاء
توزيع وإزالة الأنسولين glulisine والإنسولين البشري العادي بعد الوريد تتشابه الإدارة مع حجم توزيع 13 و 21 لتر ونصف عمر 13 و 17 دقيقة ، على التوالي. بعد تناوله تحت الجلد ، يتم التخلص من الأنسولين glulisine بسرعة أكبر من الأنسولين البشري العادي مع فترة نصف عمر واضحة تبلغ 42 دقيقة مقارنة بـ 86 دقيقة.
علم الصيدلة السريرية في مجموعات سكانية محددة
الأطفال المرضى
تم تقييم الخواص الدوائية والدوائية الديناميكية لأبيدرا والأنسولين البشري العادي في دراسة أجريت على الأطفال من 7 إلى 11 سنة (ن = 10) والمراهقين 12 إلى 16 سنة (ن = 10) مع النوع 1 داء السكري. الاختلافات النسبية في الحرائك الدوائية والديناميكا الدوائية بين الأبيدرا والأنسولين البشري المنتظم في كان هؤلاء المرضى الذين يعانون من مرض السكري من النوع الأول مشابهين لمرضى البالغين الأصحاء والبالغين المصابين بالنوع 1 داء السكري.
سباق
قارنت دراسة أجريت على 24 قوقازيًا صحيًا ومواضيع يابانية بين الحرائك الدوائية والديناميكا الدوائية بعد الحقن تحت الجلد للجلوليولين الأنسولين ، والأنسولين ليسبرو ، والأنسولين البشري العادي. مع الحقن تحت الجلد من الأنسولين glulisine ، تعرض الأشخاص اليابانيون إلى تعرض أولي أكبر (33٪) لنسبة AUC (0-1h) إلى AUC (0-clamp end) من القوقازيين (21٪) على الرغم من أن إجمالي التعرضات كانت مماثل. كانت هناك نتائج مماثلة مع الأنسولين lispro والأنسولين البشري العادي.
بدانة
الأنسولين glulisine والأنسولين البشري العادي كانت تدار تحت الجلد بجرعة 0.3 وحدة / كيلوغرام في أ دراسة المشبك النحاسي في الأشخاص الذين يعانون من السمنة المفرطة وغير المصابين بالسكري (ن = 18) مع مؤشر كتلة الجسم (BMI) بين 30 و 40 كجم / M2. كان متوسط الوقت لتركيز أقصى (Tmax) 85 دقيقة (المدى 49 إلى 150 دقيقة) وكان متوسط تركيز الذروة (Cmax) 192 ميكرونيت / مل (المدى 98 إلى 380 ميكرونيت / مل) للجلولين الأنسولين مقارنة بمتوسط Tmax من 150 دقيقة (من 90 إلى 240 دقيقة) و Cmax متوسط من 86 وحدة / مل (نطاق 43 إلى 175 وحدة / مل) للإنسان العادي الأنسولين.
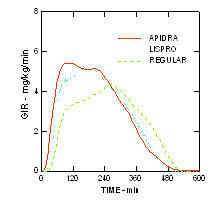
تم الحفاظ على بداية أسرع للعمل ومدة أقصر من نشاط Apidra والأنسولين lispro مقارنة مع الأنسولين البشري العادي في السكان غير المصابين بالسكري يعانون من السمنة المفرطة (ن = 18). (الشكل 4.)
الشكل 4. معدلات ضخ الجلوكوز (GIR) في دراسة المشبك النابض بعد الحقن تحت الجلد من 0.3 وحدة / كيلوغرام من Apidra ، الأنسولين lispro أو الأنسولين البشري العادي في السكان يعانون من السمنة المفرطة.
القصور الكلوي
أظهرت الدراسات التي أجريت على الأنسولين البشري زيادة مستويات الأنسولين في المرضى الذين يعانون من الفشل الكلوي. في دراسة أجريت على 24 شخصًا غير مصابين بالسكري مع وظيفة كلوية طبيعية (ClCr> 80 مل / دقيقة) ، وضعف كلوي معتدل (30-50 مل / دقيقة) وضعف كلوي حاد (التحذيرات والاحتياطات].
اختلال كبدي
لم يتم دراسة تأثير الاختلال الكبدي على الحرائك الدوائية والديناميكية الدوائية لأبيدرا. أظهرت بعض الدراسات التي أجريت على الأنسولين البشري زيادة في مستويات الأنسولين في المرضى الذين يعانون من قصور الكبد. [نرى المحاذير والإحتياطات].
جنس
لم يتم دراسة تأثير الجنس على الحرائك الدوائية والديناميكية الدوائية لأبيدرا.
حمل
لم يتم دراسة تأثير الحمل على الحرائك الدوائية والديناميكية الدوائية لأبيدرا.
التدخين
لم يتم دراسة تأثير التدخين على الحرائك الدوائية والديناميكية الدوائية لأبيدرا.
أعلى
علم السموم غير الإكلينيكي
التسرطن والطفرات وضعف الخصوبة
لم يتم إجراء دراسات سرطانية قياسية لمدة عامين على الحيوانات. في الفئران Sprague Dawley ، أجريت دراسة سمية للجرعة المتكررة لمدة 12 شهرًا باستخدام الأنسولين glulisine بجرعات تحت الجلد من 2.5 أو 5 أو 20 أو 50 وحدة / كجم مرتين يوميًا (الجرعة الناتجة عن التعرض 1 و 2 و 8 و 20 ضعف متوسط الجرعة البشرية ، استنادًا إلى مساحة سطح الجسم مقارنة).
كان هناك ارتفاع في معدل الإصابة بأورام الغدة الثديية في الجرذان التي تديرها الأنسولين glulisine مقارنة مع الضوابط غير المعالجة. كانت نسبة حدوث أورام الثدي بالنسبة لجلوليولين الأنسولين والإنسولين البشري العادي مماثلة. أهمية هذه النتائج للبشر غير معروفة. لم يكن الأنسولين glulisine مطفرا في الاختبارات التالية: اختبار أميس ، في كروموسوم الثدييات المختبر اختبار انحراف في خلايا الهامستر الصينية V79 ، واختبار نواة كريات الدم الحمراء في الجسم الحي الفئران.
في دراسات الخصوبة لدى فئران ذكور وإناث بجرعات تحت الجلد تصل إلى 10 وحدات / كغ مرة واحدة يوميًا (الجرعة تؤدي إلى التعرض مرتين في المتوسط للإنسان الجرعة ، على أساس مقارنة مساحة سطح الجسم) ، لم تكن هناك آثار ضارة واضحة على خصوبة الذكور والإناث ، أو الأداء التناسلي العام للحيوانات ملاحظ.
أعلى
الدراسات السريرية
تمت دراسة سلامة وفعالية Apidra في المرضى البالغين الذين يعانون من مرض السكري من النوع 1 والنوع 2 (ن = 1833) وفي الأطفال والمرضى المراهقين (4 إلى 17 سنة) مع مرض السكري من النوع 1 (ن = 572). كانت المعلمة الفعالية الأولية في هذه التجارب السيطرة على نسبة السكر في الدم ، وتقييمها باستخدام الهيموغلوبين السكري (ذكرت GHb كما يعادل HbA1c).
مرض السكري من النوع 1 - البالغين
تم إجراء دراسة عشوائية مدتها 26 أسبوعًا ، وعملية فتح علامة مفتوحة ، غير خاضعة للرقابة ، على مرضى السكري من النوع الأول لتقييم سلامة وفعالية Apidra (ن = 339) مقارنة بالأنسولين ليسبرو (ن = 333) عندما تدار تحت الجلد في غضون 15 دقيقة قبل وجبة. كانت تدار الأنسولين glargine مرة واحدة يوميا في المساء كما الأنسولين القاعدي. كان هناك فترة تشغيل لمدة 4 أسابيع مع الأنسولين ليسبرو وغلارجين الأنسولين قبل التوزيع العشوائي. وكان معظم المرضى قوقازي (97 ٪). ثمانية وخمسون في المئة من المرضى من الرجال. كان متوسط العمر 39 عامًا (يتراوح من 18 إلى 74 عامًا). كانت السيطرة على نسبة السكر في الدم ، وعدد حقن الأنسولين اليومي قصير المفعول والجرعات اليومية الإجمالية من Apidra والأنسولين ليسبرو مماثلة في مجموعات العلاج اثنين (الجدول 6).
الجدول 6: داء السكري من النوع 1 - بالغ
| مدة العلاج العلاج بالاشتراك مع: |
26 أسبوع الأنسولين glargine |
|
|---|---|---|
| أبيدرا | الأنسولين ليسبرو | |
| ||
| الهيموغلوبين السكري (GHb)* (%) | ||
| عدد المرضى | 331 | 322 |
| خط الأساس يعني | 7.6 | 7.6 |
| تعديل يعني التغيير من الأساس | -0.1 | -0.1 |
| علاج الفرق: Apidra - الأنسولين Lispro | 0.0 | |
| 95 ٪ CI لفرق العلاج | (-0.1; 0.1) | |
| جرعة الأنسولين القاعدية (وحدات / يوم) | ||
| خط الأساس يعني | 24 | 24 |
| تعديل يعني التغيير من الأساس | 0 | 2 |
| جرعة الأنسولين قصيرة المفعول (وحدات / يوم) | ||
| خط الأساس يعني | 30 | 31 |
| تعديل يعني التغيير من الأساس | -1 | -1 |
| متوسط عدد حقن الأنسولين قصير المفعول في اليوم الواحد | 3 | 3 |
| وزن الجسم (كجم) | ||
| خط الأساس يعني | 73.9 | 74.1 |
| يعني التغيير من الأساس | 0.6 | 0.3 |
داء السكري من النوع 2 - البالغين
تم إجراء دراسة عشوائية مدتها 26 أسبوعًا ، وعملية فتح علامة مفتوحة ، غير خاضعة للرقابة ، على المرضى المعالجين بالأنسولين المصابين بداء السكري من النوع 2 لتقييم سلامة وفعالية Apidra (ن = 435) تعطى في غضون 15 دقيقة قبل وجبة مقارنة بالأنسولين البشري العادي (ن = 441) تدار 30 إلى 45 دقيقة قبل وجبة. أعطيت الأنسولين البشري NPH مرتين في اليوم كما الأنسولين القاعدي. شارك جميع المرضى في فترة تشغيل مدتها 4 أسابيع مع الأنسولين البشري العادي والأنسولين البشري NPH. خمسة وثمانون في المئة من المرضى كانوا من القوقاز و 11 ٪ من السود. كان متوسط العمر 58 عامًا (يتراوح من 26 إلى 84 عامًا). وكان متوسط مؤشر كتلة الجسم (BMI) 34.6 كجم / م 2. في العشوائية ، كان 58 ٪ من المرضى يتناولون مضادات السكري عن طريق الفم. تم توجيه هؤلاء المرضى لمواصلة استخدام عامل مضاد للسكري عن طريق الفم في نفس الجرعة طوال المحاكمة. غالبية المرضى (79 ٪) خلط الأنسولين قصير المفعول مع الأنسولين البشري NPH مباشرة قبل الحقن. كانت التخفيضات من خط الأساس في GHb مماثلة بين مجموعات العلاج 2 (انظر الجدول 7). لم تلاحظ فروق بين Apidra ومجموعات الأنسولين البشري العادية في عدد حقن الأنسولين اليومية قصيرة المفعول أو جرعات الأنسولين القاعدية أو قصيرة المفعول. (انظر الجدول 7.)
الجدول 7: مرض السكري من النوع 2 - الكبار
| مدة العلاج | 26 أسبوع | |
|---|---|---|
| العلاج بالاشتراك مع: | الأنسولين البشري NPH | |
| أبيدرا | الأنسولين البشري العادي | |
| ||
| الهيموغلوبين السكري (GHb)* (%) | ||
| عدد المرضى | 404 | 403 |
| خط الأساس يعني | 7.6 | 7.5 |
| تعديل يعني التغيير من الأساس | -0.5 | -0.3 |
| اختلاف العلاج: Apidra - الأنسولين البشري العادي | -0.2 | |
| 95 ٪ CI لفرق العلاج | (-0.3; -0.1) | |
| جرعة الأنسولين القاعدية (وحدات / يوم) | ||
| خط الأساس يعني | 59 | 57 |
| تعديل يعني التغيير من الأساس | 6 | 6 |
| جرعة الأنسولين قصيرة المفعول (وحدات / يوم) | ||
| خط الأساس يعني | 32 | 31 |
| تعديل يعني التغيير من الأساس | 4 | 5 |
| متوسط عدد حقن الأنسولين قصير المفعول في اليوم الواحد | 2 | 2 |
| وزن الجسم (كجم) | ||
| خط الأساس يعني | 100.5 | 99.2 |
| يعني التغيير من الأساس | 1.8 | 2.0 |
داء السكري من النوع 1 - البالغين: قبل وبعد تناول وجبة
وقد أجريت دراسة لمدة 12 أسبوعًا ، عشوائية ، مفتوحة ، نشطة ، غير متحكم فيها ، في المرضى الذين يعانون من مرض السكري من النوع 1 لتقييم سلامة وفعالية Apidra تدار في أوقات مختلفة فيما يتعلق أ وجبة. كانت تدار Apidra تحت الجلد إما في غضون 15 دقيقة قبل وجبة (ن = 286) أو مباشرة بعد أ كانت تدار وجبة (ن = 296) والأنسولين البشري العادي (ن = 278) تحت الجلد 30 إلى 45 دقيقة قبل وجبة. كانت تدار الأنسولين glargine مرة واحدة يوميا في وقت النوم والأنسولين القاعدي. كانت هناك فترة تشغيل مدتها 4 أسابيع مع الأنسولين البشري المنتظم وغلارجين الأنسولين يليه التوزيع العشوائي. وكان معظم المرضى قوقازي (94 ٪). كان متوسط العمر 40 عامًا (يتراوح من 18 إلى 73 عامًا). كان التحكم في نسبة السكر في الدم (انظر الجدول 8) مشابهًا لأنظمة العلاج الثلاثة. لم يلاحظ أي تغييرات من الأساس بين العلاجات في العدد الإجمالي اليومي لحقن الأنسولين قصيرة المفعول. (انظر الجدول 8.)
الجدول 8: قبل وبعد وجبة الإدارة في مرض السكري من النوع 1 - الكبار
| مدة العلاج العلاج بالاشتراك مع: |
12 أسبوع الأنسولين glargine |
12 أسبوع الأنسولين glargine |
12 أسبوع الأنسولين glargine |
|---|---|---|---|
| أبيدرا قبل الوجبة |
أبيدرا بعد وجبة |
الأنسولين البشري العادي | |
| |||
| الهيموغلوبين السكري (GHb)* (%) | |||
| عدد المرضى | 268 | 276 | 257 |
| خط الأساس يعني | 7.7 | 7.7 | 7.6 |
| تعديل يعني التغيير من الأساس†| -0.3 | -0.1 | -0.1 |
| جرعة الأنسولين القاعدية (وحدات / يوم) | |||
| خط الأساس يعني | 29 | 29 | 28 |
| تعديل يعني التغيير من الأساس | 1 | 0 | 1 |
| جرعة الأنسولين قصيرة المفعول (وحدات / يوم) | |||
| خط الأساس يعني | 29 | 29 | 27 |
| تعديل يعني التغيير من الأساس | -1 | -1 | 2 |
| متوسط عدد حقن الأنسولين قصير المفعول في اليوم الواحد | 3 | 3 | 3 |
| وزن الجسم (كجم) | |||
| خط الأساس يعني | 79.2 | 80.3 | 78.9 |
| يعني التغيير من الأساس | 0.3 | -0.3 | 0.3 |
مرض السكري من النوع 1 - الأطفال
أجريت دراسة عشوائية مدتها 26 أسبوعًا وعملية التصنيف غير نشطة ذات دلالة مفتوحة على الأطفال والمراهقين الذين تزيد أعمارهم عن 4 سنوات من النوع 1 داء السكري لتقييم سلامة وفعالية Apidra (ن = 277) مقارنة بالأنسولين ليسبرو (ن = 295) عند تناوله تحت الجلد في غضون 15 دقيقة قبل وجبة. كما تلقى المرضى غلارجولين الأنسولين (يعطى مرة واحدة يوميًا في المساء) أو الأنسولين NPH (يعطى مرة واحدة في الصباح ومرة في المساء). كان هناك فترة تشغيل لمدة 4 أسابيع مع الأنسولين ليسبرو وغلارجين الأنسولين أو NPH قبل التوزيع العشوائي. وكان معظم المرضى قوقازي (91 ٪). وكان خمسون في المئة من المرضى من الذكور. كان متوسط العمر 12.5 سنة (تتراوح من 4 إلى 17 سنة). كان متوسط مؤشر كتلة الجسم 20.6 كجم / م 2. كان التحكم في نسبة السكر في الدم (انظر الجدول 9) مشابهًا لنظامي العلاج.
الجدول 9: نتائج دراسة استمرت 26 أسبوعًا على مرضى الأطفال المصابين بداء السكري من النوع الأول
| أبيدرا | يسبرو] | |
|---|---|---|
| عدد المرضى | 271 | 291 |
| الأنسولين القاعدي | NPH أو الأنسولين glargine | NPH أو الأنسولين glargine |
| ||
| الهيموغلوبين السكري (GHb)* (%) | ||
| خط الأساس يعني | 8.2 | 8.2 |
| تعديل يعني التغيير من الأساس | 0.1 | 0.2 |
| علاج الفرق: يعني (فاصل الثقة 95 ٪) | -0.1 (-0.2, 0.1) | |
| جرعة الأنسولين القاعدية (وحدات / كجم / يوم) | ||
| خط الأساس يعني | 0.5 | 0.5 |
| يعني التغيير من الأساس | 0.0 | 0.0 |
| جرعة الأنسولين قصيرة المفعول (وحدات / كجم / يوم) | ||
| خط الأساس يعني | 0.5 | 0.5 |
| يعني التغيير من الأساس | 0.0 | 0.0 |
| متوسط عدد حقن الأنسولين قصير المفعول في اليوم الواحد | 3 | 3 |
| خط الأساس يعني وزن الجسم (كجم) | 51.5 | 50.8 |
| متوسط التغير في الوزن من خط الأساس (كجم) | 2.2 | 2.2 |
داء السكري من النوع 1 - البالغين: التسريب المستمر للأنسولين تحت الجلد
دراسة عشوائية نشطة لمدة 12 أسبوعًا (Apidra مقابل الأنسولين aspart) أجريت في البالغين المصابين بداء السكري من النوع 1 (Apidra n = 29 ، الأنسولين aspart n = 30) قام بتقييم استخدام Apidra في الأنسولين تحت الجلد المستمر الخارجي مضخة. وكان جميع المرضى قوقازي. كان متوسط العمر 46 عامًا (يتراوح من 21 إلى 73 عامًا). زيادة GHb يعني من الأساس إلى نقطة النهاية في كل من مجموعات العلاج (من 6.8 ٪ إلى 7.0 ٪ لأبيدرا ؛ من 7.1 ٪ إلى 7.2 ٪ للأنسولين الأسبارت).
أعلى
كيف زودت / التخزين والمناولة
كيف زودت
| |
| تتوفر وحدات Apidra 100 لكل مل (U-100) على النحو التالي: | |
| 10 مل قارورة | NDC 0088-2500-33 |
| 3 مل نظام خرطوشة*، حزمة من 5 | NDC 0088-2500-52 |
| 3 مل SoloStar القلم مملوءة مسبقا ، حزمة من 5 | NDC 0088-2502-05 |
لا يتم تضمين إبر القلم في الحزم.
يتم استخدام إبر القلم BD Ultra-Fine ™ بالاشتراك مع OptiClik بشكل منفصل ويتم تصنيعها بواسطة Becton Dickinson and Company.
Solostar متوافق مع جميع إبر القلم من Becton Dickinson and Company و Ypsomed و Owen Mumford.
تخزين
لا تستخدم بعد تاريخ انتهاء الصلاحية (انظر الكرتون والحاوية).
فيال / نظام خرطوشة غير مفتوح / SoloStar
يجب أن يتم تخزين قارورة Apidra غير مفتوحة وأنظمة الخراطيش و SoloStar في الثلاجة ، 36 درجة فهرنهايت 46 درجة فهرنهايت (2 درجة مئوية -8 درجة مئوية). احم من الضوء. يجب ألا يتم تخزين Apidra في الثلاجة ولا يجب السماح بتجميده. تجاهل إذا كان قد تم تجميده.
يجب استخدام أنظمة قارورة / خرطوشة غير مفتوحة / SoloStar غير مخزنة في الثلاجة في غضون 28 يومًا.
فتح (قيد الاستخدام) قارورة:
يجب استخدام قوارير مفتوحة ، سواء كانت مبردة أم لا ، في غضون 28 يومًا. إذا لم يكن التبريد ممكنًا ، يمكن إبقاء القارورة المفتوحة قيد الاستخدام دون تبريد لمدة تصل إلى 28 يومًا من الحرارة والضوء المباشر ، طالما أن درجة الحرارة لا تزيد عن 77 درجة فهرنهايت (25 درجة مئوية).
نظام خرطوشة مفتوح (قيد الاستخدام):
لا ينبغي أن يكون نظام خرطوشة الفتح (قيد الاستخدام) الذي تم إدخاله في OptiClik® مبردًا ولكن يجب أن يبقى أقل من 77 درجة فهرنهايت (25 درجة مئوية) بعيدًا عن الحرارة والضوء المباشر. يجب التخلص من نظام خرطوشة فتح (قيد الاستخدام) بعد 28 يومًا. لا تقم بتخزين OptiClik® ، مع أو بدون نظام خرطوشة ، في الثلاجة في أي وقت.
فتح (قيد الاستخدام) قلم SoloStar المملوء مسبقًا:
لا ينبغي تبريد SoloStar المفتوح (قيد الاستخدام) ولكن يجب إبقائه تحت 77 درجة فهرنهايت (25 درجة مئوية) بعيدا عن الحرارة والضوء المباشر. يجب التخلص من SoloStar المفتوح (قيد الاستخدام) المحفوظ في درجة حرارة الغرفة بعد 28 يومًا.
مجموعات التسريب:
يجب التخلص من مجموعات التسريب (الخزانات والأنابيب والقسطرة) والأبيدرا في الخزان بعد 48 ساعة من الاستخدام أو بعد التعرض لدرجات حرارة تتجاوز 98.6 درجة فهرنهايت (37 درجة مئوية).
استخدام الوريد:
أكياس ضخ أعدت كما هو موضح أدناه الجرعة والإدارة مستقرة في درجة حرارة الغرفة لمدة 48 ساعة.
التحضير والتعامل
بعد التخفيف للاستخدام في الوريد ، يجب فحص المحلول بصريًا بحثًا عن الجسيمات وتغير اللون قبل تناوله. لا تستخدم الحل إذا أصبح غائمًا أو يحتوي على جزيئات ؛ استخدم فقط إذا كان واضحًا وعديم اللون. لا يتوافق Apidra مع محلول Dextrose ومحلول Ringers ، وبالتالي ، لا يمكن استخدامه مع سوائل المحلول هذه. لم يتم دراسة استخدام Apidra مع حلول أخرى ، وبالتالي ، لا ينصح به.
نظام الخرطوشة: في حالة حدوث خلل في OptiClik® (جهاز تسليم الأنسولين لـ Apidra) ، يمكن سحب Apidra من نظام الخرطوشة إلى حقنة U-100 وحقنه.
Apidra ، الأنسولين glusine ، معلومات المريض (في سهل الانجليزية)
آخر تحديث: 02/2009
معلومات مفصلة عن العلامات والأعراض والأسباب والعلاج من مرض السكري
لا تهدف المعلومات الواردة في هذه الدراسة إلى تغطية جميع الاستخدامات أو الاتجاهات أو الاحتياطات الممكنة أو التفاعلات الدوائية أو الآثار الضارة. هذه المعلومات معممة ولا تهدف إلى تقديم المشورة الطبية المحددة. إذا كانت لديك أسئلة حول الأدوية التي تتناولها أو ترغب في مزيد من المعلومات ، فاستشر طبيبك أو الصيدلي أو الممرض.
ارجع الى: تصفح جميع الأدوية لمرض السكري



