Starlix لعلاج مرض السكري
اسم العلامة التجارية: Starlix
اسم عام: أقراص nateglinide
محتويات:
وصف
علم الصيدلة السريرية
الدراسات السريرية
المؤشرات والاستخدام
موانع
الاحتياطات
ردود الفعل السلبية
جرعة زائدة
الجرعة والإدارة
كيف زودت
Starlix ، nateglinide ، معلومات كاملة للمريض (في سهل الانجليزية)
وصف
Starlix® (nateglinide) هو عامل مضاد لمرض السكر عن طريق الفم يستخدم في إدارة داء السكري من النوع 2 [المعروف أيضًا باسم داء السكري غير المعتمد على الأنسولين (NIDDM) أو مرض السكري الذي يصيب البالغين]. Starlix ، (-) - N - [(trans-4-isopropylcyclohexane) carbonyl] -D-phenylalanine ، لا علاقة له من الناحية الهيكلية بسراغات الأنسولين السلفونيل يوريا عن طريق الفم.
الصيغة الهيكلية كما هو موضح
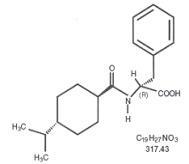
Nateglinide هو مسحوق أبيض مع وزن جزيئي قدره 317.43. وهو قابل للذوبان بحرية في الميثانول والإيثانول والكلوروفورم ، وهو قابل للذوبان في الأثير ، قابل للذوبان بشكل متفرق في أسيتونيتريل واوكتانول ، وغير قابل للذوبان عملياً في الماء. تحتوي أقراص Starlix biconvex على 60 ملغ ، أو 120 ملغ ، من النتلاينيد للإعطاء عن طريق الفم.
المكونات غير النشطة: ثاني أكسيد السيليكون الغروي ، كروسارميلوز الصوديوم ، هيدروكسي بروبيل ميثيل السلولوز ، أكاسيد الحديد (أحمر أو الأصفر) ، مونوهيدرات اللاكتوز ، ستيرات المغنيسيوم ، السليلوز الجريزوفولفين ، البولي إيثيلين جليكول ، البوفيدون ، التلك ، والتيتانيوم ثاني أكسيد.
أعلى
علم الصيدلة السريرية
آلية العمل
Nateglinide هو مشتق من الأحماض الأمينية يخفض مستويات الجلوكوز في الدم عن طريق تحفيز إفراز الأنسولين من البنكرياس. هذا العمل يعتمد على عمل خلايا بيتا في الجزر البنكرياس. يتفاعل Nateglinide مع قناة ATP الحساسة للبوتاسيوم (K + ATP) على خلايا بيتا البنكرياس. الاستقطاب اللاحق لخلية بيتا يفتح قناة الكالسيوم ، وينتج تدفق الكالسيوم وإفراز الأنسولين. يعتمد مدى إفراز الأنسولين على الجلوكوز ويقلل من مستويات الجلوكوز المنخفضة. Nateglinide انتقائي للغاية للأنسجة مع تقارب منخفض للقلب والعضلات الهيكلية.
الدوائية
استيعاب
بعد تناوله عن طريق الفم مباشرة قبل الوجبة ، يتم امتصاص النتكلينيد بسرعة مع متوسط تركيزات الذروة القصوى لعقاقير البلازما (Cmax) التي تحدث بشكل عام خلال ساعة واحدة (Tmax) بعد الجرعات. عندما تدار لمرضى السكري من النوع 2 على مدى الجرعة 60 ملغ إلى 240 ملغ ثلاث مرات في اليوم واحد الأسبوع ، أظهر nateglinide الدوائية الخطية لكلا AUC (منطقة تحت منحنى تركيز الوقت / البلازما) و Cmax. تم العثور على Tmax أيضًا بشكل مستقل عن الجرعة في هذا المريض. يقدر التوافر الحيوي المطلق بحوالي 73٪. عند إعطاء وجبات الطعام أو بعدها ، يظل مدى امتصاص النيتكلينيد (AUC) غير متأثر. ومع ذلك ، هناك تأخير في معدل الامتصاص يتميز بانخفاض في Cmax وتأخر في الوقت المناسب لذروة تركيز البلازما (Tmax). تتميز ملامح البلازما بعدة قمم لتركيز البلازما عند إعطاء nateglinide في ظروف الصيام. هذا التأثير يتضاءل عندما يؤخذ nateglinide قبل وجبة الطعام.
توزيع
استنادًا إلى البيانات التالية لإدارة الوريد (الوريد) عن طريق الوريد (الوريد) ، يقدر حجم الحالة المستقرة لتوزيع النتيكلينيد بحوالي 10 لترات في الأشخاص الأصحاء. يرتبط Nateglinide على نطاق واسع (98 ٪) ببروتينات المصل ، في المقام الأول الزلال في المصل ، وبدرجة أقل ± ± 1 بروتين سكري حمض. مدى ارتباط بروتين المصل مستقل عن تركيز الدواء على مدى اختبار يتراوح بين 0.1 و 10 ميكروغرام / مل.
التمثيل الغذائي
يتم استقلاب Nateglinide بواسطة نظام أوكسيديز متعدد الوظائف قبل التخلص منه. الطرق الرئيسية لعملية التمثيل الغذائي هي الهيدروكسيل تليها اقتران الجلوكورونيد. المستقلبات الرئيسية هي عوامل مضادة لمرض السكر أقل فعالية من nateglinide. يمتلك مستقلب الأيزوبرين البسيط فاعلية مماثلة لتلك الموجودة في nateglinide المركب الأصلي.
في المعمل ، تظهر البيانات أن النيتلاينيد يتم استقلابه في الغالب عن طريق انزيمات السيتوكروم P450 CYP2C9 (70٪) و CYP3A4 (30٪).
إفراز
يتم التخلص بسرعة وكاملة من Nateglinide وعناصره التالية بعد تناوله عن طريق الفم. في غضون 6 ساعات بعد الجرعات ، تم استرداد ما يقرب من 75 ٪ من 14-nateglinide تدار في البول. تم إفراغ ثلاثة وثمانين في المئة من 14-nateglinide في البول مع إزالة 10 ٪ إضافية في البراز. ما يقرب من 16 ٪ من 14C - nateglinide تفرز في البول كمركب الأصل. في جميع الدراسات التي أجريت على متطوعين أصحاء ومرضى السكري من النوع 2 ، انخفضت تركيزات بلازما nateglinide بسرعة مع متوسط عمر تقريبي يبلغ حوالي 1.5 ساعة. تمشياً مع فترة نصف العمر القصيرة للتخلص ، لم يكن هناك تراكم ظاهر للنايتكلينيد عند الجرعات المتعددة التي تصل إلى 240 مجم ثلاث مرات يوميًا لمدة 7 أيام.
تفاعل الأدوية
في دراسات استقلاب المخدرات في المختبر تشير إلى أن Starlix يتم استقلابه في الغالب بواسطة السيتوكروم P450 أيزوزيم CYP2C9 (70 ٪) وبدرجة أقل CYP3A4 (30 ٪). Starlix هو مثبط محتمل لإيزوزيم CYP2C9 في الجسم الحي كما هو مشار إليه من خلال قدرته على تثبيط عملية التمثيل الغذائي في المختبر من tolbutamide. لم يتم الكشف عن تثبيط التفاعلات الأيضية CYP3A4 في التجارب المختبرية.
Glyburide: في دراسة عشوائية متعددة الجرعات ، كان مرضى السكري من النوع 2 تعطى 120 ملغ Starlix ثلاث مرات في اليوم قبل وجبات الطعام ليوم واحد في تركيبة مع glyburide 10 ملغ يوميا. لم تكن هناك تعديلات ذات الصلة سريريا في الدوائية لأي وكيل.
الميتفورمين: عندما يتم إعطاء ستارليكس 120 ملغ ثلاث مرات يوميًا قبل تناول الوجبات مع الميتفورمين 500 ملغ ثلاث مرات مرات يوميا لمرضى السكري من النوع 2 ، لم تكن هناك تغييرات ذات الصلة سريريا في الدوائية لأي منهما وكيل.
الديجوكسين: عندما يدار Starlix 120 ملغ قبل وجبات الطعام في تركيبة مع جرعة واحدة من 1 ملغ من الديجوكسين للمتطوعين الأصحاء ، لم تكن هناك تغييرات ذات صلة سريرياً في الدوائية لأي منهما وكيل.
الوارفارين: عندما كانت تدار موضوعات صحية Starlix 120 ملغ ثلاث مرات يوميا قبل وجبات الطعام لمدة أربعة أيام في مع جرعة واحدة من الوارفارين 30 ملغ في اليوم 2 ، لم تكن هناك تغييرات في الدوائية لأي وكيل. لم يتأثر وقت البروثرومبين.
ديكلوفيناك: تناول جرعات الصباح والغداء من Starlix 120 ملغ مع 75 ملغ واحد جرعة ديكلوفيناك في المتطوعين الأصحاء لم تسفر عن أي تغييرات كبيرة في الدوائية لأي منهما وكيل.
السكان الخاصة
الشيخوخة: لم يؤثر العمر على خصائص الحرائك الدوائية للناجليكلينيد. لذلك ، لا تعديلات الجرعة ضرورية للمرضى المسنين.
بين الجنسين: لم يلاحظ أي فروق ذات دلالة إكلينيكية في الدوائية nateglinide بين الرجال والنساء. لذلك ، لا يلزم تعديل الجرعة بناءً على الجنس.
العرق: تشير نتائج تحليل الحرائك الدوائية للسكان ، بما في ذلك مواضيع القوقاز والأسود والأصول العرقية الأخرى ، إلى أن العرق ليس له تأثير يذكر على الحرائك الدوائية للناتكلينيد.
القصور الكلوي: بالمقارنة مع المواضيع الصحية المتطابقة ، والمرضى الذين يعانون من مرض السكري من النوع 2 و قصور كلوي معتدلة إلى شديدة (CrCl 15-50 مل / دقيقة) وليس على غسيل الكلى عرض واضح مماثل التخليص ، AUC ، و Cmax. المرضى الذين يعانون من مرض السكري من النوع 2 والفشل الكلوي في غسيل الكلى عرضت انخفاض التعرض الكلي للمخدرات. ومع ذلك ، فقد عانى مرضى غسيل الكلى أيضًا من انخفاض ارتباط البروتين بالبلازما مقارنة بالمتطوعين الأصحاء المتطابقين.
اختلال كبدي: تم زيادة الذروة والتعرض الكلي للناتكلينيد في موضوعات غير مصابة بالسكري مع قصور كبدي خفيف بنسبة 30٪ مقارنة بالمواضيع الصحية المتطابقة. يجب استخدام Starlix® (nateglinide) بحذر عند مرضى الكبد المزمن. (انظر الاحتياطات ، ضعف الكبد.)
الدوائية
يتم امتصاص Starlix بسرعة ويحفز إفراز البنكرياس للأنسولين في غضون 20 دقيقة من تناوله عن طريق الفم. عندما يتم تناول جرعة Starlix ثلاث مرات يوميًا قبل الوجبات ، يكون هناك ارتفاع سريع في أنسولين البلازما ، حيث تبلغ مستويات الذروة ما يقرب من ساعة واحدة بعد الجرعات وتراجع إلى خط الأساس بمقدار 4 ساعات بعد الجرعات.
في تجربة سريرية مزدوجة التعمية يتم التحكم فيها ، حيث تم إعطاء Starlix قبل كل ثلاثة تم تحديد مستويات الجلوكوز في البلازما على مدار 12 ساعة خلال النهار بعد 7 أسابيع علاج او معاملة. كانت تدار Starlix قبل 10 دقائق من وجبات الطعام. استندت وجبات الطعام على قوائم الحفاظ على وزن السكري القياسية مع إجمالي محتوى السعرات الحرارية على أساس ارتفاع كل موضوع. أنتجت Starlix انخفاضات ذات دلالة إحصائية في الصيام وسكر الدم بعد الأكل مقارنة مع الدواء الوهمي.
أعلى
الدراسات السريرية
تم اختيارهم بصورة عشوائية ما مجموعه 3566 مريضا في تسعة دراسات مزدوجة التعمية ، وهمي أو النشط التي تسيطر عليها 8-24 أسابيع في مدة لتقييم سلامة وفعالية Starlix® (nateglinide). كان 3،513 مريضا قيم الفعالية وراء خط الأساس. في هذه الدراسات كانت تدار Starlix ما يصل إلى 30 دقيقة قبل كل من ثلاث وجبات رئيسية يوميا.
Starlix® أحادي بالمقارنة مع الدواء الوهمي
في دراسة عشوائية ، مزدوجة التعمية ، وهمي تسيطر عليها ، لمدة 24 أسبوعا ، والمرضى الذين يعانون من مرض السكري من النوع 2 مع HbA1C â ‰ ¥ 6.8 ٪ تم اختيارهم بصورة عشوائية على النظام الغذائي وحده لتلقي إما Starlix (60 ملغ أو 120 ملغ ثلاث مرات يوميا قبل وجبات الطعام) أو وهمي. تراوحت نسبة HbA1C الأساسية من 7.9٪ إلى 8.1٪ و 77.8٪ من المرضى لم يتم علاجهم سابقًا من خلال العلاج المضاد لمرض السكر عن طريق الفم. كان على المرضى الذين عولجوا سابقًا بالأدوية المضادة لمرض السكر التوقف عن هذا الدواء لمدة شهرين على الأقل قبل التوزيع العشوائي. أدت إضافة Starlix قبل وجبات الطعام إلى تخفيضات كبيرة إحصائيا في متوسط HbA1C ويعني الجلوكوز في البلازما الصيام (FPG) مقارنة مع الدواء الوهمي (انظر الجدول 1). كانت التخفيضات في HbA1C و FPG مماثلة للمرضى الساذجة ، والأشخاص الذين تعرضوا سابقًا للأدوية المضادة لمرض السكر.
في هذه الدراسة ، تم الإبلاغ عن حلقة واحدة من نقص السكر في الدم الحاد (الجلوكوز في البلازما <36 ملغ / دل) في مريض عولج بـ Starlix 120 ملغ ثلاث مرات يوميًا قبل الوجبات. لم يختبر أي من المرضى نقص السكر في الدم الذي تطلب مساعدة من طرف ثالث. كان لدى المرضى الذين عولجوا بـ Starlix زيادة في الوزن ذات دلالة إحصائية مقارنةً بالعلاج الوهمي (انظر الجدول 1).
في دراسة عشوائية أخرى ، مزدوجة التعمية ، لمدة 24 أسبوعًا ، يتم التحكم فيها وهميًا ، تم اختيار عشوائي لمرضى السكري من النوع 2 لتلقي Starlix (120 ملغ ثلاث مرات يوميًا قبل الوجبات) ، الميتفورمين 500 ملغ (ثلاث مرات يوميًا) ، مزيج من ستارليكس 120 ملغ (ثلاث مرات يوميًا قبل الوجبات) والميتفورمين 500 ملغ (ثلاث مرات يوميًا) ، أو الوهمي. تراوح خط الأساس HbA1C من 8.3 ٪ إلى 8.4 ٪. سبعة وخمسون في المئة من المرضى لم يعالجوا من قبل عن طريق العلاج بمضادات السكر عن طريق الفم. أسفر العلاج أحادي النجم Starlix عن تخفيضات كبيرة في متوسط HbA1C و FPG المتوسط مقارنةً بالعلاج الوهمي التي كانت مماثلة لنتائج الدراسة المذكورة أعلاه (انظر الجدول 2).
الجدول 1: نتائج نقطة النهاية لدراسة جرعة ثابتة لمدة 24 أسبوعًا من العلاج الأحادي Starlix®
|
الوهمي |
Starlix® 60 ملغ ثلاث مرات اليومي قبل الوجبات |
Starlix® 120 ملغ ثلاث مرات اليومي قبل الوجبات |
|
| HBA1C (%) | N = 168 | N = 167 | N = 168 |
| خط الأساس (الوسط) | 8.0 | 7.9 | 8.1 |
| التغيير من خط الأساس (الوسط) | +0.2 | -0.3 | -0.5 |
| الفرق من الدواء الوهمي (الوسط) | -0.5 أ | -0.7 أ | |
| FPG (mg / dL) | N = 172 | N = 171 | N = 169 |
| خط الأساس (الوسط) | 167.9 | 161.0 | 166.5 |
| التغيير من خط الأساس (الوسط) | +9.1 | +0.4 | -4.5 |
| الفرق من الدواء الوهمي (الوسط) | -8.7 أ | -13.6 أ | |
| الوزن (كلغ) | N = 170 | N = 169 | N = 166 |
| خط الأساس (الوسط) | 85.8 | 83.7 | 86.3 |
| التغيير من خط الأساس (الوسط) | -0.7 | +0.3 | +0.9 |
| الفرق من الدواء الوهمي (الوسط) | +1.0 أ | +1.6 أ |
قيمة p â ‰ 4 0.004
Starlix® Monotherapy مقارنةً بالعوامل الأخرى المضادة لمرض السكر عن طريق الفم
غليبوريد
في غضون 24 أسبوعًا ، تجربة مزدوجة التعمية يتم التحكم فيها بشكل نشط ، ومرضى السكري من النوع 2 الذين كانوا يتناولون السلفونيل يوريا لمدة 3 أشهر والذين كان خط الأساس HbA1C - تم اختيارهم بصورة عشوائية 6.5 ٪ لتلقي Starlix (60 ملغ أو 120 ملغ ثلاث مرات يوميا قبل وجبات الطعام) أو glyburide 10 ملغ مرة واحدة اليومي. كان المرضى الذين تم اختيارهم بصورة عشوائية لستارليكس زيادات كبيرة في متوسط HbA1C ويعني FPG في نقطة النهاية مقارنة مع المرضى الذين تم اختيارهم بصورة عشوائية ل glyburide.
ميتفورمين
في دراسة عشوائية أخرى ، مزدوجة التعمية ، لمدة 24 أسبوعًا ، يتم التحكم فيها وهميًا ، تم اختيار عشوائي لمرضى السكري من النوع 2 لتلقي Starlix (120 ملغ ثلاث مرات يوميًا قبل الوجبات) ، الميتفورمين 500 ملغ (ثلاث مرات يوميًا) ، مزيج من ستارليكس 120 ملغ (ثلاث مرات يوميًا قبل الوجبات) والميتفورمين 500 ملغ (ثلاث مرات يوميًا) ، أو الوهمي. تراوح خط الأساس HbA1C من 8.3 ٪ إلى 8.4 ٪. سبعة وخمسون في المئة من المرضى لم يعالجوا من قبل عن طريق العلاج بمضادات السكر عن طريق الفم. كانت التخفيضات في متوسط HbA1C و FPG المتوسط عند نقطة النهاية مع حيد الميتفورمين أكبر بكثير من التخفيضات في هذه المتغيرات مع العلاج الأحادي Starlix (انظر الجدول 2). بالنسبة للعلاج الوهمي ، ارتبط العلاج الأحادي Starlix بزيادة كبيرة في متوسط الوزن ، في حين ارتبط الميتفورمين أحادي النقصان بشكل ملحوظ في متوسط الوزن. من بين مجموعة فرعية من المرضى الذين لا يتعاملون مع العلاج المضاد للسكري ، كانت التخفيضات في متوسط HbA1C و FPG المتوسط لـ Starlix monotherapy مماثلة لتلك الخاصة بالميتفورمين أحادي (انظر الجدول 2). من بين مجموعة فرعية من المرضى الذين عولجوا سابقًا بعوامل أخرى مضادة لمرض السكر ، وهي في المقام الأول غليبيريد ، HbA1C في Starlix زادت مجموعة العلاج الأحادي قليلاً من خط الأساس ، في حين تم تخفيض HbA1C في مجموعة الميتفورمين أحادي (انظر الجدول 2).
Starlix® الجمع بين العلاج
ميتفورمين
في دراسة عشوائية أخرى ، مزدوجة التعمية ، لمدة 24 أسبوعًا ، يتم التحكم فيها وهميًا ، تم اختيار عشوائي لمرضى السكري من النوع 2 لتلقي Starlix (120 ملغ ثلاث مرات يوميًا قبل الوجبات) ، الميتفورمين 500 ملغ (ثلاث مرات يوميًا) ، مزيج من ستارليكس 120 ملغ (ثلاث مرات يوميًا قبل الوجبات) والميتفورمين 500 ملغ (ثلاث مرات يوميًا) ، أو الوهمي. تراوح خط الأساس HbA1C من 8.3 ٪ إلى 8.4 ٪. سبعة وخمسون في المئة من المرضى لم يعالجوا من قبل عن طريق العلاج بمضادات السكر عن طريق الفم. كان يتعين على المرضى الذين عولجوا سابقًا بالأدوية المضادة لمرض السكر التوقف عن الدواء لمدة شهرين على الأقل قبل التوزيع العشوائي. أدى الجمع بين Starlix والميتفورمين إلى تخفيضات أكبر بكثير من الناحية الإحصائية في HbA1C و FPG مقارنة مع Starlix أو الميتفورمين أحادي (انظر الجدول 2). قام ستارليكس ، بمفرده أو بالاشتراك مع الميتفورمين ، بتخفيض ارتفاع الجلوكوز قبل الأكل بشكل ملحوظ من الوجبة السابقة إلى ساعتين بعد الوجبة مقارنةً بالعلاج الوهمي والميتفورمين وحده.
في هذه الدراسة ، تم الإبلاغ عن حلقة واحدة من نقص السكر في الدم الحاد (الجلوكوز في البلازما - 36 ملغ / ديسيلتر) في مريض يتلقى تم الإبلاغ عن مزيج من Starlix والميتفورمين وأربع حلقات من نقص السكر في الدم الحاد في مريض واحد في الميتفورمين ذراع العلاج. لم يختبر أي مريض حلقة من نقص السكر في الدم تطلبت مساعدة من طرف ثالث. مقارنة مع الدواء الوهمي ، ارتبط العلاج الأحادي Starlix بزيادة معتد بها إحصائياً في الوزن ، في حين لم يلاحظ أي تغيير كبير في الوزن مع العلاج Starlix والميتفورمين مجتمعة (انظر الجدول 2).
في تجربة أخرى مدتها 24 أسبوعًا ، تم فيها الدخول في تجربة مزدوجة التعمية ، يتم التحكم فيها عن طريق الدواء الوهمي ، وتم إدخال مرضى السكري من النوع 2 المصابون بـ HbA1C - 6.8٪ بعد العلاج بالميتفورمين (1500 ملغ يوميًا لمدة شهر واحد) لأول مرة في فترة تشغيل مدتها أربعة أسابيع من الميتفورمين أحادي (2000 ملغ يوميًا) ، ثم تم اختيارهم بصورة عشوائية لتلقي ستارليكس (60 ملغ أو 120 ملغ ثلاث مرات يوميًا قبل الوجبات) أو دواء وهمي بالإضافة إلى الميتفورمين. ارتبط الجمع بين العلاج مع Starlix والميتفورمين مع تخفيضات أكبر بكثير إحصائيا في HbA1C مقارنة مع حيد الميتفورمين (-0.4 ٪ و -0.6 ٪ لستارليكس 60 ملغ و Starlix 120 ملغ زائد الميتفورمين ، على التوالي).
الجدول 2: نتائج نقطة النهاية لدراسة لمدة 24 أسبوعًا من العلاج Starlix®monmon والجمع مع الميتفورمين
|
الوهمي |
Starlix® 120 ملغ ثلاث مرات يوميا قبل وجبات |
ميتفورمين 500 ملغ ثلاث مرات اليومي |
Starlix® 120 ملغ قبل وجبات زائد الميتفورمين * |
|
| HBA1C (%) | ||||
| الكل | N = 160 | N = 171 | N = 172 | N = 162 |
| خط الأساس (الوسط) | 8.3 | 8.3 | 8.4 | 8.4 |
| التغيير من خط الأساس (الوسط) | +0.4 | -0.4 قبل الميلاد | -0.8 ج | -1.5 |
| الفرق من الدواء الوهمي | -0.8 أ | -1.2 أ | -1.9 أ | |
| نان-هاء | N = 98 | N = 99 | N = 98 | N = 81 |
| خط الأساس (الوسط) | 8.2 | 8.1 | 8.3 | 8.2 |
| التغيير من خط الأساس (الوسط) | +0.3 | -0.7 ج | -0.8 ج | -1.6 |
| الفرق من الدواء الوهمي | -1.0 أ | -1.1 أ | -1.9 أ | |
| غير نان-هاء | N = 62 | N = 72 | N = 74 | N = 81 |
| خط الأساس (الوسط) | 8.3 | 8.5 | 8.7 | 8.7 |
| التغيير من خط الأساس (الوسط) | +0.6 | +0.004 قبل الميلاد | -0.8 ج | -1.4 |
| الفرق من الدواء الوهمي | -0.6 أ | -1.4 أ | -2.0 أ | |
| FPG (mg / dL) | ||||
| الكل | N = 166 | N = 173 | N = 174 | N = 167 |
| خط الأساس (الوسط) | 194.0 | 196.5 | 196.0 | 197.7 |
| التغيير من خط الأساس (الوسط) | +8.0 | -13.1 قبل الميلاد | -30.0 ج | -44.9 |
| الفرق من الدواء الوهمي | -21.1 أ | -38.0 أ | -52.9 أ | |
| الوزن (كلغ) | ||||
| الكل | N = 160 | N = 169 | N = 169 | N = 160 |
| خط الأساس (الوسط) | 85.0 | 85.0 | 86.0 | 87.4 |
| التغيير من خط الأساس (الوسط) | -0.4 | +0.9 قبل الميلاد | -0.1 | +0.2 |
| الفرق من الدواء الوهمي | +1.3 أ | +0.3 | +0.6 |
قيمة p â 5 5 0.05 مقابل الوهمي
b p-value ¤ ¤ 0.03 vs. ميتفورمين
c p-value ¤ 5 0.05 vs. مزيج
* تم إعطاء الميتفورمين ثلاث مرات يومياً
روزيجليتازون
تم إجراء تجربة لمدة 24 أسبوعًا ، متعددة المراكز مزدوجة التعمية ، وهمي تسيطر عليها في المرضى الذين يعانون من النوع 2 لم يتم السيطرة على مرض السكري بشكل كاف بعد استجابة علاجية للعلاج وحيد الصوديوم 8 ملغ اليومي. ارتبط إضافة Starlix (120 ملغ ثلاث مرات في اليوم مع وجبات الطعام) مع تخفيضات أكبر بكثير إحصائيا في HbA1C مقارنة مع العلاج بالروزيجليتازون. كان الفرق -0.77 ٪ في 24 أسبوعا. كان متوسط التغير في الوزن من خط الأساس حوالي 3 كجم للمرضى الذين عولجوا بـ Starlix plus rosiglitazone مقابل حوالي +1 كجم للمرضى الذين عولجوا بدواء وهمي بالإضافة إلى روزيجليتازون.
غليبوريد
في دراسة استمرت 12 أسبوعًا للمرضى المصابين بداء السكري من النوع 2 ، لم يتم التحكم بشكل كافٍ في الغلوبريد 10 ملغ مرة واحدة يوميًا ، إضافة Starlix (60 ملغ أو 120 ملغ ثلاث مرات يوميا قبل وجبات الطعام) لم تنتج أي إضافية فائدة.
أعلى
المؤشرات والاستخدام
يشار إلى Starlix® (nateglinide) كعامل مساعد في اتباع نظام غذائي وممارسة التمارين الرياضية لتحسين السيطرة على نسبة السكر في الدم لدى البالغين المصابين بداء السكري من النوع 2.
أعلى
موانع
بطلان Starlix® (nateglinide) في المرضى الذين يعانون من:
1. يعرف فرط الحساسية للدواء أو مكوناته غير النشطة.
2. مرض السكر النوع 1.
3. الحماض الكيتوني السكري. يجب أن يعامل هذا الشرط مع الأنسولين.
أعلى
الاحتياطات
نتائج الأوعية الدموية الكبرى: لم تكن هناك دراسات سريرية تثبت وجود أدلة قاطعة على الحد من مخاطر الأوعية الدموية الكبيرة باستخدام ستارليكس أو أي دواء آخر مضاد لمرض السكر.
نقص السكر في الدم: جميع الأدوية التي تخفض نسبة الجلوكوز في الدم عن طريق الفم تكون قادرة على إنتاج نقص السكر في الدم. يرتبط تواتر نقص السكر في الدم بشدة مرض السكري ، ومستوى التحكم في نسبة السكر في الدم ، وخصائص المريض الأخرى. مرضى الشيخوخة والمرضى الذين يعانون من سوء التغذية ، والذين يعانون من قصور الغدة الكظرية أو الغدة النخامية أو القصور الكلوي الحاد هم أكثر عرضة لتأثير خفض الجلوكوز من هذه العلاجات. يمكن زيادة خطر نقص السكر في الدم عن طريق التمارين البدنية الشاقة ، تناول الكحول ، عدم كفاية السعرات الحرارية على أساس حاد أو مزمن ، أو مزيج من مضادات السكري عن طريق الفم الأخرى عملاء. قد يصعب التعرف على نقص السكر في الدم لدى مرضى الاعتلال العصبي اللاإرادي و / أو أولئك الذين يستخدمون حاصرات بيتا. يجب أن تدار Starlix® (nateglinide) قبل الوجبات لتقليل خطر نقص السكر في الدم. يجب على المرضى الذين يتخطون الوجبات أيضًا تخطي جرعتهم المقررة من Starlix لتقليل خطر نقص السكر في الدم.
القصور الكبدي: يجب استخدام Starlix بحذر عند المرضى الذين يعانون من أمراض الكبد متوسطة إلى شديدة لأن مثل هؤلاء المرضى لم تتم دراستهم.
فقدان السيطرة على نسبة السكر في الدم
قد يحدث فقدان مؤقت للتحكم في نسبة السكر في الدم مع الحمى أو العدوى أو الصدمة أو الجراحة. قد تكون هناك حاجة إلى العلاج بالأنسولين بدلاً من علاج Starlix في مثل هذه الأوقات. قد يحدث فشل ثانوي ، أو انخفاض فعالية Starlix على مدى فترة من الزمن.
معلومات للمرضى
يجب إطلاع المرضى على المخاطر والفوائد المحتملة لـ Starlix والأساليب البديلة للعلاج. وينبغي شرح مخاطر وإدارة نقص السكر في الدم. يجب أن يُطلب من المرضى تناول Starlix من 1 إلى 30 دقيقة قبل تناول الوجبة ، ولكن تخطي الجرعة المقررة إذا تخطوا الوجبة لتقليل خطر نقص السكر في الدم. ينبغي مناقشة التفاعلات الدوائية مع المرضى. يجب إخطار المرضى بالتفاعلات الدوائية المحتملة مع Starlix.
اختبارات المعمل
يجب تقييم الاستجابة للعلاج بشكل دوري باستخدام قيم الجلوكوز ومستويات HbA1C.
تفاعل الأدوية
يرتبط Nateglinide بدرجة كبيرة ببروتينات البلازما (98 ٪) ، وخاصة الألبومين. في دراسات النزوح في المختبر مع أدوية شديدة البروتين مثل فوروسيميد ، بروبرانولول ، كابتوبريل ، نيكارديبين ، برافاستاتين ، لم يظهر أي من الغليبيريد والوارفارين والفينيتوين وحمض أسيتيل الساليسيليك وتولبوتاميد وميتفورمين أي تأثير على مدى بروتين نيتكلينيد ربط. وبالمثل ، لم يكن لنتيجلاينيد أي تأثير على ارتباط بروتين المصل بالبروبرانولول ، والجليبورايد ، والنيكارديبين ، والوارفارين ، والفينيتوين ، وحمض أسيتيل الساليسيليك ، وتولبوتاميد في المختبر. ومع ذلك ، هناك ما يبرر التقييم الحكيم للحالات الفردية في الإعداد السريرية.
بعض الأدوية ، بما في ذلك العوامل المضادة للالتهابات غير الستيرويدية (مضادات الالتهاب غير الستيروئيدية) ، والساليسيلات ، ومثبطات أوكسيديز أحادي الأمين ، و عوامل حصر بيتا الأدرينالية غير الانتقائية قد تعمل على تحفيز عمل سكر الدم لدى ستارليكس ومضادات السكر الأخرى عن طريق الفم المخدرات.
بعض الأدوية بما في ذلك الثيازيدات والكورتيكوستيرويدات ومنتجات الغدة الدرقية ومحاكاة الودي قد تقلل من عمل سكر الدم لدى ستارليكس وغيره من الأدوية المضادة لمرض السكر عن طريق الفم.
عندما يتم إعطاء هذه الأدوية أو سحبها من المرضى الذين يتلقون Starlix ، يجب ملاحظة المريض عن كثب عن التغييرات في السيطرة على نسبة السكر في الدم.
المخدرات / التفاعلات الغذائية
لم تتأثر الحرائك الدوائية للناتكلينيد بتكوين الوجبة (نسبة عالية من البروتين أو الدهون أو الكربوهيدرات). ومع ذلك ، تم تخفيض مستويات البلازما الذروة بشكل كبير عندما تم إعطاء Starlix قبل 10 دقائق من تناول وجبة سائلة. لم يكن لـ Starlix أي تأثير على إفراغ المعدة في الأشخاص الأصحاء كما تم تقييمها بواسطة اختبار الأسيتامينوفين.
التسرطن / الطفرات / ضعف الخصوبة
التسرطن: أجريت دراسة مسرطنة مدتها سنتان في فئران سبراغ داولي بجرعات عن طريق الفم من نيتللايد يصل إلى 900 ملغ / كغ / يوم ، مما أدى إلى التعرض للمفوضية في الفئران من الذكور والإناث ما يقرب من 30 و 40 أضعاف التعرض البشري العلاجي على التوالي مع جرعة Starlix الموصى بها من 120 ملغ ، ثلاث مرات يوميا قبل وجبات. أجريت دراسة سرطانية لمدة عامين في الفئران B6C3F1 مع جرعات عن طريق الفم من nateglinide تصل إلى 400 ملغ / كغ / يوم ، والتي أنتجت التعرض AUC في الذكور والفئران الإناث حوالي 10 و 30 ضعف التعرض البشري العلاجي بجرعة Starlix الموصى بها من 120 ملغ ، ثلاث مرات يوميا قبل وجبات الطعام. لم يتم العثور على دليل على وجود ورم في أي من الفئران أو الفئران.
الطفرات: لم يكن Nateglinide سامًا جينياً في اختبار Ames في المختبر ، أو فحص سرطان الغدد الليمفاوية في الماوس ، أو اختبار انحراف الكروموسوم في خلايا الرئة في الهامستر الصيني ، أو في اختبار النواة المجهرية للماوس.
ضعف الخصوبة: لم تتأثر الخصوبة بإعطاء nateglinide للفئران بجرعات تصل إلى 600 مجم / كجم (حوالي 16 مرة من التعرض العلاجي البشري بجرعة Starlix الموصى بها من 120 ملغ ثلاث مرات يوميا من قبل وجبات).
حمل
الحمل الفئة C
لم يكن Nateglinide مسخًا في الجرذان بجرعات تصل إلى 1000 ملغم / كغم (حوالي 60 مرة من التعرض العلاجي البشري بجرعة Starlix الموصى بها من 120 ملغ ، ثلاث مرات يوميًا قبل الوجبات). في الأرانب ، تأثر النمو الجنيني سلبا وتزايدت الإصابة بالمرارة المرارية أو المرارة الصغيرة عند جرعة 500 ملغ / كغ (حوالي 40 مرة من التعرض العلاجي البشري مع جرعة ستارليكس الموصى بها من 120 ملغ ، ثلاث مرات يوميا قبل وجبات). لا توجد دراسات كافية وتسيطر عليها بشكل جيد في النساء الحوامل. لا ينبغي أن تستخدم Starlix أثناء الحمل.
العمل و الانجاز
تأثير Starlix على المخاض والولادة عند البشر غير معروف.
الأمهات المرضعات
أظهرت الدراسات التي أجريت على الفئران المرضعة أن النتلاينيد يفرز في اللبن. كانت نسبة AUC0-48h في الحليب إلى البلازما حوالي 1: 4. خلال فترة ما بعد الولادة وما بعدها ، كانت أوزان الجسم أقل في ذرية الفئران التي تعطى nateglinide عند 1000 مغ / كغ (حوالي 60 مرة من التعرض العلاجي البشري بجرعة Starlix الموصى بها من 120 ملغ ، ثلاث مرات يوميا من قبل وجبات). ليس من المعروف ما إذا كان Starlix يفرز في حليب الإنسان. نظرًا لأن العديد من الأدوية تفرز في حليب الإنسان ، لا ينبغي إعطاء ستارليكس إلى امرأة تمريض.
استخدام الأطفال
لم تثبت سلامة وفعالية ستارليكس في مرضى الأطفال.
استخدام المسنين
لم يلاحظ أي اختلافات في سلامة أو فعالية Starlix بين المرضى الذين تتراوح أعمارهم بين 65 وما فوق ، وأقل من 65 سنة. ومع ذلك ، لا يمكن استبعاد حساسية أكبر لبعض الأفراد الأكبر سنا للعلاج Starlix.
أعلى
ردود الفعل السلبية
في التجارب السريرية ، تم علاج ما يقرب من 2600 مريض يعانون من مرض السكري من النوع 2 مع Starlix® (nateglinide). من هؤلاء ، تم علاج حوالي 1،335 مريض لمدة 6 أشهر أو أكثر وحوالي 190 مريض لمدة سنة واحدة أو أكثر.
كان نقص السكر في الدم غير شائع نسبيًا في جميع علاجات التجارب السريرية. 0.3 ٪ فقط من مرضى Starlix توقفوا بسبب نقص السكر في الدم. لم تكن أعراض الجهاز الهضمي ، وخاصة الإسهال والغثيان ، أكثر شيوعًا في المرضى الذين يستخدمون مزيجًا من Starlix والميتفورمين أكثر من المرضى الذين يتلقون الميتفورمين فقط. وبالمثل ، لم تكن الوذمة المحيطية أكثر شيوعًا في المرضى الذين يستخدمون مزيجًا من Starlix و rosiglitazone مقارنة بالمرضى الذين يتلقون روزيجليتازون وحدهم. يسرد الجدول التالي الأحداث التي حدثت بشكل متكرر في مرضى Starlix أكثر من المرضى الوهميين في تجارب سريرية محكومة.
الأحداث الضائرة الشائعة (حوالي 2 ٪ في مرضى Starlix®) في تجارب العلاج الأحادي Starlix® (٪ من المرضى)
| الوهمي | Starlix® | |
| N = 458 | N = 1441 | |
| المدة المفضلة | ||
| عدوى الجهاز التنفسي العلوي | 8.1 | 10.5 |
| ألم في الظهر | 3.7 | 4.0 |
| أعراض الانفلونزا | 2.6 | 3.6 |
| دوخة | 2.2 | 3.6 |
| المفاصل | 2.2 | 3.3 |
| إسهال | 3.1 | 3.2 |
| الصدمة العرضية | 1.7 | 2.9 |
| التهاب شعبي | 2.6 | 2.7 |
| يسعل | 2.2 | 2.4 |
| نقص سكر الدم | 0.4 | 2.4 |
خلال تجربة ما بعد التسويق ، تم الإبلاغ عن حالات نادرة من تفاعلات فرط الحساسية مثل الطفح الجلدي والحكة والشرى. وبالمثل ، تم الإبلاغ عن حالات من اليرقان والتهاب الكبد الصفراوي وأنزيمات الكبد المرتفعة.
تشوهات المختبر
حمض اليوريك: كانت هناك زيادة في متوسط مستويات حمض اليوريك للمرضى الذين عولجوا بـ Starlix وحدهم ، و Starlix في تركيبة مع الميتفورمين ، والميتفورمين وحده ، وغليبيريد وحده. وكانت الاختلافات المعنية من الدواء الوهمي 0.29 ملغ / ديسيلتر ، 0.45 ملغ / ديسيلتر ، 0.28 ملغ / ديسيلتر ، و 0.19 ملغ / ديسيلتر. الأهمية السريرية لهذه النتائج غير معروفة.
أعلى
جرعة زائدة
في دراسة سريرية على مرضى السكري من النوع 2 ، كانت تدار Starlix® (nateglinide) في زيادة جرعات تصل إلى 720 ملغ يوميا لمدة 7 أيام ولم تكن هناك أحداث سلبية هامة سريريا ذكرت. لم تكن هناك حالات جرعة زائدة من Starlix في التجارب السريرية. ومع ذلك ، قد تؤدي الجرعة الزائدة إلى تأثير مبالغ فيه لخفض نسبة الجلوكوز مع ظهور أعراض انخفاض السكر في الدم. يجب أن تعالج أعراض نقص السكر في الدم دون فقدان الوعي أو النتائج العصبية مع الجلوكوز عن طريق الفم والتعديلات في أنماط الجرعة و / أو الوجبة. يجب علاج تفاعلات سكر الدم الشديدة مع الغيبوبة أو النوبات العصبية أو غيرها من الأعراض العصبية بالجلوكوز في الوريد. نظرًا لأن nateglinide شديد الارتباط بالبروتين ، فإن غسيل الكلى ليس وسيلة فعالة لإزالته من الدم.
أعلى
الجرعة والإدارة
يجب أن تؤخذ Starlix® (nateglinide) قبل دقيقة إلى 30 دقيقة من الوجبات.
حيد والجمع بين الميتفورمين أو ثيازوليدينيديون
جرعة البدء والصيانة الموصى بها من Starlix ، بمفردها أو بالاشتراك مع الميتفورمين أو الثيازيدوليدين ، 120 ملغ ثلاث مرات يوميًا قبل الوجبات.
يمكن استخدام جرعة 60 ملغ من Starlix ، سواء بمفردها أو بالاشتراك مع الميتفورمين أو الثيازيدوليدين ، في المرضى الذين يكونون بالقرب من الهدف HbA1C عند بدء العلاج.
جرعة في مرضى الشيخوخة
لا تعديلات الجرعة الخاصة وعادة ما تكون ضرورية. ومع ذلك ، لا يمكن استبعاد حساسية أكبر من بعض الأفراد للعلاج Starlix.
الجرعة في القصور الكلوي والكبد
ليس هناك حاجة لتعديل الجرعة في المرضى الذين يعانون من قصور كلوي خفيف إلى شديد أو في المرضى الذين يعانون من قصور كبدي خفيف. لم يتم دراسة الجرعات من المرضى الذين يعانون من اختلال وظيفي كبدي معتدلة إلى شديدة. لذلك ، يجب استخدام Starlix بحذر في المرضى الذين يعانون من مرض الكبد من المعتدل إلى الحاد (انظر الاحتياطات ، ضعف الكبد).
أعلى
كيف زودت
أقراص Starlix® (nateglinide)
60 ملغ
تابلت ذو حافة مستديرة من القرنفل ومزخرف بأوراق "Starlix" على جانب واحد و "60" من الجانب الآخر.
زجاجات من 100... NDC 0078-0351-05
120 ملغ
قرص أصفر بيضاوي الشكل مع "Starlix" تم نزعه على جانب و "120" من الجانب الآخر.
زجاجات من 100... NDC 0078-0352-05
تخزين
متجر في 25 درجة مئوية (77 درجة فهرنهايت) ؛ الرحلات المسموح بها إلى 15 درجة مئوية إلى 30 درجة مئوية (59 درجة مئوية إلى 86 درجة مئوية).
الاستغناء في وعاء ضيق ، جامعة جنوب المحيط الهادئ.
T2008-01
REV: يوليو 2008
صنع بواسطة:
نوفارتيس فارما شتاين
شتاين ، سويسرا
موزع من قبل:
شركة نوفارتيس للأدوية
شرق هانوفر ، نيو جيرسي 07936
© شركة نوفارتيس
آخر تحديث 07/2008
Starlix ، nateglinide ، معلومات كاملة للمريض (في سهل الانجليزية)
معلومات مفصلة عن العلامات والأعراض والأسباب والعلاج من مرض السكري
لا تهدف المعلومات الواردة في هذه الدراسة إلى تغطية جميع الاستخدامات أو الاتجاهات أو الاحتياطات الممكنة أو التفاعلات الدوائية أو الآثار الضارة. هذه المعلومات معممة ولا تهدف إلى تقديم المشورة الطبية المحددة. إذا كانت لديك أسئلة حول الأدوية التي تتناولها أو ترغب في مزيد من المعلومات ، فاستشر طبيبك أو الصيدلي أو الممرض.
ارجع الى: تصفح جميع الأدوية لمرض السكري


